深入解析了 2026 年 ADA 指引中 SGLT 抑制劑(SGLT Inhibitors)角色的重大演變。這不僅是藥物使用順序的調整,更是一場從單一器官保護轉向 「心-腎-代謝(Cardio-Renal-Metabolic, CKM)」 整體照護的哲學變革。
1: SGLT2 抑制劑的典範轉移——邁向 CKM 整體治療

2026 年的指引標誌著 SGLT2 抑制劑在臨床定位上的根本性轉變。過去我們傾向將其視為單純的降糖藥或單一器官(心臟或腎臟)的保護劑,但現在的概念已進化為維護 「心-腎-代謝(CKM)」 健康系統的核心基石。這份手冊旨在協助臨床專家理解這一典範轉移,從關注單一疾病點,擴展到對心血管、腎臟與代謝系統進行全面性的聯合防護。
2: 2026 年的三大核心轉變——重新思考 SGLT 抑制劑

指引更新體現了三個決定性的臨床思維轉變:
- 從單兵作戰轉向聯合治療(From Solo to Combo): SGLT2i 不再是心衰竭(HFpEF)或慢性腎病(CKD)的唯一主角,指引現在強調它與 GLP-1 RA 或 GIP/GLP-1 RA 處於「平行」甚至「聯合」的地位,需依據患者表型進行組合治療。
- 從模糊地帶走向明確指令(From Ambiguity to Certainty): 過去臨床上對於「肌酸酐初期上升是否停藥」或「腎功能極差時是否續用」常有疑慮,現在這些慣例已被正式寫入 A 級推薦,確認了不應因肌酸酐短期波動停藥,且應持續用藥至透析前一刻,提供了堅實的法律與臨床依據。
- 從特定藥物擴展至廣泛機制(From Specific to Broad): 術語從 "SGLT2 inhibitors" 擴大為 "SGLT inhibitors",正式納入 SGLT1/2 雙重抑制劑(如 Sotagliflozin),確立了「抑制 SGLT 機制」本身的核心治療價值。
3: CKD 關鍵更新 (1)——「續用至腎衰竭」寫入 Grade A 推薦

這是一個對腎臟科與基層醫師極為重要的法律與臨床保障。在 2025 年以前,指引僅建議在 eGFR ≥ 20 時「起始」使用,至於能否用到洗腎,往往僅存在於圖表註腳,證據位階不明確。
到了 2026 年,指引在內文以 Grade A 的最高證據等級 明確指出:雖然起始治療仍需 eGFR ≥ 20,但一旦啟用後,即便 eGFR 跌破 20,仍應 「安全地續用直至腎衰竭(safely continue until kidney failure)」。這意味著醫師在患者 eGFR 降至 15 或更低時,擁有強力的指引背書可繼續處方以延緩透析,直到患者真正進入長期透析或移植為止。
4: CKD 關鍵更新 (2)——治療演算法重組,GLP-1 RA 晉升第一線
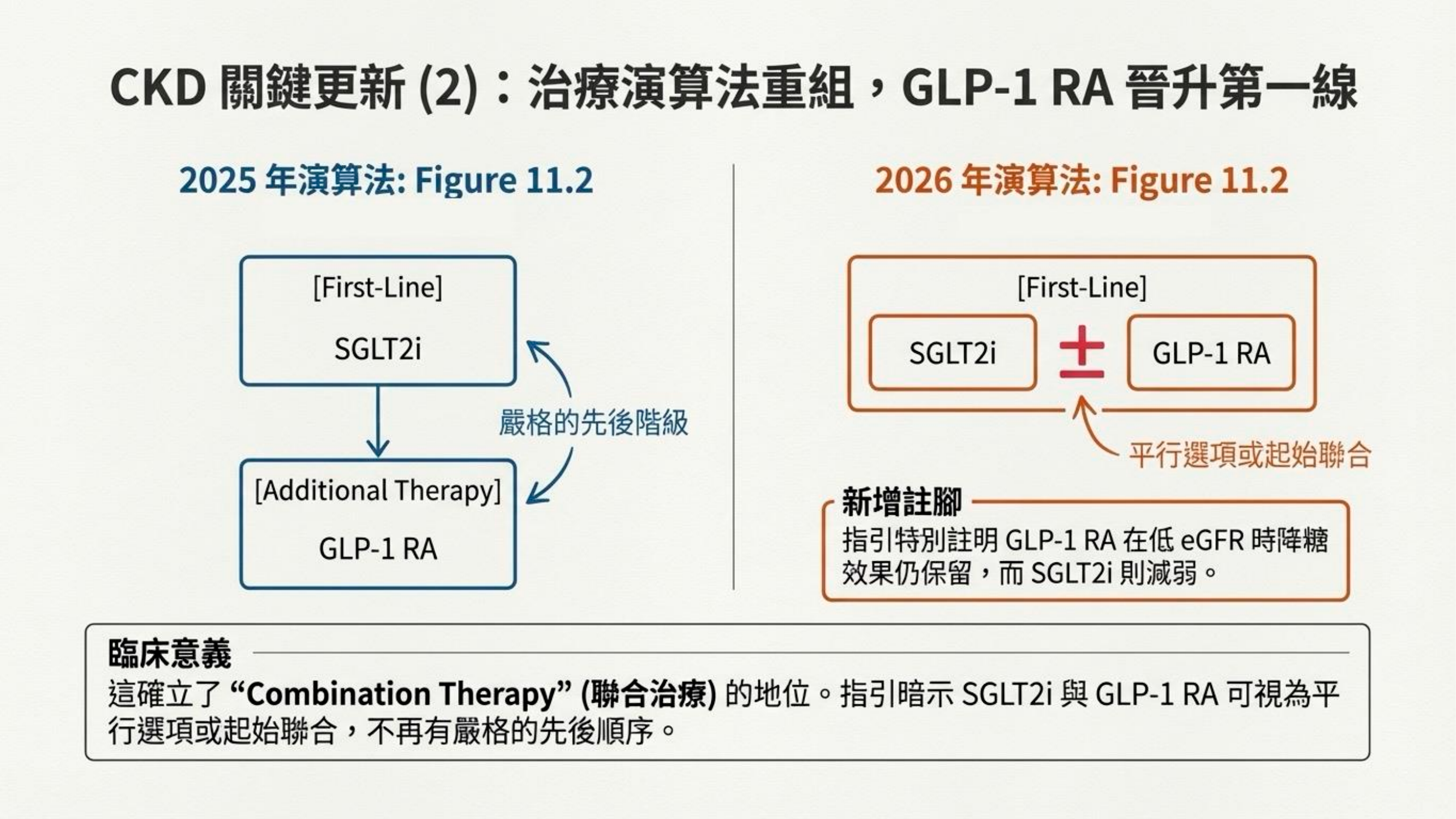
腎臟病治療的演算法出現了結構性的重組。過去 SGLT2i 是絕對的第一線,GLP-1 RA 往往被視為次要的「疊加選項」或「替代品」。但在 2026 年的演算法中,GLP-1 RA 被提升至與 SGLT2i 並列的位置,兩者皆為 「第一線藥物(First-Line)」。
這確立了 「聯合治療(Combination Therapy)」 的新標準。指引特別註明,當 eGFR 較低時(<45),SGLT2i 的降糖效果會減弱,但 GLP-1 RA 仍能保持療效。因此,臨床上不再有嚴格的先後階級,SGLT2i 與 GLP-1 RA 可視為平行選項,甚至鼓勵在治療初期就進行 「起始聯合」,以同時獲得兩種機轉的器官保護。
5: CKD 關鍵更新 (3&4)——安全性免責與藥物等效宣言

針對臨床上最讓醫師糾結的「用藥後肌酸酐上升(eGFR Dip)」,2026 年指引給予了明確的「免責條款」。指引新增文字指出,SGLT2i 啟動後出現的肌酸酐上升(30% 以內)屬於 「血液動力學改變(Hemodynamic changes)」,類似於 ACEi/ARB 的反應,並下達了強硬指令:「藥物不應因此被停用(medication should not be discontinued)」。
此外,指引也發布了 Empagliflozin 與 Dapagliflozin 的「等效宣言」。官方引用新數據認證這兩款藥物在六年的長期追蹤下,其護腎效果是 「可比擬的(comparable)」。這確認了護腎效果屬於 類別效應(Class Effect),讓臨床醫師在選藥時能更靈活,不必過度糾結於單一藥物的個別試驗差異。
6: CKD 關鍵更新 (5)——蛋白尿(Albuminuria)的角色升級

這是一個概念上的重大昇華。過去我們將蛋白尿視為腎臟風險的指標(Risk Marker),但在 2026 年,指引將其地位提升為 「療效中介因子(Therapeutic Mediator)」。指引明確指出,SGLT2i 與 Finerenone 的大部分臨床獲益,其實是 「透過減少蛋白尿來介導的(mediated by reduction in albuminuria)」。
在臨床應用上,這意味著蛋白尿的下降不僅是數字好看,更是藥物發揮心腎保護機制的核心。若患者在使用 SGLT2i 後,UACR(尿液白蛋白/肌酸酐比值)未見改善,這暗示該患者可能未能從藥物中獲得最大的保護效果,醫師需考量採取更積極的手段,如強化限鹽飲食或增加其他藥物。
7: 心血管(CV)關鍵更新——從 "SGLT2i" 到 "SGLT Inhibitors" 的定義擴張
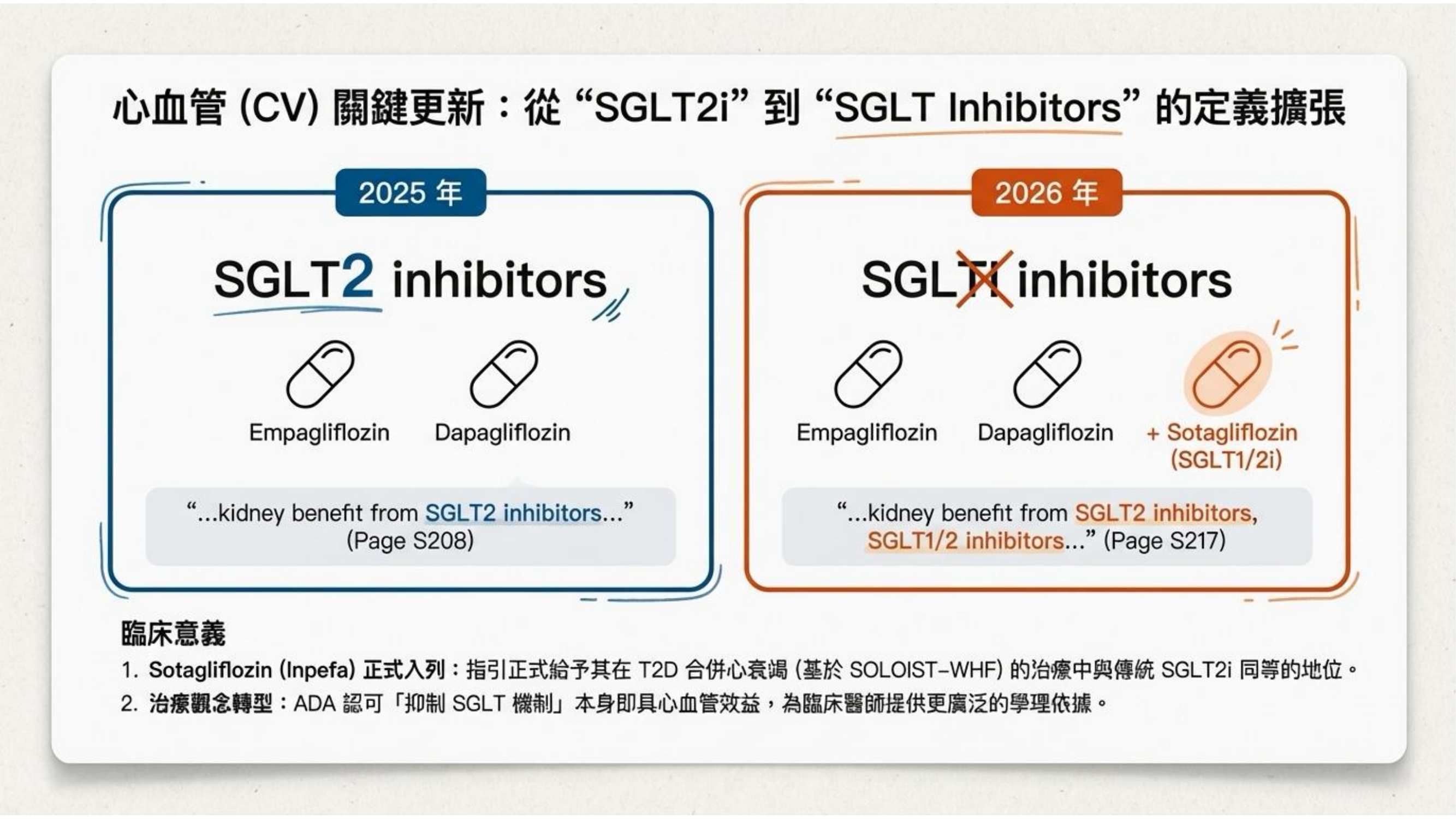
在心血管章節,指引的標題與內文發生了微妙但關鍵的變化:從 "SGLT2 inhibitors" 擴展為 "SGLT inhibitors"。這主要是為了正式納入 Sotagliflozin(SGLT1/2 雙重抑制劑)。基於 SOLOIST-WHF 試驗的結果,指引給予 Sotagliflozin 在第二型糖尿病合併心衰竭治療中,與傳統 SGLT2i 同等的地位。
這代表 ADA 正式認可 「抑制 SGLT 機制」——無論是選擇性抑制 SGLT2 還是雙重抑制 SGLT1/2——本身即具備心血管效益。對於臨床醫師而言,這擴大了治療武器庫,提供了更廣泛的學理依據來選擇藥物。
8: 關鍵更新——高血壓章節的「安全性指引分流」
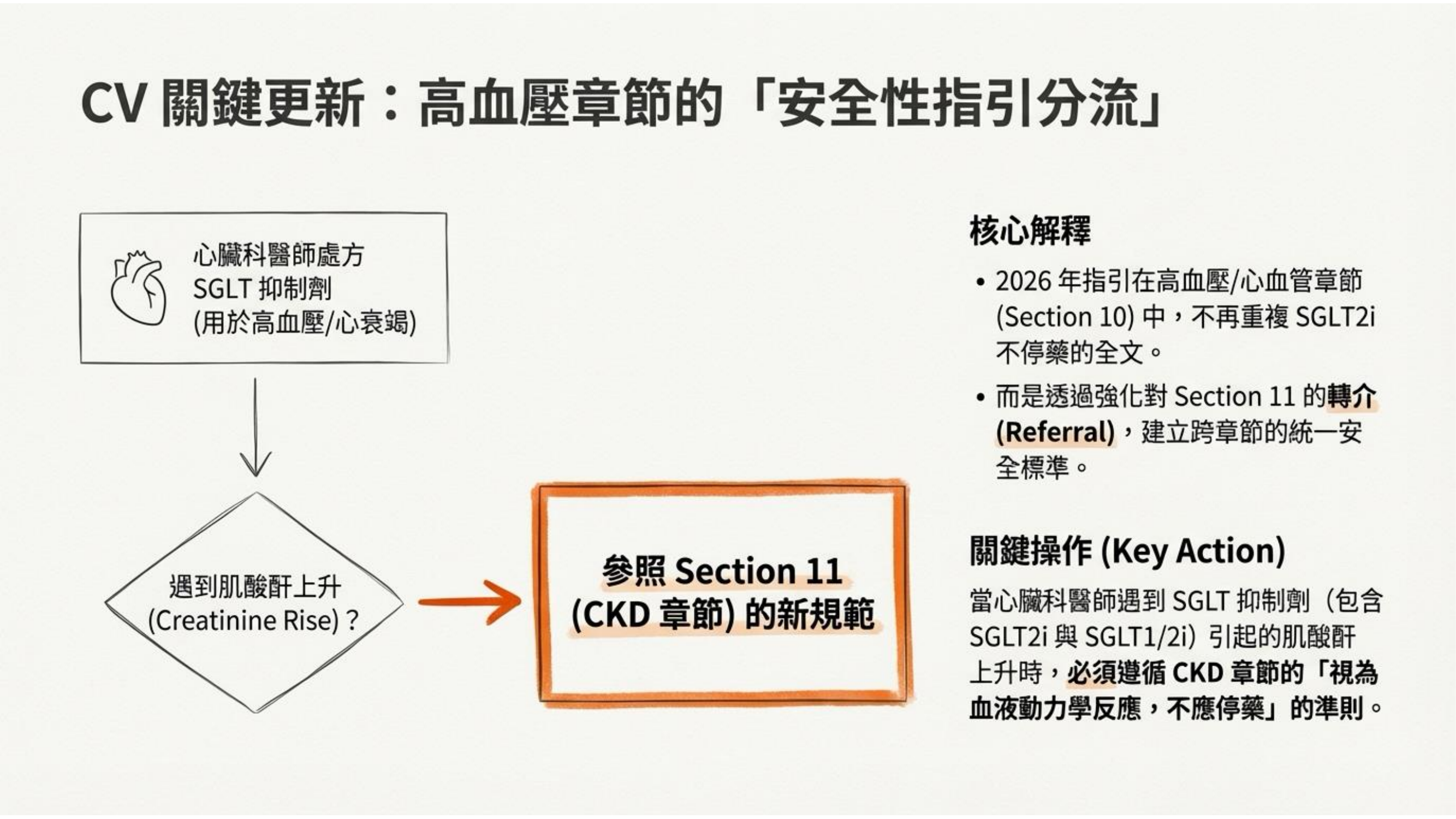
為了避免指引內容重複並建立統一標準,2026 年指引在高血壓與心血管章節(Section 10)做了一個操作性的調整。當心臟科醫師處方 SGLT 抑制劑遇到肌酸酐上升時,指引不再重複解釋,而是直接要求 「參照 Section 11(CKD 章節)的新規範」。
這個「轉介(Referral)」動作強化了跨科別的安全性標準。無論是心臟科還是腎臟科醫師,面對 SGLT 抑制劑引起的肌酸酐上升,都必須遵循同一準則:將其視為良性的血液動力學反應,並堅守 「不應停藥」 的底線。
9: T2D 治療變革 (1)——HFpEF 合併肥胖,SGLT2i 不再單打獨鬥
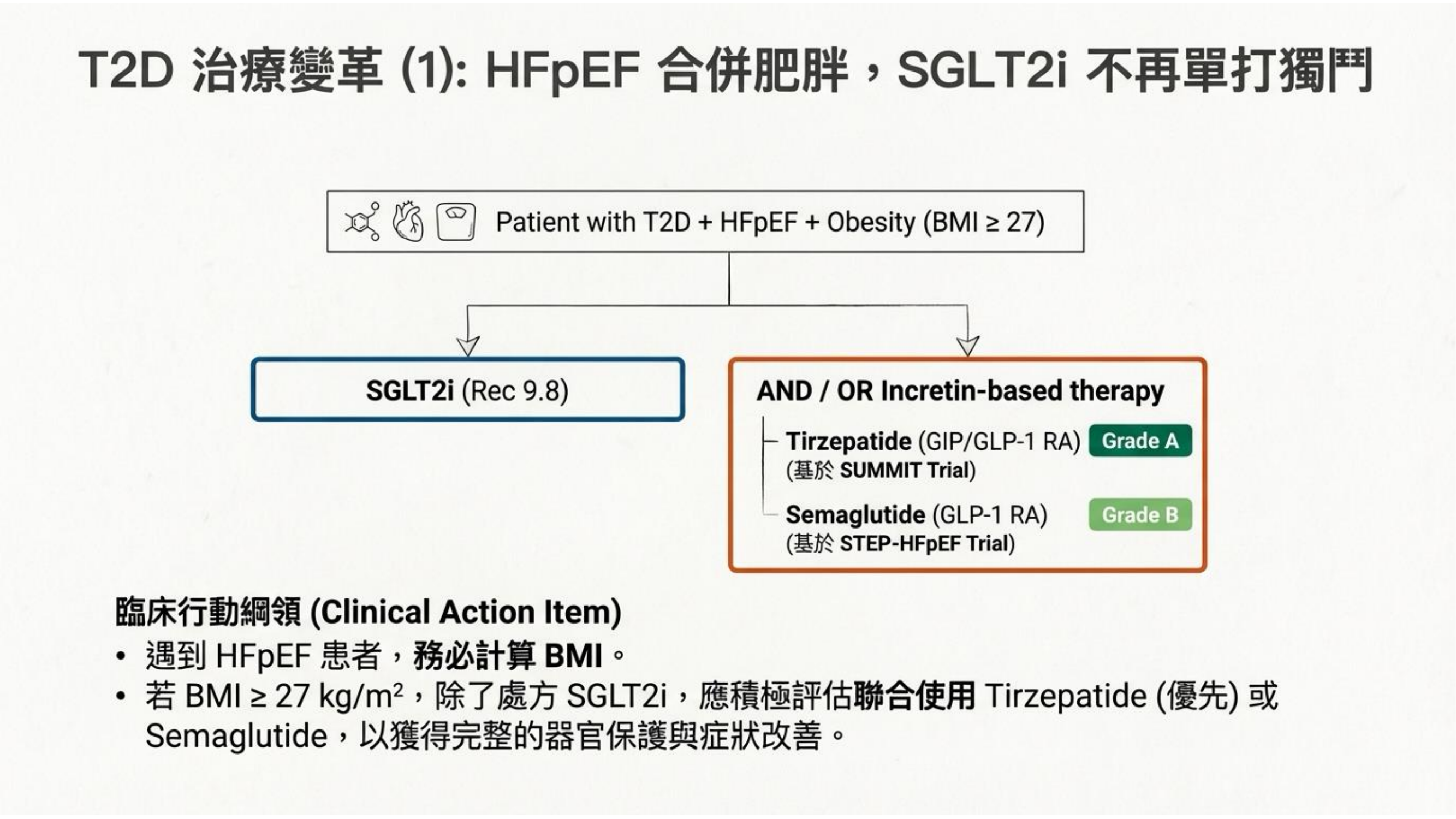
針對 第二型糖尿病合併 HFpEF 且肥胖(BMI ≥ 27) 的患者,治療策略已從單一藥物轉向聯合治療。過去 SGLT2i 是唯一主角,但在 2026 年,指引建議除了處方 SGLT2i,應積極評估 聯合使用腸泌素療法(Incretin-based therapy)。
其中,Tirzepatide 基於 SUMMIT 試驗降低心衰竭事件的成果,獲得了 Grade A 的最高推薦;而 Semaglutide 則基於 STEP-HFpEF 試驗改善症狀的成果,獲得 Grade B 推薦。臨床醫師在面對此類患者時,務必計算 BMI,若符合標準,應主動採取 SGLT2i + Incretin 的組合,以獲得完整的器官保護與症狀改善。
10: T2D 治療變革 (2)——FLOW 試驗確立 GLP-1 RA 的 CKD 雙支柱地位
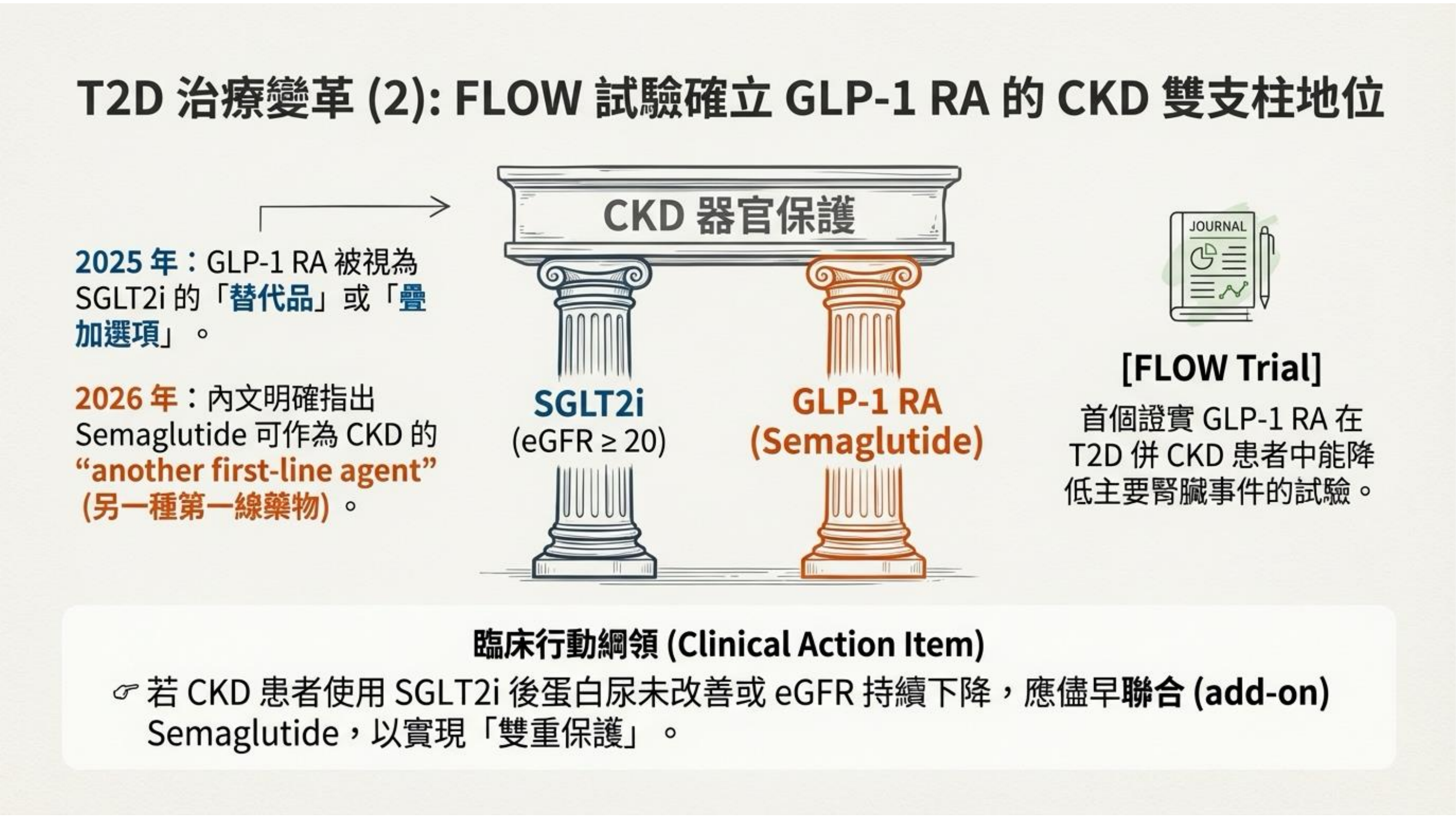
FLOW 試驗的成功,徹底改變了 GLP-1 RA 在腎臟病治療中的地位。過去它被視為 SGLT2i 的替代品,現在指引明確指出 Semaglutide 可作為 CKD 的 「另一種第一線藥物(another first-line agent)」。這意味著 GLP-1 RA 正式成為 CKD 治療的 「雙支柱」 之一。
這直接強化了臨床上的聯合治療策略。若 CKD 患者(eGFR ≥ 20)在使用 SGLT2i 後,蛋白尿仍未改善或腎功能持續惡化,醫師應儘早 聯合(add-on) Semaglutide,利用其獨立的腎臟保護機制,實現對腎臟的「雙重保護」,而非被動等待病情惡化。
11: T2D 治療變革 (3)——更嚴格的安全規範與新的應用場景

本頁強調了安全規範的升級與新適應症的拓展。在安全性方面,針對 生酮飲食(Ketogenic diet) 引發 DKA 的風險,指引語氣從過去的「建議衛教」轉強為 「強烈建議醫療人員勸阻(discourage)」。臨床醫師在開立 SGLT2i 前,必須詢問飲食習慣,若患者堅持生酮飲食,則不應處方此藥。
在新應用場景方面,指引新增推薦,指出針對癌症治療中 PI3K 抑制劑(如 Alpelisib) 引起的高血糖,SGLT2i 可作為 Metformin 之後的二線或三線治療選項。但需特別注意,此類患者使用 SGLT2i 時需嚴密監測酮體,以防範 DKA 風險。
12: 實戰精粹——晚期 CKD 至透析的「藥物退場與接手」機制

指引為晚期 CKD 患者建立了一套清晰的 「退場與接手」 機制。對於 晚期 CKD(eGFR < 30 但未透析) 的患者,策略是 「續用(若已在用)」 SGLT2i,這是基於 Grade A 的證據;同時,GLP-1 RA 在此階段為 「首選(Preferred)」,可新開立或續用(基於 FLOW 試驗 Grade B 證據)。
當患者 進入透析(Dialysis) 後,SGLT2i 必須 「停用(Stop)」,正式退場。此時,指引(Grade C)建議 「啟動或續用」 GLP-1 RA 來接手心血管保護的任務。這填補了 SGLT2i 依規定停藥後的治療空窗,構建出完整的連續性照護路徑。
13: 驅動變革的關鍵新證據——三大試驗速覽
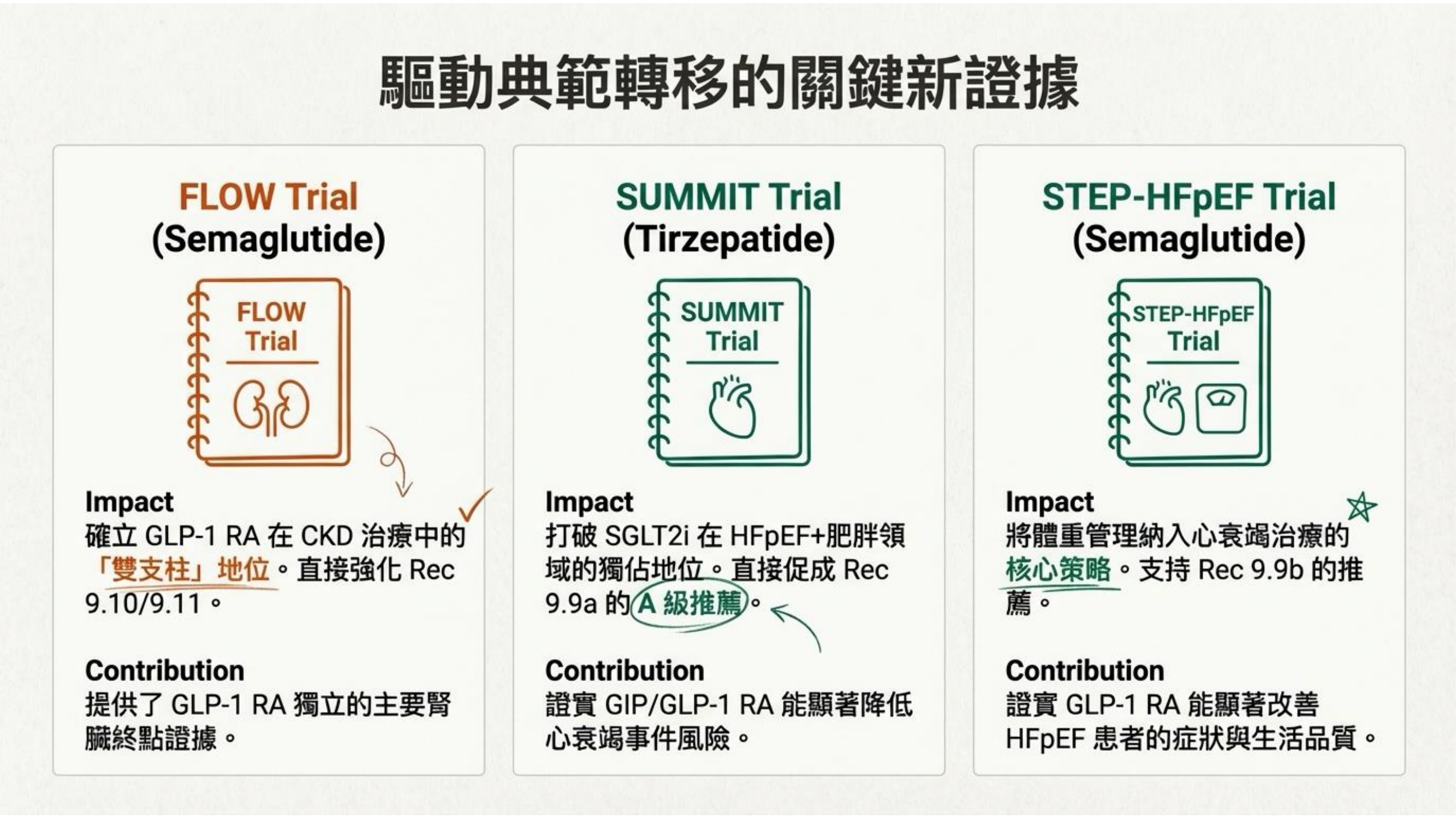
2026 年指引的變革是由三個關鍵試驗所驅動的:
- FLOW 試驗: 提供了 Semaglutide 獨立的主要腎臟終點證據,確立了其在 CKD 治療中的「雙支柱」地位。
- SUMMIT 試驗: 證實 Tirzepatide 能顯著降低心衰竭事件風險,打破了 SGLT2i 在 HFpEF 合併肥胖領域的獨佔地位,直接促成了 Grade A 的推薦。
- STEP-HFpEF 試驗: 證實 Semaglutide 能顯著改善症狀與生活品質,支持了將體重管理納入心衰竭治療的核心策略。
14: 2026 SGLT 抑制劑臨床操作手冊 (SOP)

這張表總結了 2026 年的新標準操作程序:
- 藥物選擇: Sotagliflozin 正式入列,Empa/Dapa 護腎效果被視為相等。
- 聯合治療: CKD 患者應積極考慮 SGLT2i 加 GLP-1 RA,HFpEF 合併肥胖者則務必評估 SGLT2i 加 Incretin。
- 安全性: 啟動後的肌酸酐上升應視為血液動力學反應而不停藥;並強烈勸阻生酮飲食。
- 退場與接手: SGLT2i 應持續使用至腎衰竭(透析/移植)才停用,透析後則由 GLP-1 RA 接手進行心血管保護。
15: 結語——超越降糖,SGLT 抑制劑作為 CKM 健康的基石
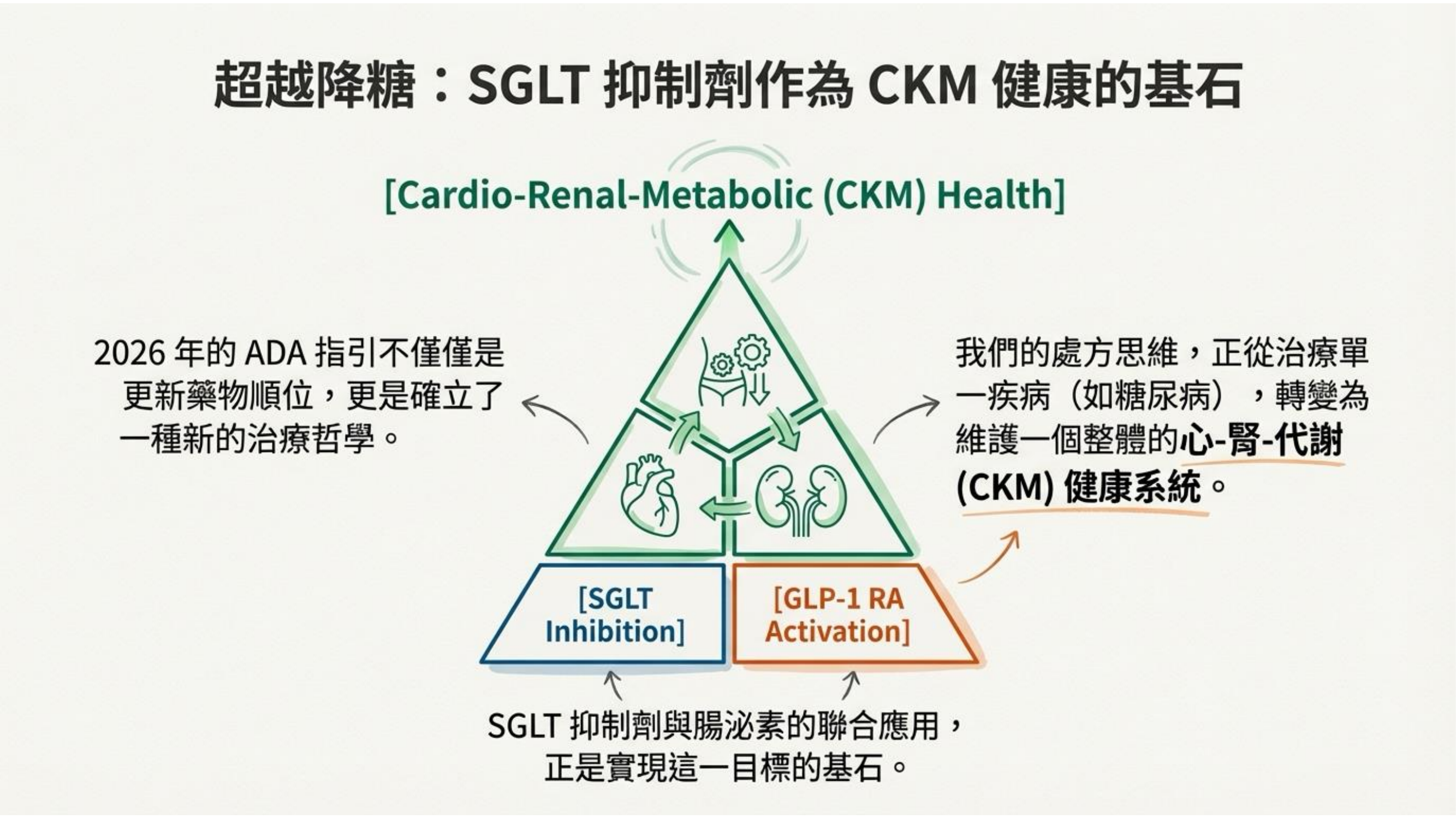
總結來說,2026 年的 ADA 指引不僅僅是更新藥物順位,更是確立了一種新的治療哲學。SGLT 抑制劑與腸泌素(GLP-1 RA)的聯合應用,正是實現 「心-腎-代謝(Cardio-Renal-Metabolic, CKM)」 健康目標的基石。
我們的處方思維,正從治療單一疾病(如糖尿病),轉變為維護一個整體的健康系統。透過 「SGLT 抑制(Inhibition)」 與 「GLP-1 RA 活化(Activation)」 的雙重機制,我們能為患者提供更全面、更長遠的器官保護。