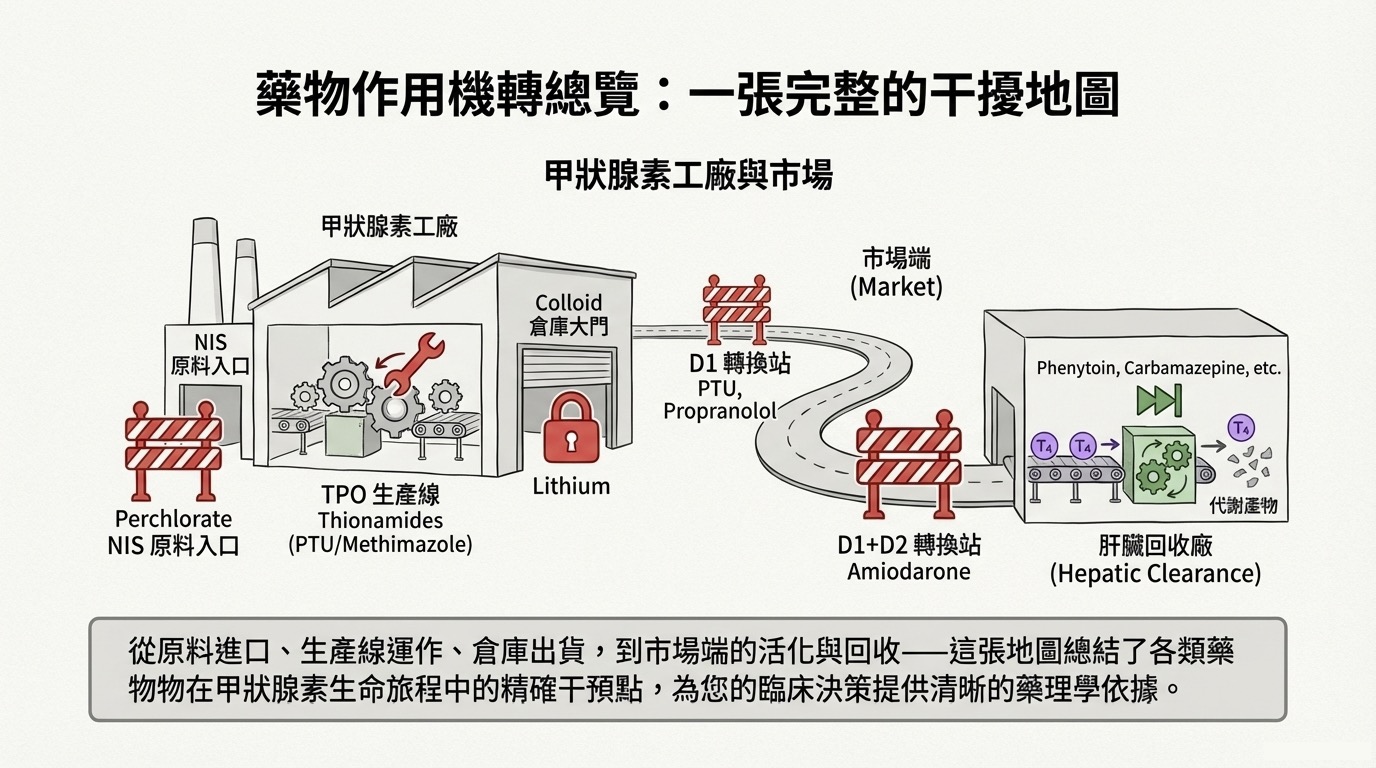
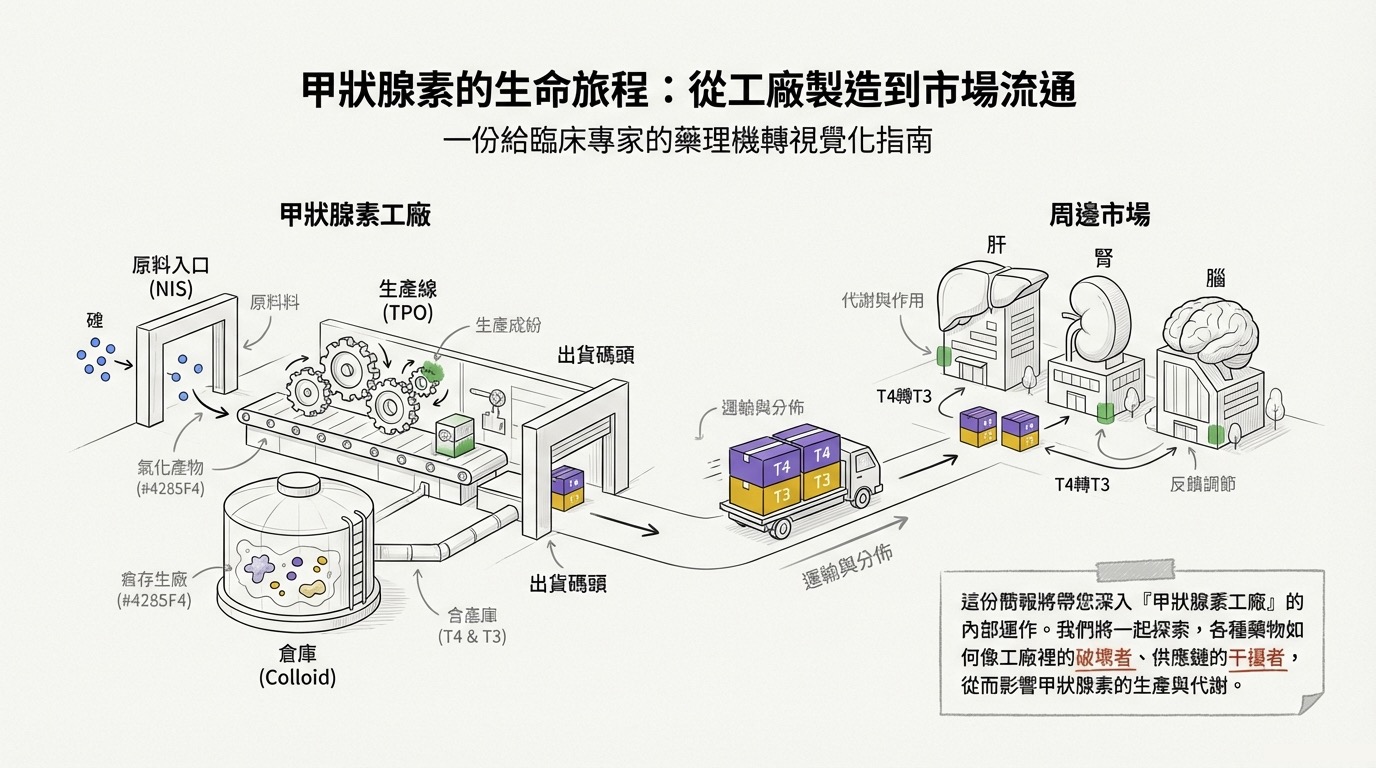
甲狀腺生理受到藥物的干擾主要發生在兩個戰場:一是甲狀腺濾泡細胞內的「生產與出貨(合成與分泌)」,二是周邊組織的「代謝與轉換」。理解這些機制,是精準調控甲狀腺疾病與迴避藥物交互作用的關鍵。
第一部分:抑制合成與分泌的藥物 (Synthesis and Secretion)
這類藥物直接作用於甲狀腺濾泡細胞,導致工廠「停工」或產品「無法出貨」。主要分為三大類機制:
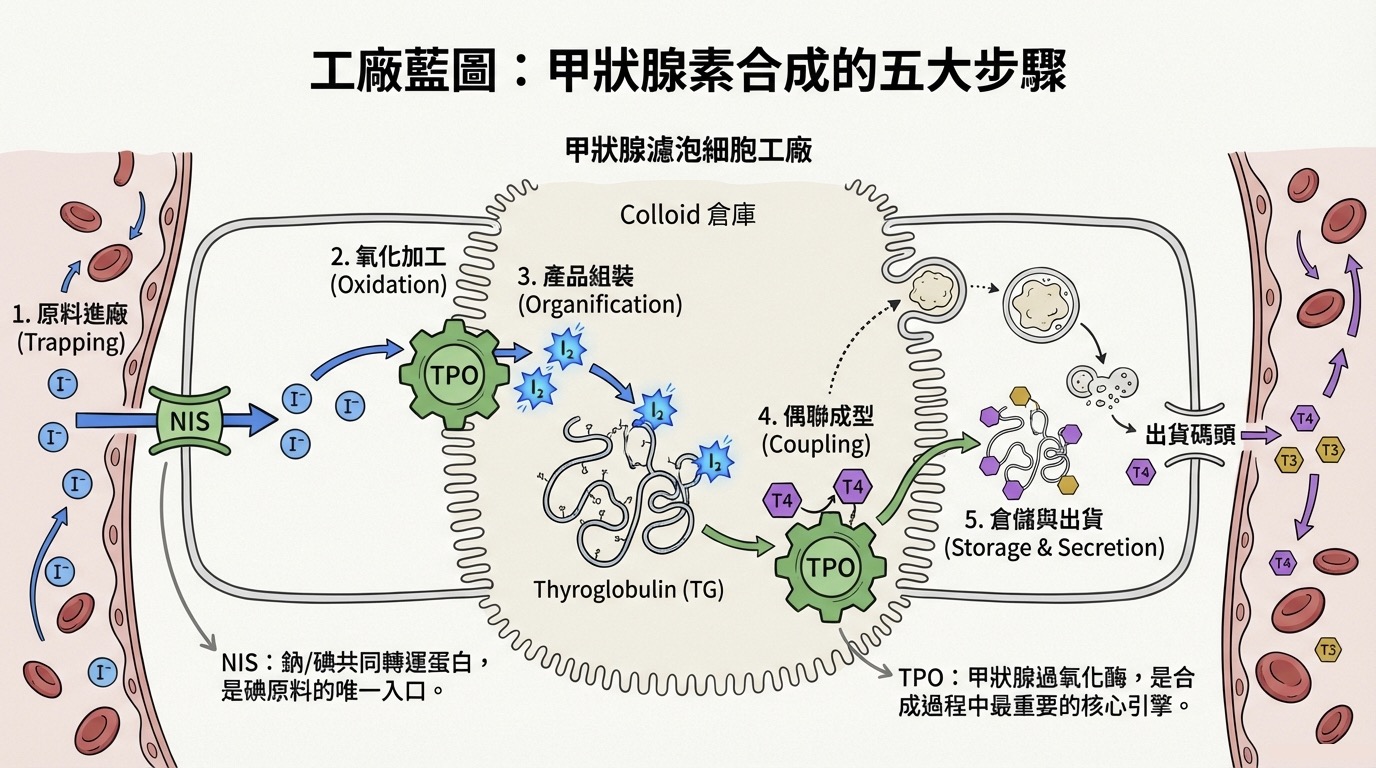
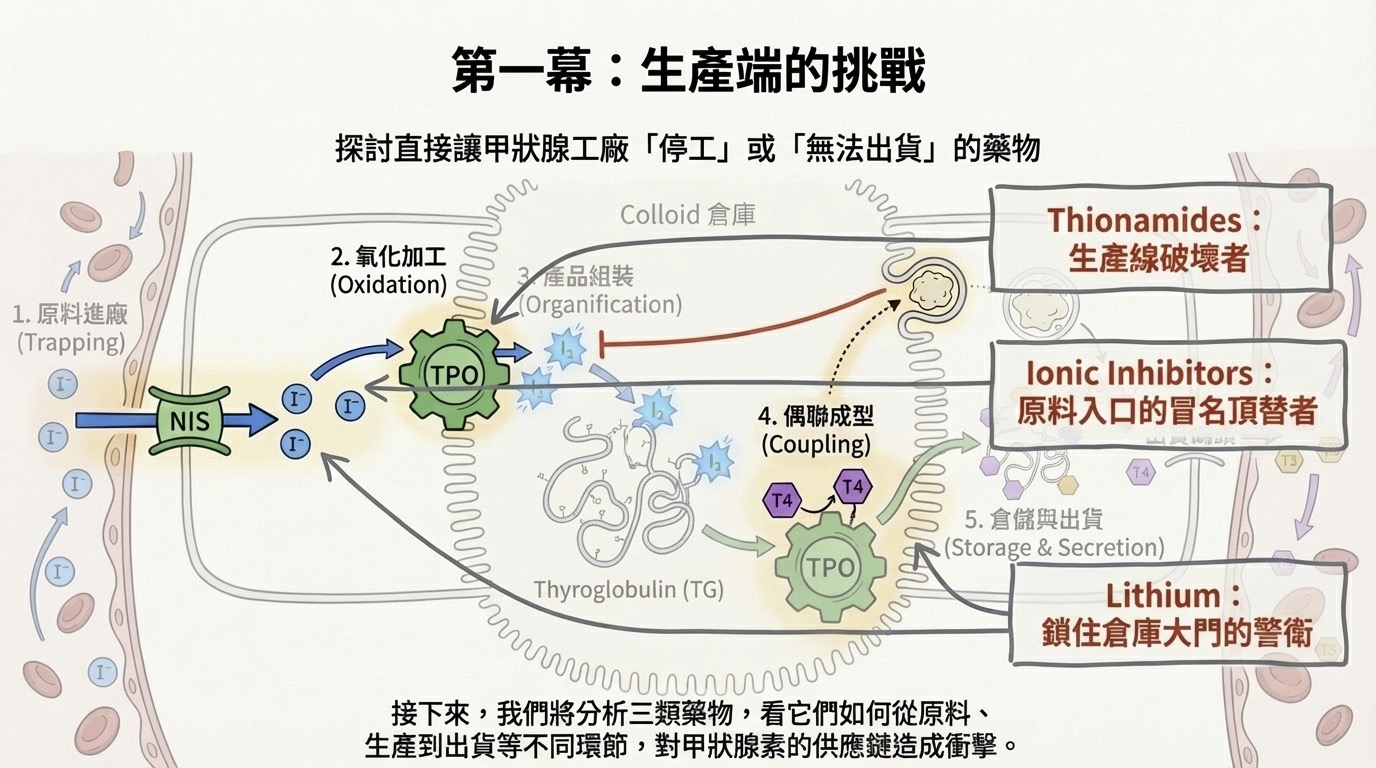
1. Thionamides (抗甲狀腺藥物)
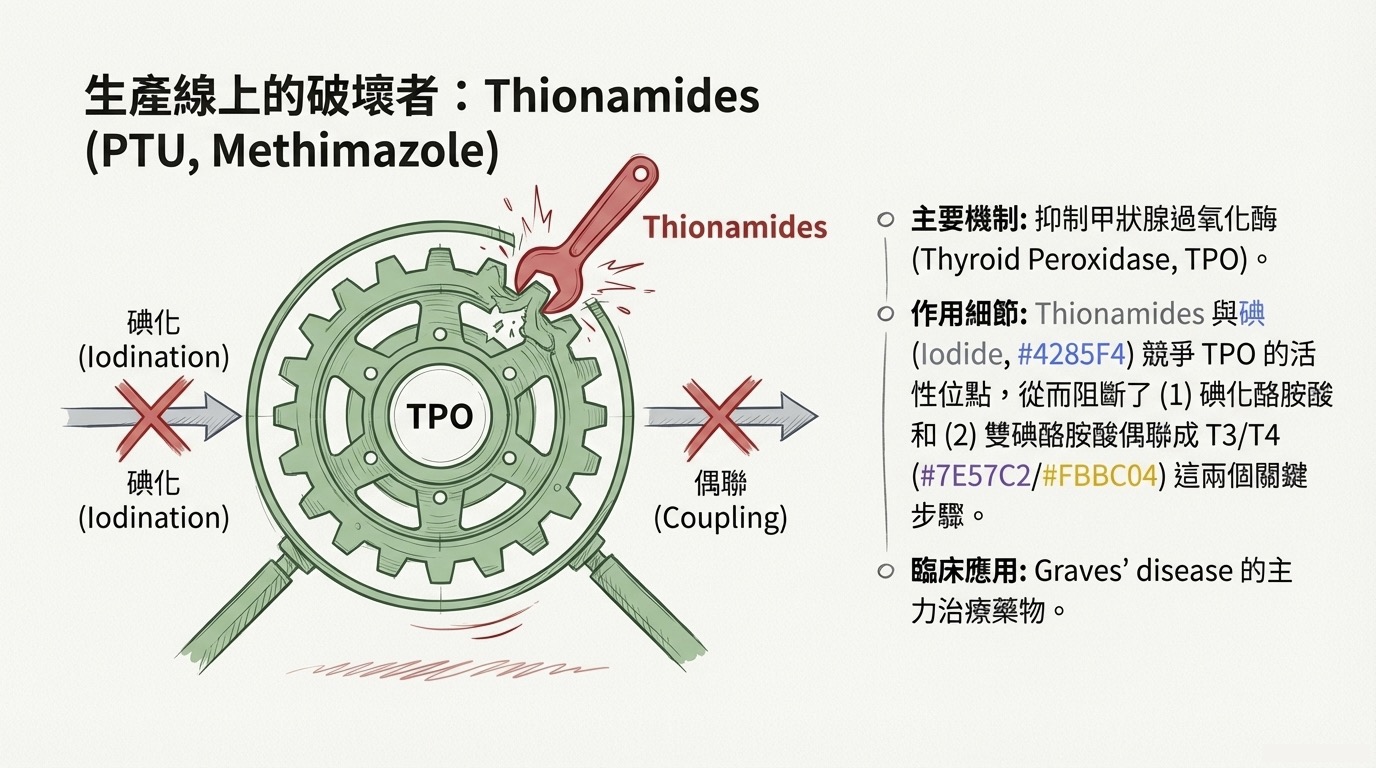
這是治療 Graves' disease 的臨床主力,包含 PTU, Methimazole, Carbimazole。
-
核心機制: 抑制 甲狀腺過氧化物酶 (Thyroid Peroxidase, TPO)。
-
分子細節: TPO 是甲狀腺素合成的關鍵酵素,負責兩大步驟:
- Iodination (碘化): 將碘加到酪胺酸上。
- Coupling (偶聯): 將雙碘酪胺酸 (DIT) 與單碘酪胺酸 (MIT) 結合成 T3 或 T4。
Thionamides 透過與碘離子 (Iodide) 競爭 TPO 的活性位點,阻斷上述過程。
-
藥物差異 (PTU vs. Methimazole):
- 兩者皆能抑制 TPO。
- PTU 的特殊功能: 在高劑量下,PTU 具有額外的周邊作用,它能抑制 Type 1 Deiodinase (D1),阻止 T4 在周邊組織轉換為 T3。這是 Methimazole 所不具備的特性。
2. Ionic Inhibitors (離子抑制劑)
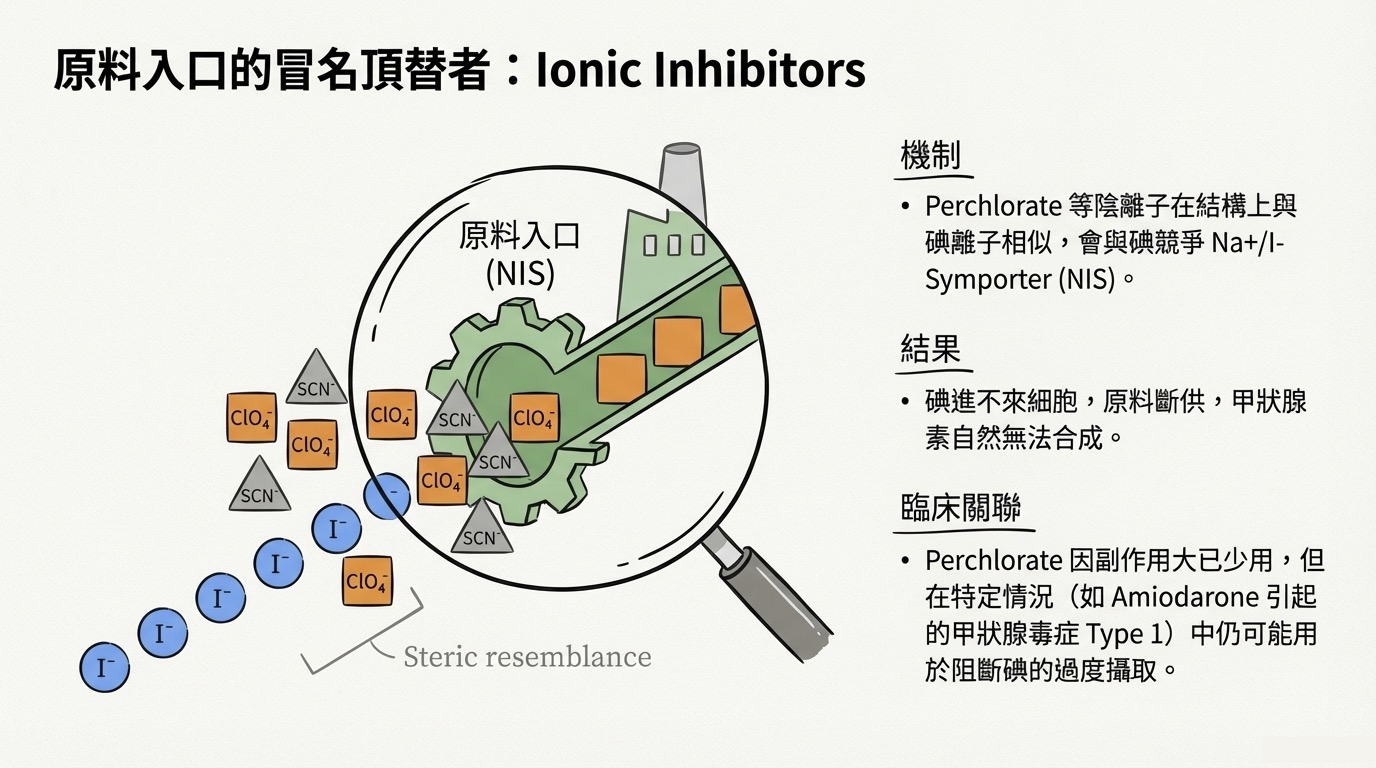 包含 Perchlorate () 與 Thiocyanate ()。
包含 Perchlorate () 與 Thiocyanate ()。
-
核心機制: 競爭 Symporter (NIS)。
-
分子細節: 這些陰離子在立體結構上與碘離子 () 極為相似 (Steric resemblance)。它們會卡住細胞膜上的 NIS 通道,導致碘原料無法進入濾泡細胞。
-
臨床關聯:
- 原料短缺,荷爾蒙合成受阻。
- Perchlorate 因副作用(如再生障礙性貧血)限制了常規使用,但在 Amiodarone 引起的甲狀腺毒症 (Type 1) 中,可用於阻斷碘攝取。
3. Lithium (鋰鹽)
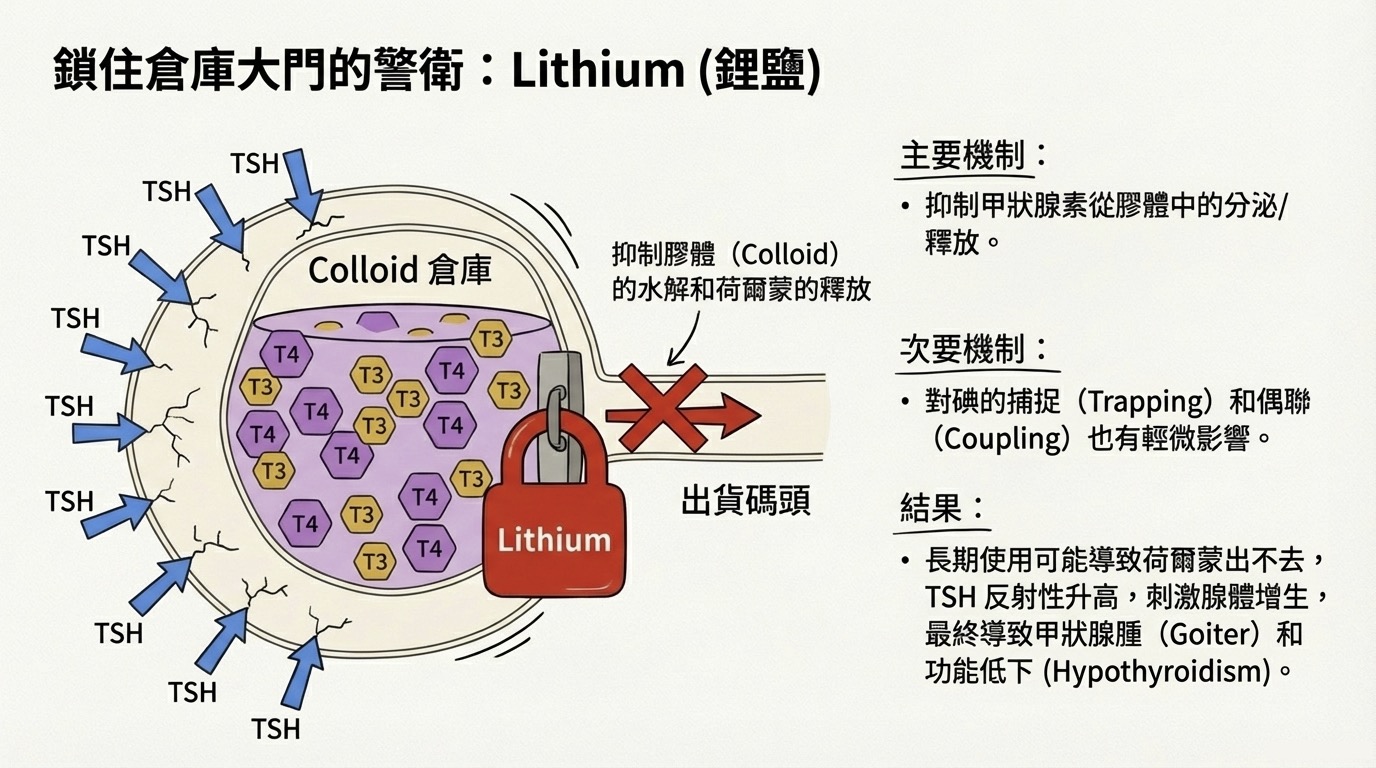 精神科用於治療躁鬱症 (Bipolar disorder) 的藥物。
精神科用於治療躁鬱症 (Bipolar disorder) 的藥物。
- 核心機制: 主要抑制 分泌 (Secretion) 步驟。
- 分子細節: 雖然鋰鹽對碘的捕捉 (Trapping) 和偶聯 (Coupling) 也有微弱影響,但其主要作用是抑制膠體 (Colloid) 的水解過程,導致合成好的荷爾蒙無法釋放進入血液。
- 臨床後果:
- 長期使用可能導致 甲狀腺腫 (Goiter) 和 甲狀腺低下 (Hypothyroidism)。
- 機制:荷爾蒙出不去 血液 T3/T4 下降 TSH 反射性升高 刺激腺體增生。
臨床點評 (Clinical Pearls: Part 1)
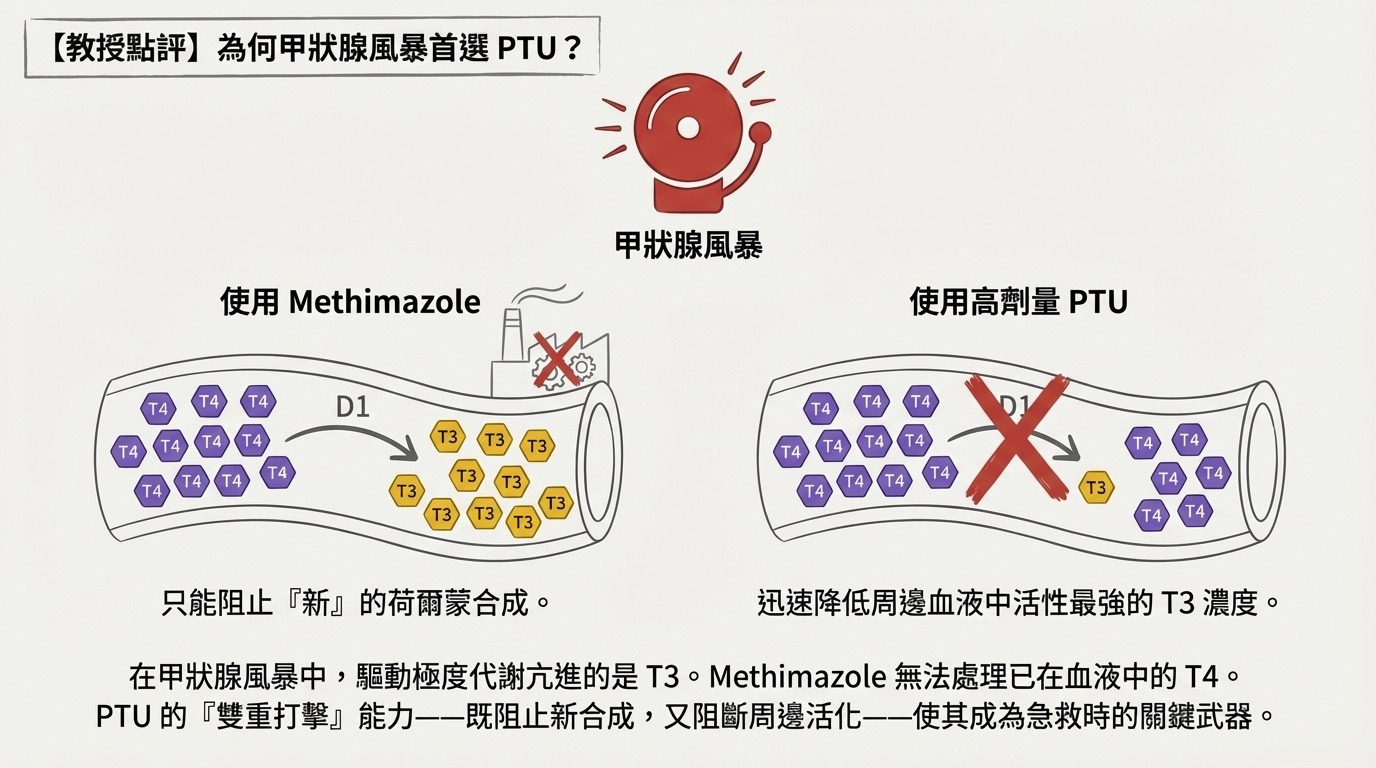
Q1: 為什麼 Thyroid Storm (甲狀腺風暴) 首選 PTU 而非 Methimazole?
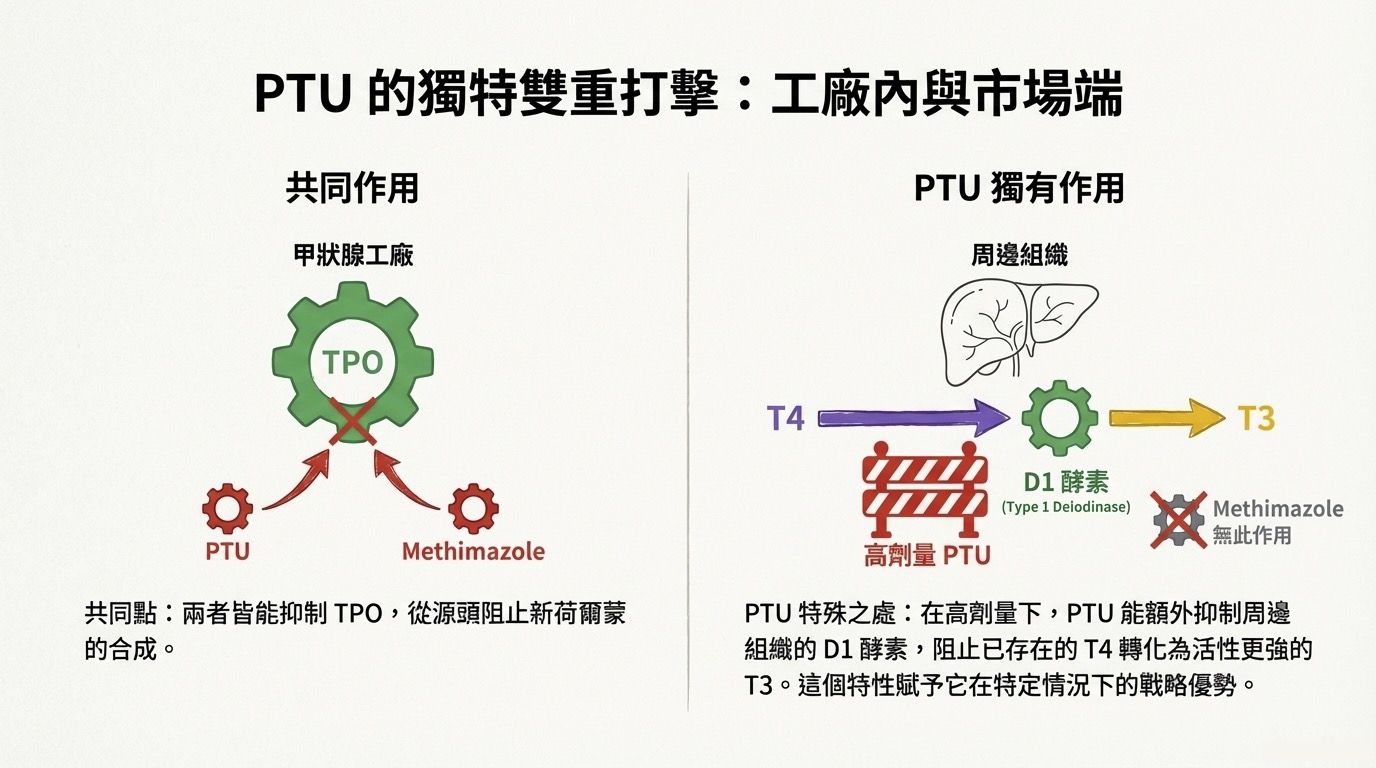 在甲狀腺風暴中,病人的代謝極度亢進,這主要是由生物活性最強的 T3 所驅動的。
在甲狀腺風暴中,病人的代謝極度亢進,這主要是由生物活性最強的 T3 所驅動的。
- Methimazole 的局限: 它只能阻止「新的」荷爾蒙合成,對於血液中已經存在的 T4 轉變為 T3 束手無策。
- PTU 的戰略地位: 高劑量 (Large doses) 的 PTU 不僅抑制合成,還能抑制周邊組織的 Type 1 Deiodinase (D1)。這能迅速阻斷 T4 轉為 T3 的路徑,快速降低血中 T3 濃度,直接緩解危急症狀。
Q2: Perchlorate Discharge Test 的原理是什麼?
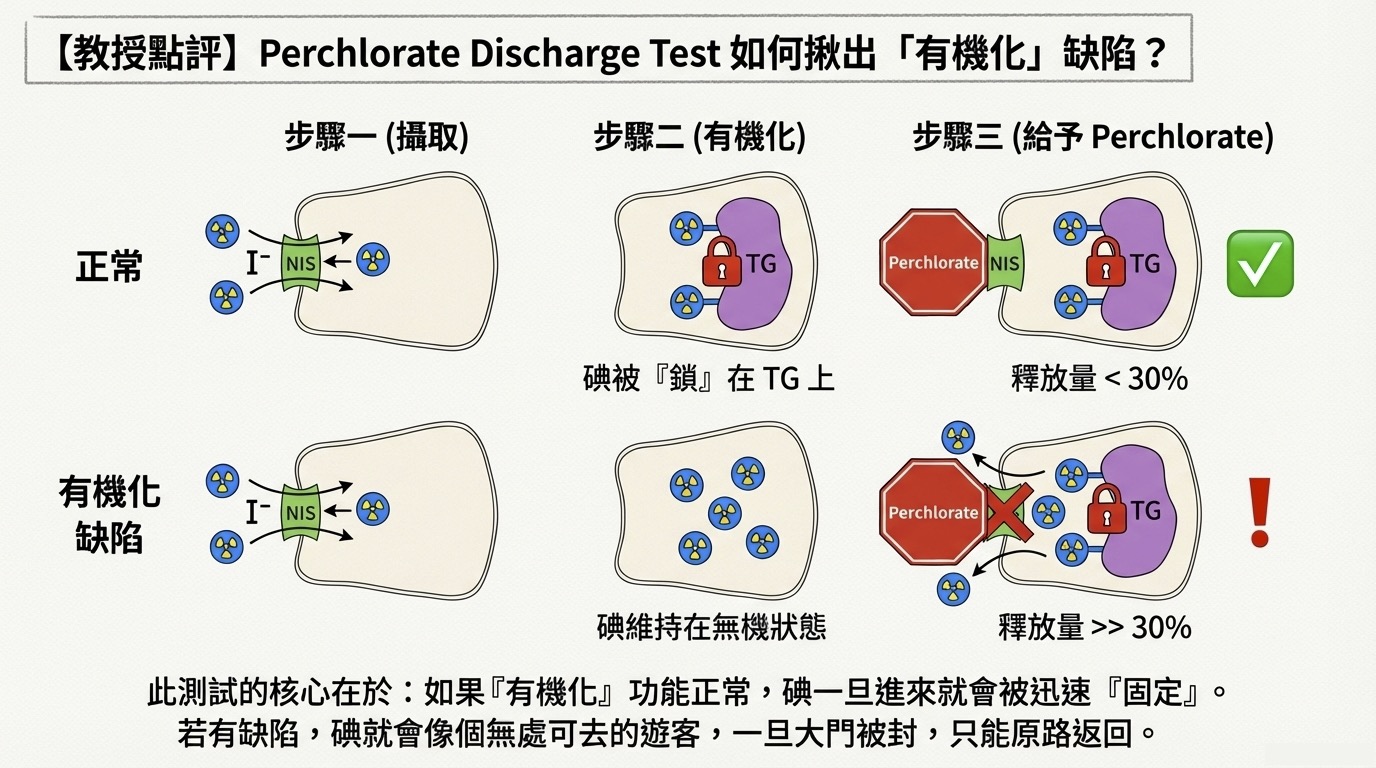 這是一個利用藥理機制來診斷「有機化缺陷 (Organification defect)」的測試。
這是一個利用藥理機制來診斷「有機化缺陷 (Organification defect)」的測試。
- 生理背景: 正常情況下,碘進入細胞後會迅速透過有機化過程 (Organification) 綁定在 Thyroglobulin 上。一旦綁定,碘就跑不掉。
- 測試機制:
- 給予放射性碘,讓細胞攝取。
- 給予 Perchlorate 封鎖 NIS 通道(關門)。
- 判讀:
- 正常人: 碘已經有機化綁住了,就算封門也不會流失。釋放量 (Discharge) 應 。
- 有機化缺陷者 (如 Hashimoto's, Pendred syndrome): 碘無法有機化,維持在無機狀態 (Inorganic iodide)。當 Perchlorate 封住 NIS,這些無處可去且未綁定的碘就會順著濃度梯度「洩漏 (Discharge)」回血液中。若釋放量遠高於正常值,即提示有機化障礙。
第二部分:改變代謝的藥物 (Drugs that Alter Metabolism)
藥物離開甲狀腺後,在周邊組織(肝、腎、腦)的命運同樣關鍵。這裡涉及「去碘作用 (Deiodination)」與「肝臟清除 (Hepatic Clearance)」兩大機制。
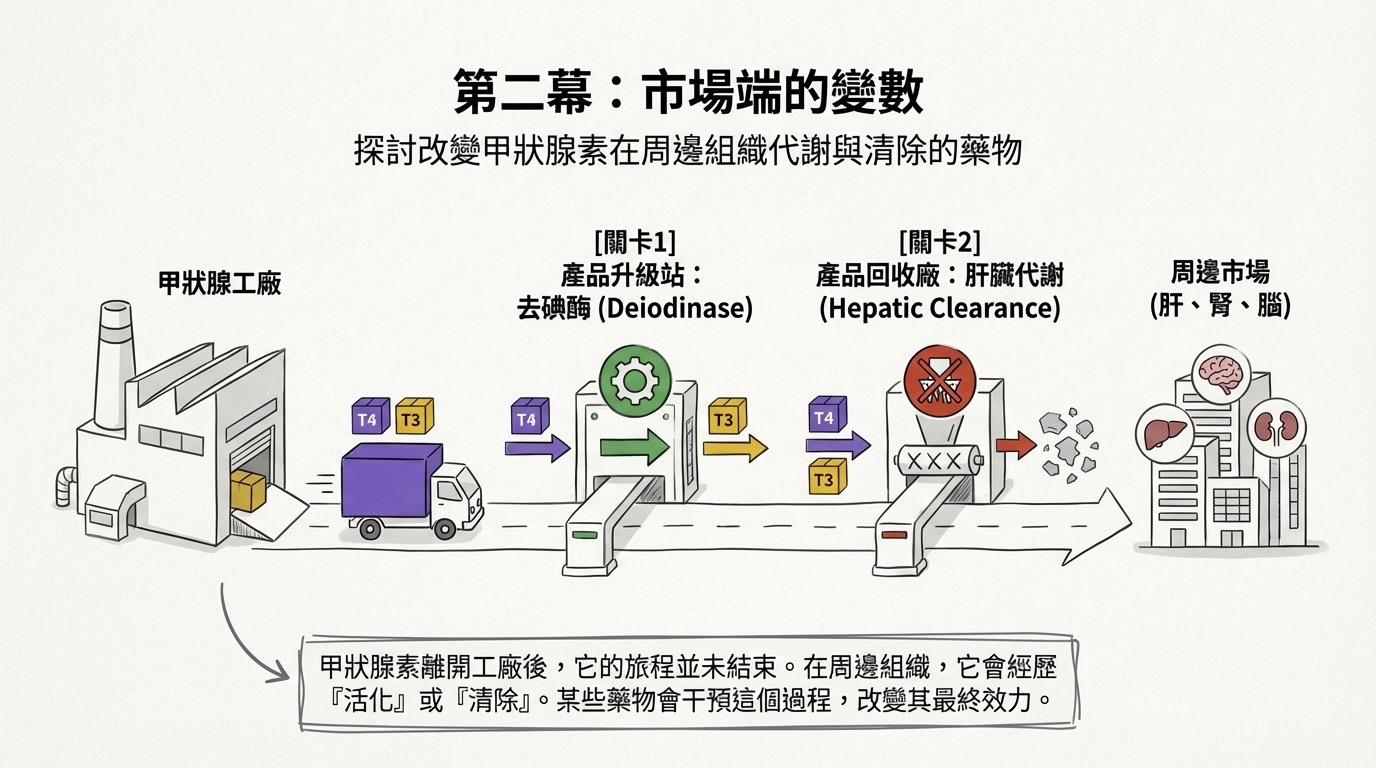
1. 抑制去碘酶 (Inhibition of Deiodination)
這類藥物阻斷 T4 轉化為活性 T3 的過程。
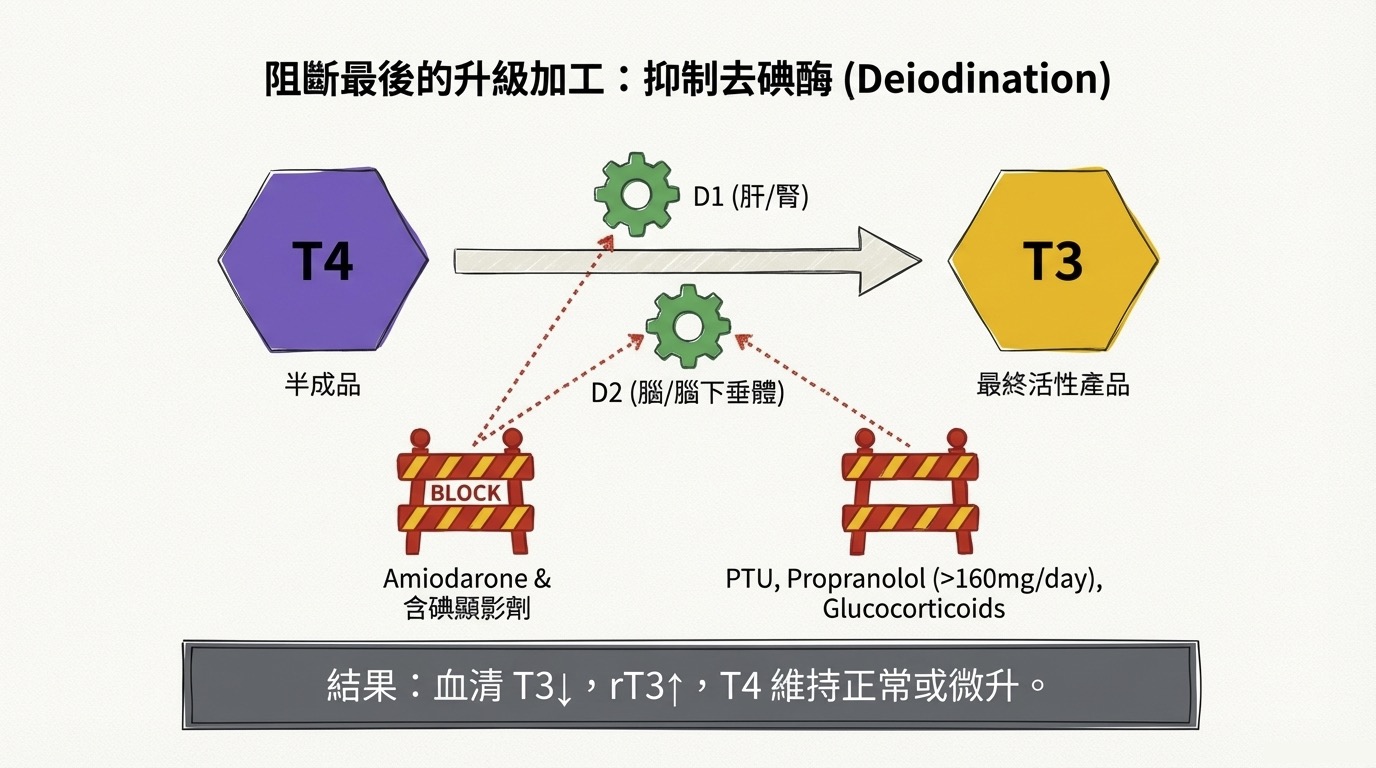
- 生化結果: 血清 T3 下降,rT3 (Reverse T3) 上升(因為 rT3 的清除路徑同樣被阻斷),而 T4 通常維持正常或微升。
- 關鍵酵素分佈:
- D1 (Type 1 Deiodinase): 主要存在於肝、腎,負責周邊 T3 的主要來源。
- D2 (Type 2 Deiodinase): 主要存在於 腦、腦下垂體、心臟。
- 藥物名單:
- Amiodarone & 含碘顯影劑: 作用最強,同時抑制 D1 與 D2。
- PTU, Propranolol (>160mg/day), Glucocorticoids: 主要抑制 D1。注意 Propranolol 需高劑量才具此效應。
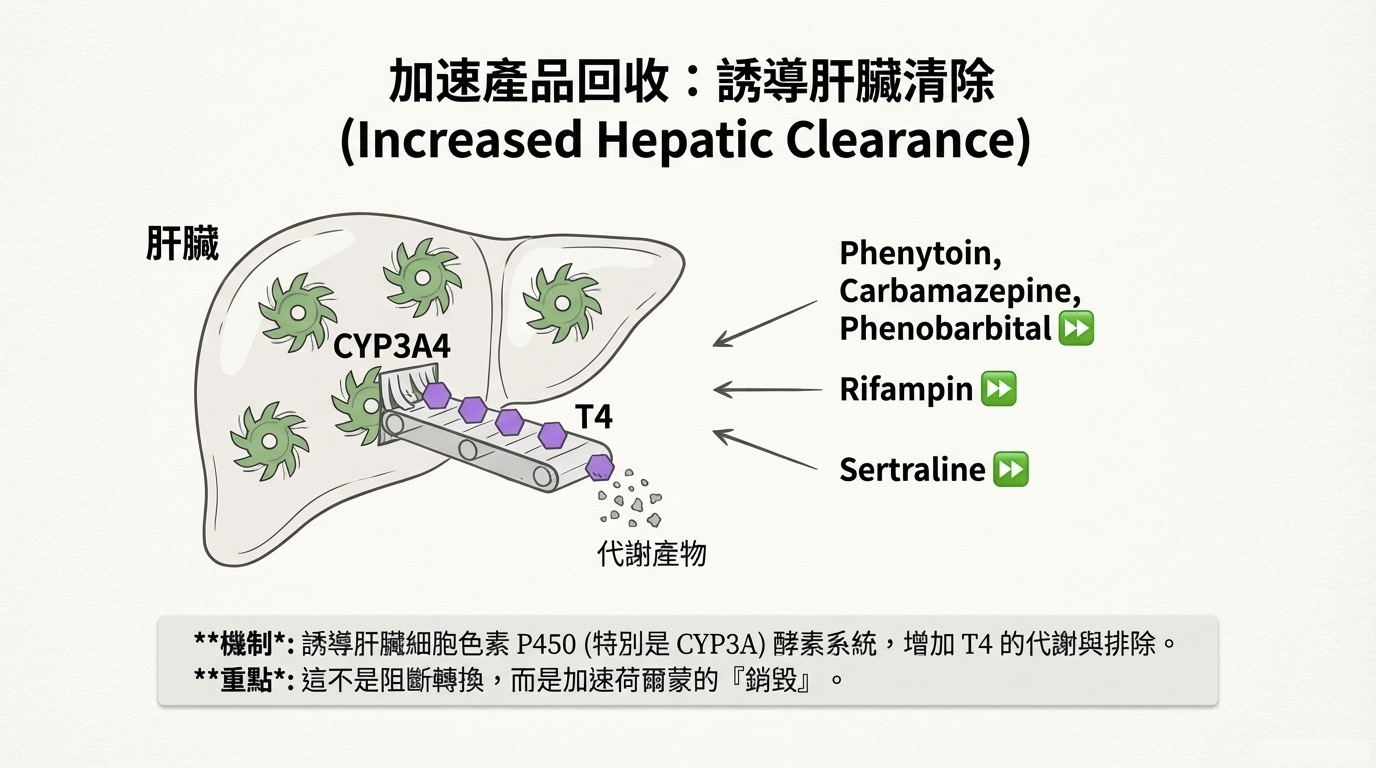
2. 加速肝臟清除 (Increased Hepatic Clearance)
這類藥物不阻斷轉換,而是加速荷爾蒙的「銷毀」。
- 核心機制: 誘導肝臟 Cytochrome P450 (特別是 CYP3a) 酵素系統,增加 T4 的葡萄糖醛酸化 (Glucuronidation) 與代謝排除。
- 藥物名單 (酵素誘導劑):
- Phenytoin, Carbamazepine, Phenobarbital (抗癲癇藥)
- Rifampin (抗結核藥)
- Sertraline (抗憂鬱藥)
- 臨床後果:
- 甲狀腺功能正常者: 身體會代償性增加 T4 產量,驗血結果通常正常。
- 甲狀腺低下 (服用 T4) 者: 這是災難性的。因為藥丸劑量是固定的,代謝一加速,藥效不足,導致 TSH 升高,病人出現低下症狀。
教授的臨床點評 (Clinical Pearls: Part 2)
Q3: Amiodarone 的矛盾現象:為何初期 TSH 會上升?
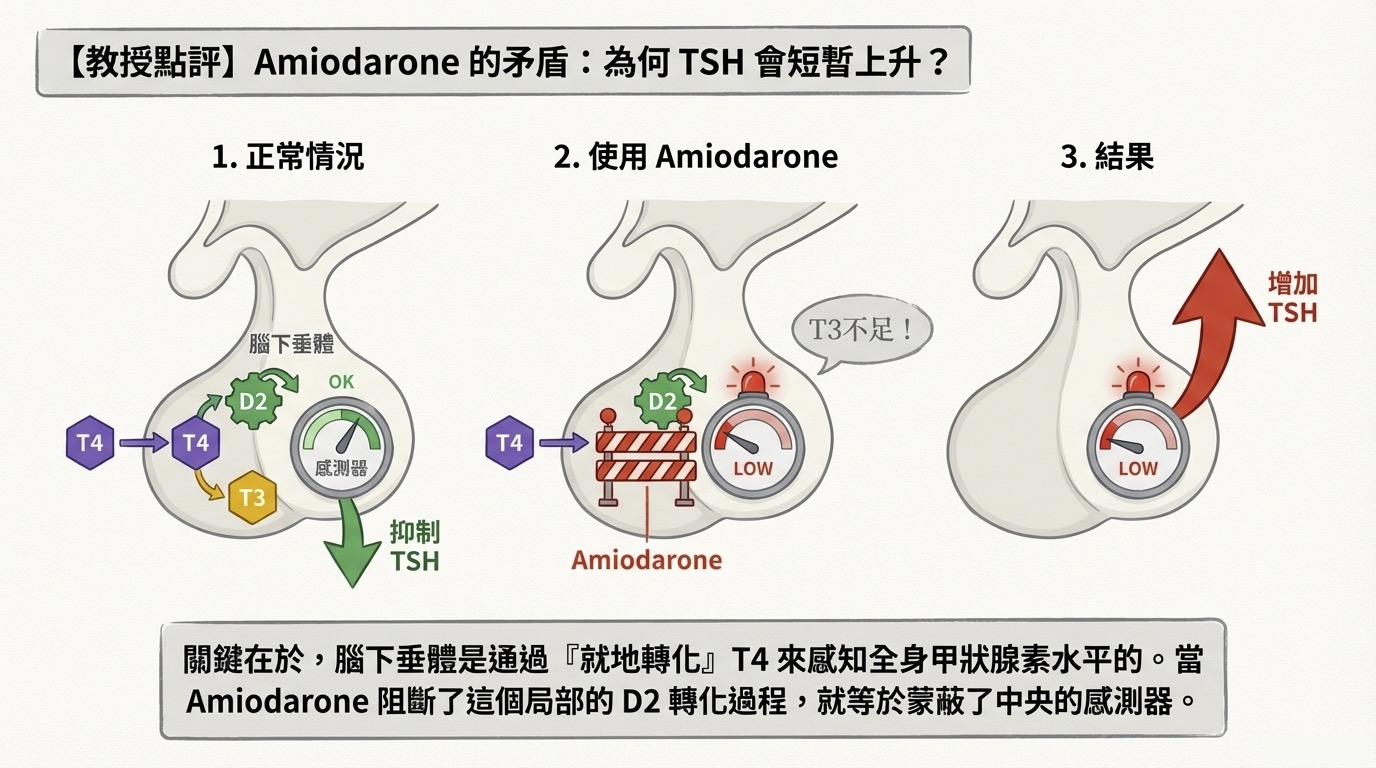 剛開始使用 Amiodarone 的短期內(前幾天到幾週),常觀察到 TSH 微幅上升 (Mild increase),伴隨 T4 上升但 T3 下降。
剛開始使用 Amiodarone 的短期內(前幾天到幾週),常觀察到 TSH 微幅上升 (Mild increase),伴隨 T4 上升但 T3 下降。
- 關鍵在於「腦下垂體感受器」: 腦下垂體前葉依賴細胞內的 Type 2 Deiodinase (D2) 將 T4 轉為 T3,藉由偵測細胞核內的 T3 濃度來判斷身體是否缺乏甲狀腺素。
- 機制: Amiodarone 強力抑制 D2。這導致腦下垂體細胞內的 T3 濃度下降,誤以為身體處於「缺甲狀腺素」狀態,因而減少負回饋抑制,導致 TSH 暫時性上升。
Q4: 抗癲癇藥物的陷阱:Carbamazepine 與 Hashimoto's
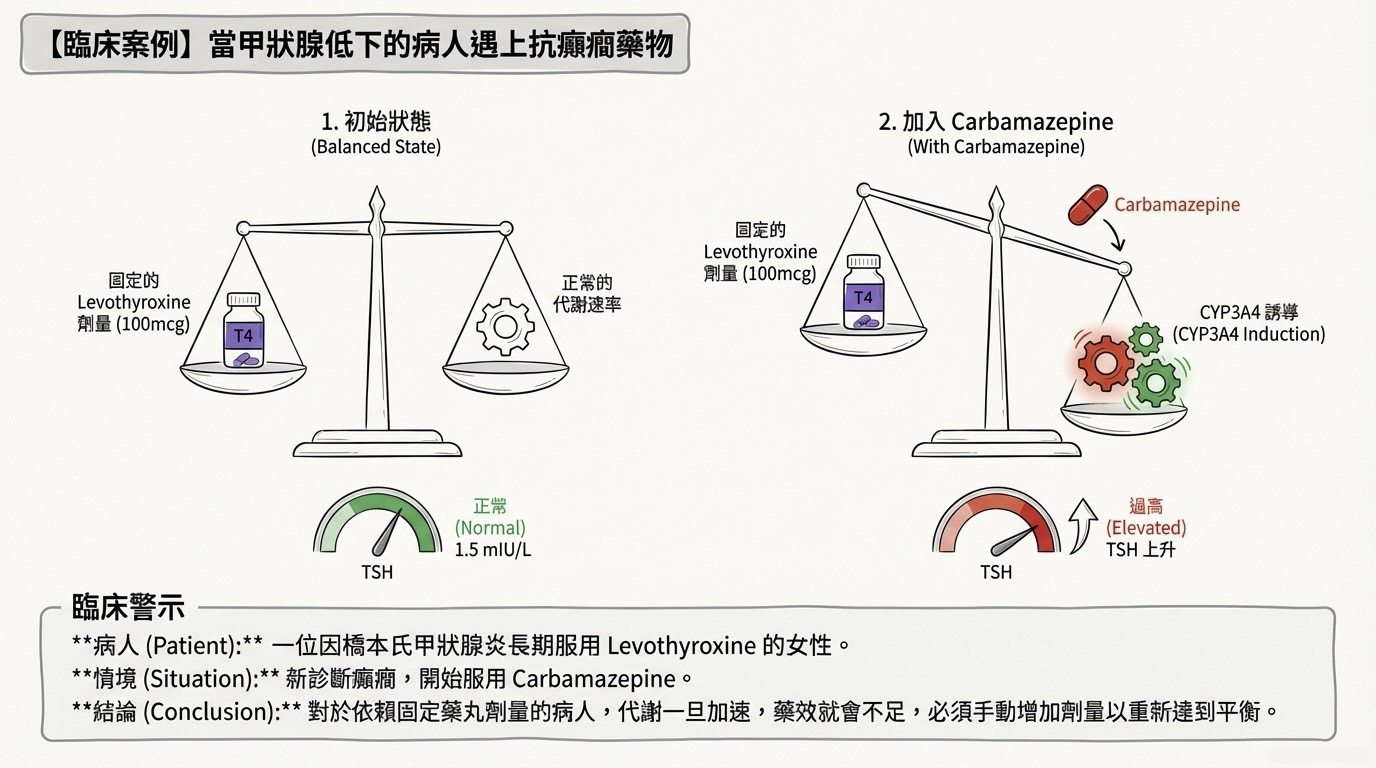 情境: 一位橋本氏甲狀腺炎女性,長期服用 Levothyroxine (100 mcg/day),TSH 控制完美 (1.5 mIU/L)。因新診斷癲癇開始服用 Carbamazepine。
情境: 一位橋本氏甲狀腺炎女性,長期服用 Levothyroxine (100 mcg/day),TSH 控制完美 (1.5 mIU/L)。因新診斷癲癇開始服用 Carbamazepine。
- 預測後果: Carbamazepine 誘導 CYP3a,加速 T4 的肝臟代謝清除。
- 處置原則:
- 對於靠吃藥維生的病人,甲狀腺無法加班代償。
- 由於 T4 被快速銷毀,血中濃度不足,TSH 將會升高。
- 醫師必須手動增加 Levothyroxine 的劑量,以抵銷被加速代謝的部分。