2026 vs 2018 ACC/AHA 血脂異常指引:綜合比較報告
版本:v1.4 | 日期:2026-03-16 來源:
- 2018 指引:Grundy SM et al. Circulation 2019;139:e1046–e1081
- 2026 指引:Blumenthal RS et al. J Am Coll Cardiol. 2026. DOI: 10.1016/j.jacc.2025.11.016
目錄
- 本文件閱讀指引
- 1. 執行摘要
- 2. 十大改變臨床實務的差異
- 3. 綜合比較表
- 4. 證據與推薦交叉矩陣
- 5. 臨床決策流程比較
- 6. 關鍵解讀釐清案例
- 7. 今天該改變臨床實務的推薦 vs 仍屬未來方向
- 8. 證據缺口與未來研究方向
- 9. 附錄:完整關鍵試驗參考文獻
1. 執行摘要
1.1 本次更新的歷史意義
2026 年 ACC/AHA 血脂異常指引(Blumenthal et al.,J Am Coll Cardiol 2026)正式取代並廢止 2018 年版「Management of Blood Cholesterol」指引,並以更廣義的「Management of Dyslipidemias」為名,標誌著心血管脂質醫學進入新紀元。本次更新距上次更新歷時 8 年,由四個關鍵 Phase 3 RCT(FOURIER、ODYSSEY OUTCOMES、CLEAR Outcomes、REDUCE-IT)、新型風險計算工具(PREVENT 方程式)、以及 Lp(a) 和 CAC 的大量流行病學數據所驅動。
1.2 三大核心典範轉移
典範轉移 1:治療目標——從「百分比降幅」回歸「數值目標(treat-to-target)」
2018 年指引刻意放棄固定 LDL-C 數值目標,改以百分比降幅(≥50% 或 ≥30%)為指導原則。2026 年指引明確恢復數值目標:極高風險(VHR ASCVD)<55 mg/dL、高風險 <70 mg/dL、中等風險 <100 mg/dL,同時設立配套的 non-HDL-C 和 ApoB 目標。這是血脂治療最根本的方向轉變,解決了 2018 年框架無法直觀評估「是否達標」的臨床困境。
典範轉移 2:風險評估——從 PCE 到 PREVENT,去種族化、現代化
Pooled Cohort Equations(PCE,2013 年)系統性高估當代人群 ASCVD 風險 40–50%,且使用種族(黑人/白人)作為生物學計算變量。2026 年以基於 330 萬人現代 EHR 數據的 PREVENT 方程式取代,移除種族、納入 eGFR 和社會剝奪指數(SDI),擴大適用年齡至 30–79 歲,並提供 30 年終生風險估算。相同患者的 PREVENT 估算值低於 PCE 40–50%,但識別相似的治療候選族群。
典範轉移 3:藥物選擇——打破「序貫治療」規定,以降幅需求和患者偏好為原則
2018 年要求在 PCSK9 抑制劑前必先嘗試 ezetimibe(強制序貫,Class I 規定),2026 年明確廢除此規定,允許根據所需 LDL-C 降幅和患者偏好直接選擇最合適藥物。同時,bempedoic acid(CLEAR Outcomes 支持)和 inclisiran(ORION 試驗)作為正式推薦藥物加入治療框架,顯著擴充了「高風險 statin 不耐受患者」的治療選項。
1.3 今天臨床醫師需要立即採取的行動
| 優先行動 | 說明 |
|---|---|
| 重新評估所有二級預防患者的 LDL-C 目標 | VHR:從「≥70 mg/dL 觸發加藥」改為「目標 <55 mg/dL」 |
| 廢棄 ezetimibe-first 強制序貫 | 高風險患者可直接依降幅需求考慮 PCSK9 mAb |
| 對所有成人開立一次性 Lp(a) 檢測 | 從「選擇性」升為 COR 1;約 1/5 成人 Lp(a) ≥125 nmol/L |
| 改用 PREVENT-ASCVD 方程式 | 取代 PCE;同一患者估算值降低約 40–50%,需重新校正風險溝通 |
| 告知患者膳食補充劑無效 | COR 3: No Benefit(魚油補充劑、植物固醇、紅麴米均不推薦) |
| 為 HIV 患者(40–75 歲)啟動 statin | REPRIEVE:HR 0.65,MACE 降低 35%;升格為 COR 1 |
| HFrEF 患者停止以「HF 本身」啟動 statin | HFrEF 無 ASCVD:COR 3: No Benefit(B-R);HFrEF 合併缺血性病因/ASCVD——新啟動:COR 2b(B-R),繼續既有 statin:COR 1(A) |
| 透析患者勿常規啟動 statin 一級預防 | 新啟動:COR 3: No Benefit(B-R)(從 Class IIa 降格);轉入透析者繼續既有 statin:COR 2b(C-LD)——"it may be reasonable to continue statin therapy" |
| CAC ≥1000 AU 按二級預防 VHR 強度治療 | 新 COR 1:LDL-C 目標 <55 mg/dL |
| 改用 Martin/Hopkins 方程式計算 LDL-C | COR 1(B-NR);Friedewald 在 LDL-C <70 mg/dL 時系統性低估 |
2. 十大改變臨床實務的差異
#1 Bempedoic Acid 正式進入治療框架 💊
變更概述
Bempedoic acid 作為 ACL(ATP citrate lyase)抑制劑,是 2026 指引中最重要的新增藥物。它是唯一以 statin 不耐受患者為主要入組人群的降脂藥物 CVOT,填補了長期以來此族群缺乏 MACE 獲益證據的空白。
2018 怎麼寫
不存在——bempedoic acid 尚未獲 FDA 批准,2018 指引無任何提及。
2026 怎麼寫
SAMS 患者(statin 不耐受)+ ASCVD:COR 1(B-R);SAMS + 高風險一級預防:COR 1(B-R);二級預防 add-on:COR 2a(B-R);嚴重高膽固醇血症 + ASCVD:COR 1(A)。
為什麼改
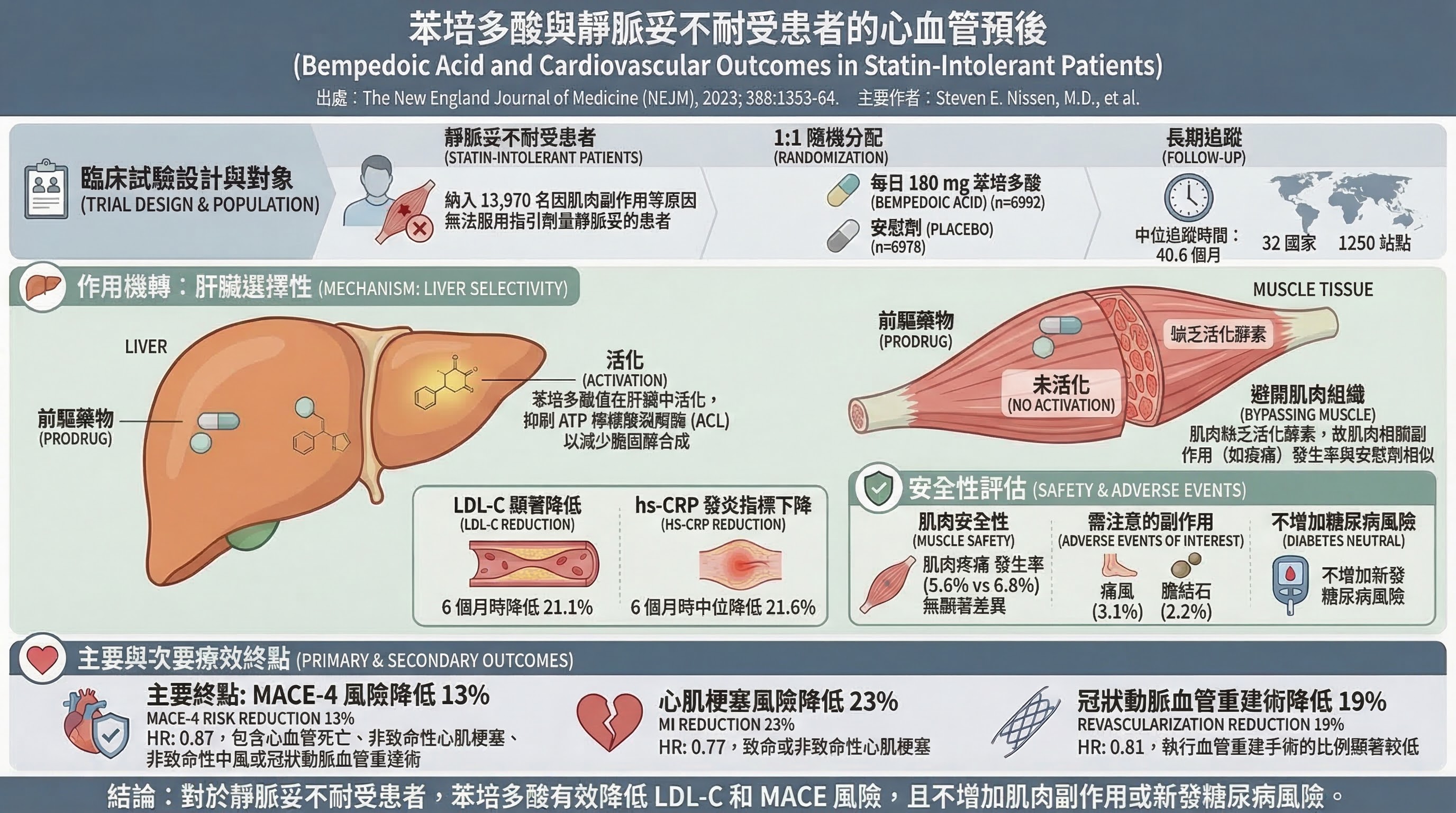
CLEAR Outcomes 試驗是驅動此變更的唯一關鍵試驗。此前 statin 不耐受患者僅能使用 ezetimibe(降 LDL-C ~18%,IMPROVE-IT 為二級預防非 statin 不耐受族群),缺乏專門針對此族群的 CVOT 數據。CLEAR Outcomes 以 13,970 名 statin 不耐受患者為入組人群,確認 bempedoic acid 降低 MACE 13%,一級預防亞組更達 30% RRR,且無肌肉毒性(肌痛症發生率與安慰劑無差異),為此族群提供首個有硬終點支持的口服降脂選項。
關鍵文獻深讀
CLEAR Outcomes (Nissen SE et al., NEJM 2023, PMID 36876740)
- 研究設計:多中心、隨機、雙盲、安慰劑對照 Phase 3 RCT
- PICO:P = statin 不耐受成人(70% 二級預防,30% 高風險一級預防);I = bempedoic acid 180 mg/day;C = 安慰劑;O = 4-component MACE(CV 死亡、非致命 MI、非致命中風、冠狀動脈血運重建)
- 主要發現:4-component MACE HR 0.87(95% CI 0.79–0.96,P = 0.004);ARR 1.6%;NNT ~63(40.6 個月中位追蹤);一級預防亞組 HR 0.70(ARR 2.3%,NNT 43)
- 為什麼重要:這是唯一以 statin 不耐受患者為主要入組人群的降脂 CVOT,證明非 statin 口服藥物可在此族群產生具有統計意義的 MACE 降低
- 主要限制:industry sponsored(Esperion);追蹤期相對短(40.6 個月);高尿酸血症/痛風風險升高(11.9% vs 7.6%);與 pravastatin(限 40 mg/day)和 simvastatin(限 20 mg/day)合用需劑量上限(OATP1B1/1B3 轉運體抑制)
臨床意義
影響所有 statin 不耐受患者(臨床估計 5–20%)。此前這類患者的降脂選項僅限 ezetimibe,現在有了具 CVOT 支持的口服替代方案。NNT 與 FOURIER/ODYSSEY 相當,應積極使用。
實務建議
- 對所有確認 statin 不耐受(需經 rechallenge 確認)的 ASCVD 或高風險一級預防患者,主動考慮 bempedoic acid 180 mg/day
- 處方前確認無活動性痛風或嚴重高尿酸血症
- 注意藥物交互作用:與 pravastatin 合用限 40 mg/day;與 simvastatin 合用限 20 mg/day
- 可與 ezetimibe 合併使用(bempedoic acid/ezetimibe 複合錠可用)
證據層級與限制
- COR 1(B-R)用於 SAMS + ASCVD / 高風險一級預防
- COR 2a(B-R)用於二級預防 add-on(可耐受 statin 者)
- Tier 分類:Tier 1 (direct_guideline) + Tier 2 (trial_supported — CLEAR Outcomes)
- 限制:單一 CVOT;追蹤期 <4 年;痛風風險需權衡
#2 Inclisiran(siRNA PCSK9 抑制劑)正式加入指引 💊
變更概述
Inclisiran 作為首個 siRNA 機制的 PCSK9 抑制劑加入 2026 指引,提供每 6 個月一次診所注射的給藥模式,但因缺乏正式 CVOT 數據,定位為 PCSK9 mAb 的二線替代。
2018 怎麼寫
不存在——inclisiran 於 2021 年才獲 FDA 批准,2018 指引無任何提及。
2026 怎麼寫
COR 2a(B-NR):作為 PCSK9 mAb 的替代選項,適用無法耐受或取得 PCSK9 mAb 者,或偏好每 6 個月給藥一次者。
為什麼改
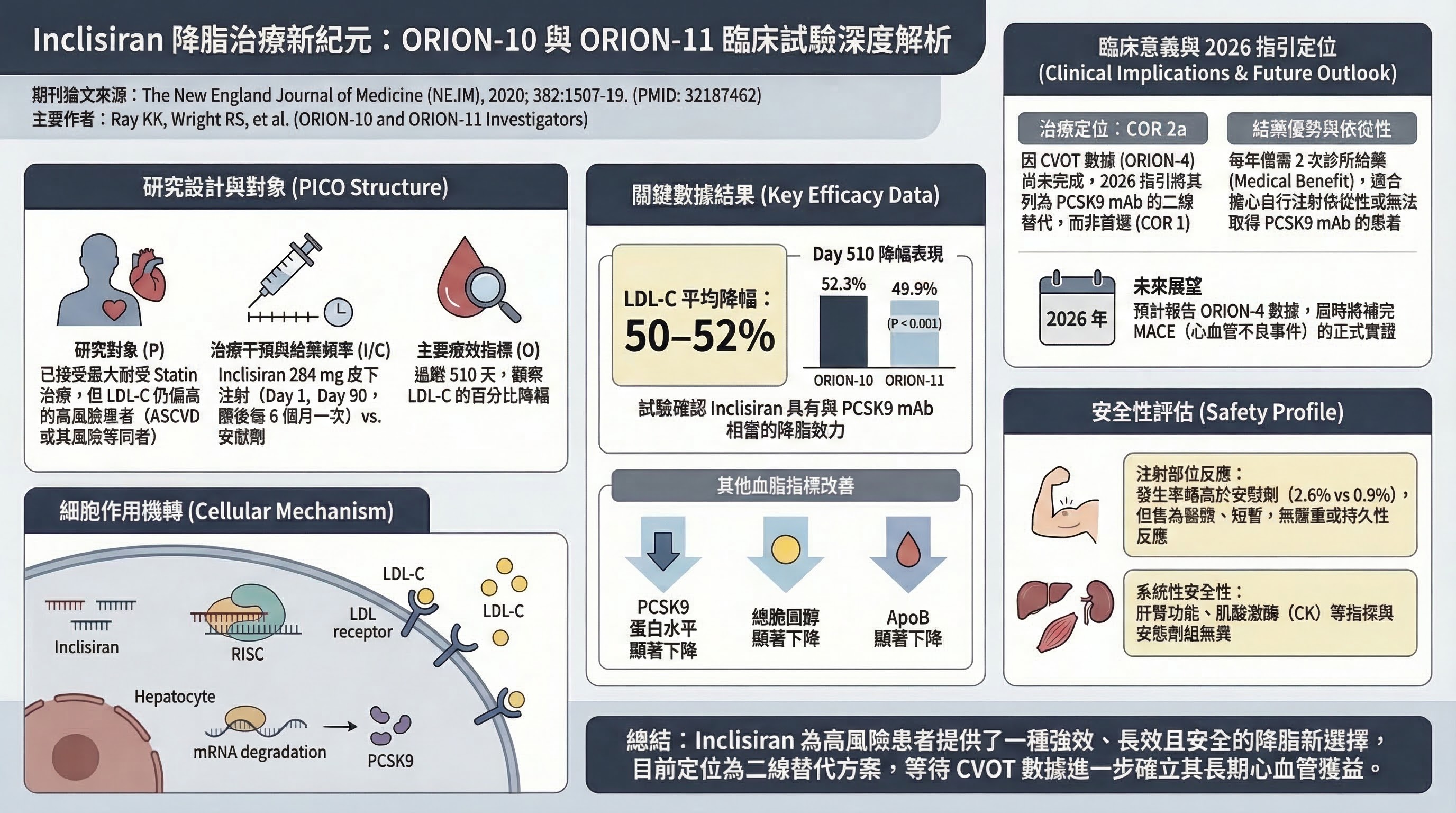
ORION-10 和 ORION-11 兩項 Phase 3 試驗確認 inclisiran 降低 LDL-C 50–52%(時間平均降幅),效力與 PCSK9 mAb 相當。然而,降 CV 事件的正式 CVOT 數據尚未完成(ORION-4 預計 2026 年報告),因此 2026 指引將其定位為 COR 2a(而非 COR 1),且明確標示為 PCSK9 mAb 的二線替代,而非並列首選。
關鍵文獻深讀
ORION-10 + ORION-11 (Ray KK et al., NEJM 2020, PMID 32187462)
- 研究設計:兩項 Phase 3 隨機、雙盲、安慰劑對照試驗(ORION-10 = ASCVD,ORION-11 = ASCVD 或 ASCVD risk equivalent)
- PICO:P = 已接受最大耐受 statin 但 LDL-C 仍偏高的高風險患者;I = inclisiran 284 mg SC(Day 1, Day 90, then Q6M);C = 安慰劑;O = LDL-C 百分比降幅
- 主要發現:時間平均 LDL-C 降幅 50–52%;Day 510 LDL-C 降幅 ~54%;探索性 MACE 分析 OR 0.74(95% CI 0.58–0.94)
- 為什麼重要:確認 siRNA 機制可達成與 PCSK9 mAb 相當的 LDL-C 降幅,且每年僅需 2 次診所注射,潛在改善長期依從性
- 主要限制:以 LDL-C 降幅為主要終點,非 MACE(CVOT 待完成);探索性 MACE 分析樣本量不足以做定論;industry sponsored(Novartis)
臨床意義
適用族群:(1) 無法取得 PCSK9 mAb 的患者、(2) 偏好 Q6M 診所注射(vs Q2W 自行注射)者、(3) 擔心自行注射依從性問題者。Inclisiran 屬醫療保險範疇(medical benefit,需診所給藥),不同於 PCSK9 mAb 的藥局自給(pharmacy benefit)。
實務建議
- PCSK9 mAb 仍為首選(有正式 CVOT 支持),inclisiran 為二線替代
- 適合在門診直接給藥的患者(回診頻率 ≥Q6M)
- 給藥時程:Day 1 → Day 90 → 此後每 6 個月
- 等待 ORION-4 結果以確認 CV 事件降低效益
證據層級與限制
- COR 2a(B-NR)——因缺乏 CVOT 數據,LOE 為 B-NR 而非 B-R
- Tier 分類:Tier 1 (direct_guideline) + Tier 2 (trial_supported — LDL-C 降幅),但 CVOT pending
- 限制:正式 CVOT(ORION-4、VICTORION-2P)尚未完成
#3 廢除 PCSK9 抑制劑「必先用 ezetimibe」的強制序貫規定 🔄
變更概述
2026 指引正式廢除 2018 年要求 PCSK9 抑制劑前必須先使用 ezetimibe 的強制序貫規定,允許臨床醫師根據所需 LDL-C 降幅和患者偏好直接選擇最合適的非 statin 藥物。
2018 怎麼寫
"In patients at very high risk whose LDL-C level remains ≥70 mg/dL... it is reasonable to add ezetimibe therapy (IIa, B-R). In patients at very high risk whose LDL-C level remains ≥70 mg/dL on maximally tolerated statin and ezetimibe therapy, adding a PCSK9 inhibitor is reasonable (IIa, A), although the long-term safety (>3 years) is uncertain and cost effectiveness is low."
此外,Class I 建議明確規定 ezetimibe 必須在 PCSK9 抑制劑之前嘗試。
2026 怎麼寫
Ezetimibe 和/或 PCSK9 mAb 均為 COR 1 並列選項(LOE A),無先後強制順序。根據「所需 LDL-C 降幅」和「患者偏好」選擇。費用相關限制性說明已移除。
為什麼改
三個因素共同驅動此變更:(1) FOURIER-OLE 確認 evolocumab 長期安全性(最長 8.4 年,中位 LDL-C ~30 mg/dL 持續維持,無安全訊號),消除 2018 年對「長期安全性不確定」的疑慮;(2) PCSK9 mAb 年費用從 2018 年 ~5,850,成本效益顯著改善;(3) 臨床實務中,強制序貫延遲高風險患者達標。
關鍵文獻深讀
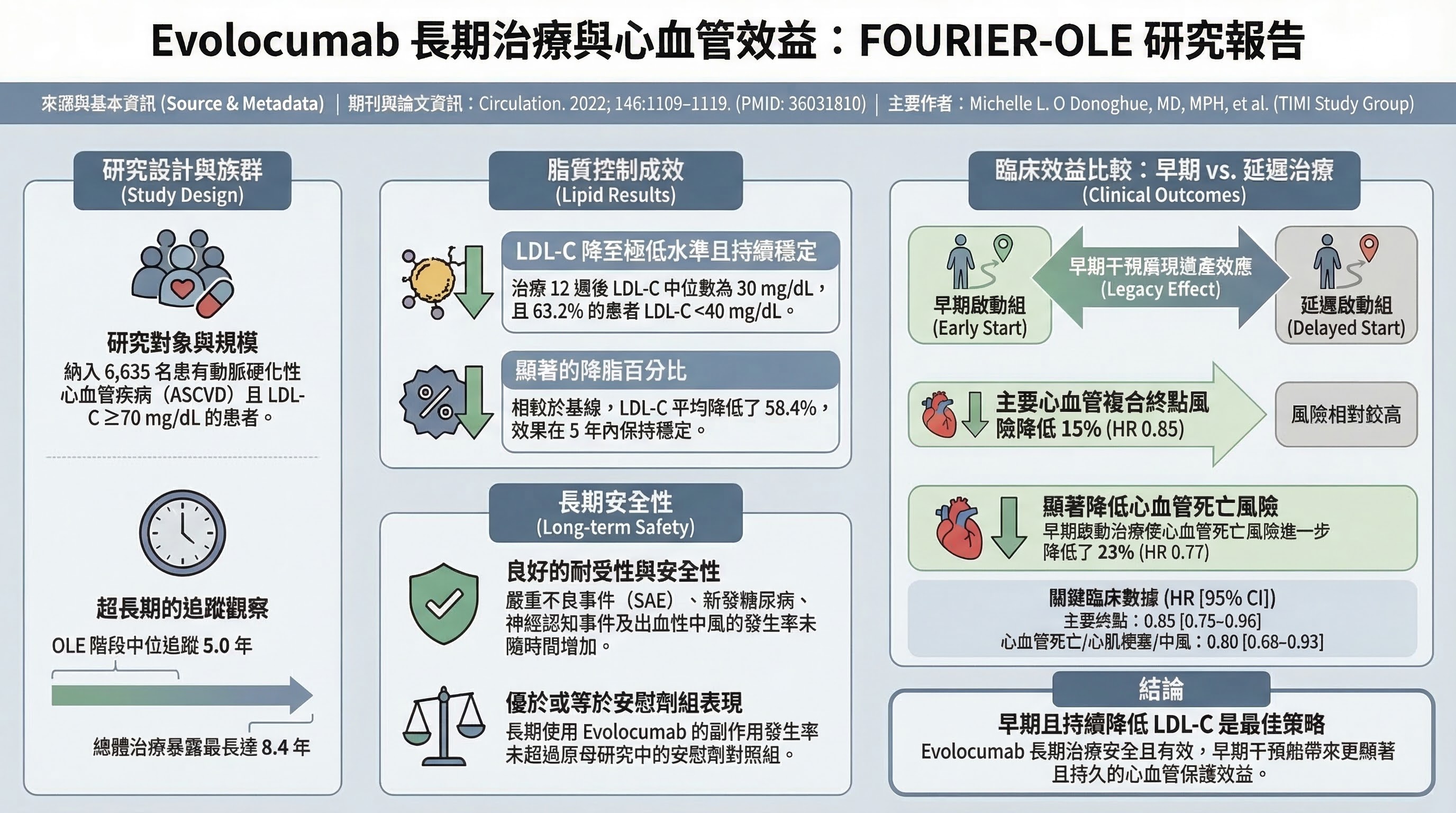
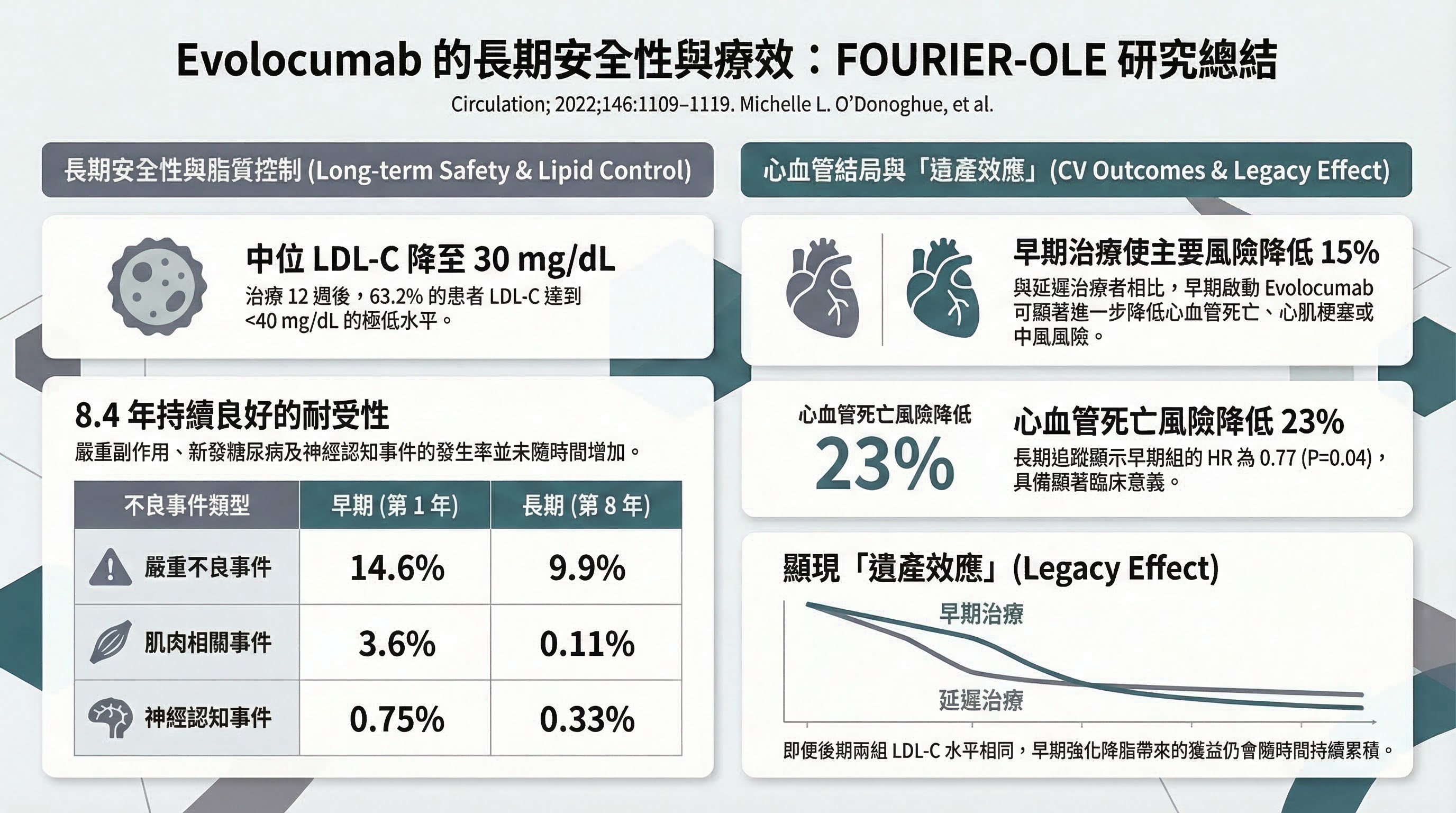
FOURIER-OLE (O'Donoghue ML et al., Circulation 2022, PMID 36031810)
- 研究設計:FOURIER 試驗的開放標籤延伸研究
- PICO:P = 完成 FOURIER 主試驗的 ASCVD 患者;I = 持續 evolocumab;C = 原安慰劑組延遲開始 evolocumab;O = 長期安全性及 MACE
- 主要發現:中位追蹤 ~5 年(累計暴露最長 8.4 年),LDL-C ~30 mg/dL 持續維持;無新安全訊號(neurocognitive events、new-onset DM、hemorrhagic stroke 均無增加);MACE 持續獲益 15–23%
- 為什麼重要:解答 2018 年指引明確提出的「長期安全性(>3 年)不確定」疑慮,為廢除序貫規定提供安全性基礎
- 主要限制:開放標籤延伸(非雙盲);選擇性偏差(完成主試驗者較健康)
臨床意義
消除原先強制序貫延遲高風險患者達標的障礙。例如:VHR 患者基線 LDL-C 120 mg/dL,加用 ezetimibe 僅降 ~25%(→ ~90 mg/dL),仍遠未達 <55 mg/dL 目標;此類患者應直接考慮 PCSK9 mAb(可再降 50–60%)。
實務建議
- 評估每位 VHR 患者所需的 LDL-C 降幅:若需降 >25%(ezetimibe 上限),直接考慮 PCSK9 mAb
- 費用已非限制因素(年費用 ~$5,850),不應再以成本為由延遲處方
- Ezetimibe 仍是合理選擇——特別是所需降幅 ≤25%、患者偏好口服、或 PCSK9 mAb 取得困難時
- 可同時使用 ezetimibe + PCSK9 mAb 以最大化降幅
證據層級與限制
- COR 1(A)——ezetimibe 和 PCSK9 mAb 並列
- Tier 分類:Tier 1 (direct_guideline)
- 限制:PCSK9 mAb 在部分保險計畫中仍有事前審查要求
#4 LDL-C 治療目標恢復數值目標制——VHR 目標 <55 mg/dL 📊
變更概述
2026 指引明確恢復數值目標(treat-to-target),為各風險層級設立具體 LDL-C / non-HDL-C / ApoB 目標值,從根本上逆轉 2018 年「只看百分比降幅」的方針。
2018 怎麼寫
"In clinical ASCVD, reduce LDL-C by ≥50%." 極高風險使用「LDL-C ≥70 mg/dL」作為觸發加藥的閾值(trigger threshold),但並無明確的 LDL-C 終點目標。
2026 怎麼寫
VHR ASCVD → LDL-C <55 mg/dL(COR 1, LOE A);ASCVD 非 VHR → <70 mg/dL(COR 1, LOE A);高風險一級預防 → <70 mg/dL(COR 2a, LOE B-R);中等風險一級預防 → <100 mg/dL(COR 2a, LOE B-NR)。同步設立 non-HDL-C 和 ApoB 配套目標。
為什麼改
CTT meta-analyses 反覆證明 LDL-C 降低與 CV 事件降低之間存在連續線性關係(每降 1 mmol/L,主要血管事件 RRR 22%),且在 LDL-C <2 mmol/L(~77 mg/dL)時獲益仍持續。FOURIER-OLE 進一步確認 LDL-C ~30 mg/dL 維持 8 年以上的安全性和持續 MACE 獲益。歐洲 ESC/EAS 指引自 2019 年起已採用 <55 mg/dL 目標,美國 ACC/AHA 在累積更多長期數據後跟進。
關鍵文獻深讀
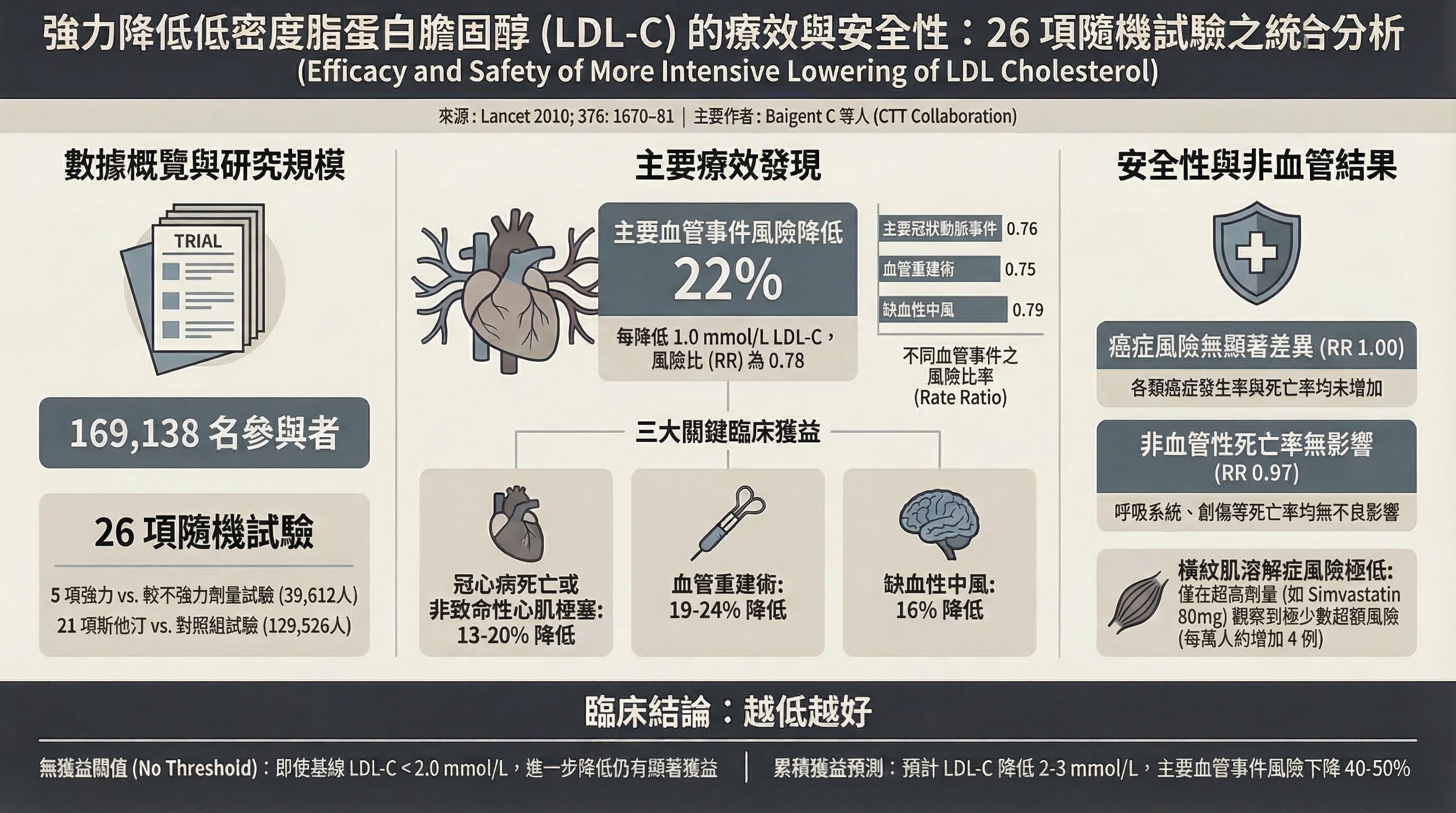
CTT 2010 meta-analysis (Baigent C et al., Lancet 2010, PMID 21067804)
- 研究設計:26 項 statin 試驗個體數據 meta-analysis,N = 170,000+
- 主要發現:每降低 1 mmol/L LDL-C,主要血管事件 RRR 22%(HR 0.78, 95% CI 0.76–0.80);在 LDL-C <2 mmol/L 時獲益曲線未見平台效應
- 為什麼重要:建立「越低越好」原則的量化基礎
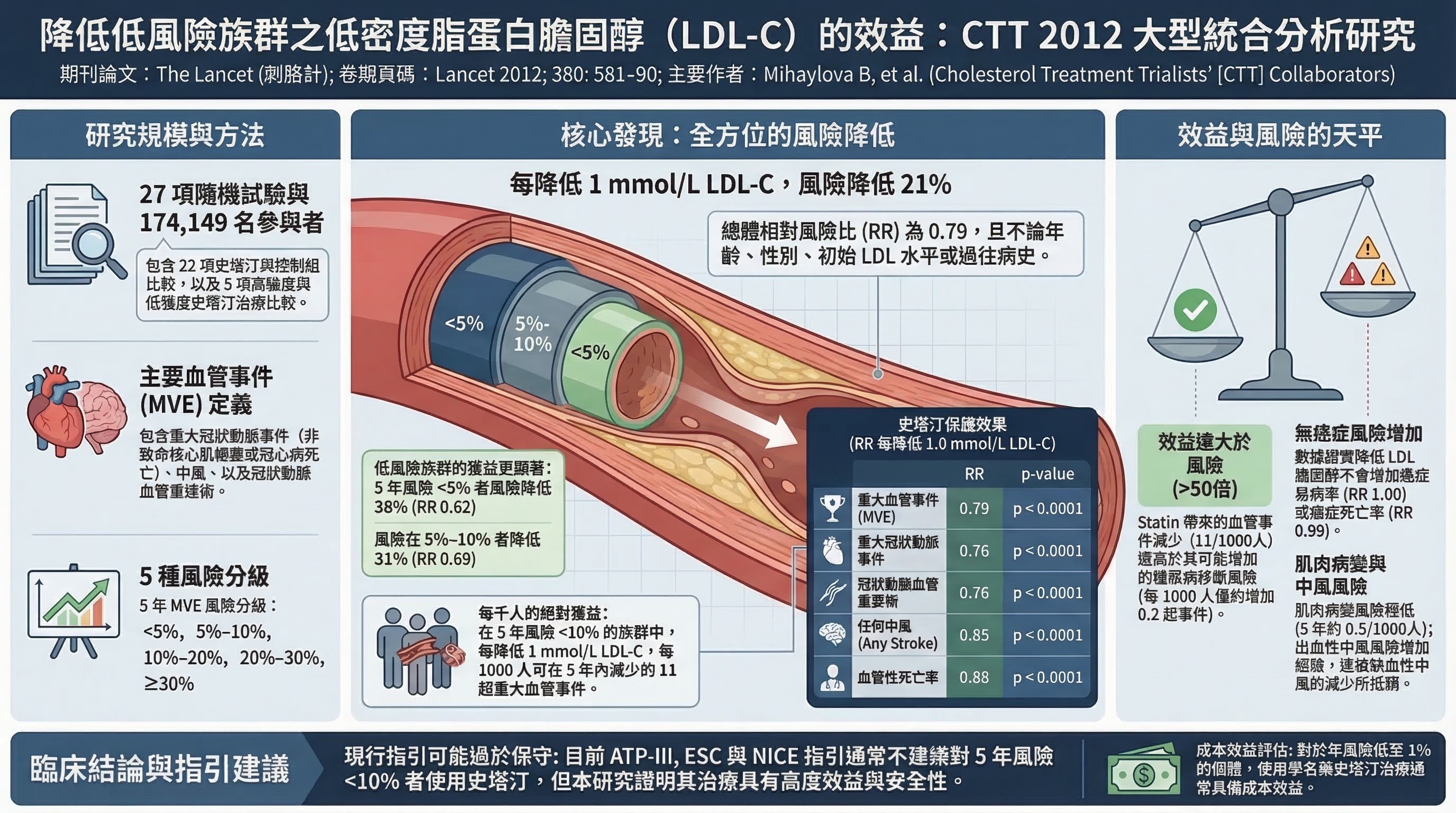
CTT 2012 meta-analysis (Mihaylova B et al., Lancet 2012, PMID 22607822)
- 研究設計:27 項試驗 meta-analysis,聚焦低風險族群
- 主要發現:低風險族群每降 1 mmol/L LDL-C,5 年減少 11 次大血管事件/1,000 人
- 為什麼重要:確認一級預防族群同樣適用「越低越好」原則
FOURIER-OLE (PMID 36031810) — 見 #3 文獻深讀
臨床意義
「越低越好」原則正式寫入指引,建立具體可評估的治療終點。2026 指引 Top Take-Home Message #4:「LDL-C and non-HDL-C treatment goals are back to guide LLT.」臨床醫師現在有了明確的「是否達標」判斷標準,取代過去模糊的「百分比降幅是否足夠」。
實務建議
- 立即重新評估所有 ASCVD 患者的 LDL-C 目標——VHR:<55 mg/dL,非 VHR:<70 mg/dL
- 採用階梯式加藥直至達標,而非僅追求「百分比降幅」
- 同步監測 non-HDL-C 和 ApoB 作為配套目標(特別是 TG 偏高或 LDL-C 已達標但 non-HDL-C 未達標時)
- 對高風險一級預防患者亦設立 LDL-C <70 mg/dL 目標(COR 2a)
證據層級與限制
- COR 1(A)用於 ASCVD 二級預防目標
- COR 2a(B-R / B-NR)用於一級預防目標
- Tier 分類:Tier 1 (direct_guideline) + Tier 2 (trial_supported — FOURIER/ODYSSEY/CTT)
- 限制:數值目標源自 RCT 事後分析和 meta-analysis,而非以特定數值目標作為隨機化設計特徵的前瞻性試驗
#5 風險評估工具更換:PCE → PREVENT-ASCVD(去種族化,估算值普降 40–50%)🔄
變更概述
2026 指引以 AHA PREVENT-ASCVD 方程式正式取代 2013 年的 Pooled Cohort Equations(PCE),是風險評估框架的根本性更新。
2018 怎麼寫
"Use the PCE to estimate 10-year ASCVD risk for adults aged 40–75 years." 高風險閾值 ≥20%;含種族(黑人/白人二元分類)作為計算變量。
2026 怎麼寫
"PREVENT-ASCVD risk calculator is recommended for estimation of 10-year absolute risk of ASCVD" (COR 1, LOE B-NR);成人 30–79 歲;高風險閾值 ≥10%;移除種族變量;納入 eGFR 和社會剝奪指數(SDI);提供 10 年及 30 年風險估算。
為什麼改
PCE 基於 1960–1980 年代的隊列推導,在當代人群中系統性高估 ASCVD 風險 40–50%。此外,PCE 使用種族作為生物學計算變量引發公平性爭議——種族是社會建構,非生物學風險因子。Khan et al. 2024 基於 330 萬現代美國 EHR 數據推導 PREVENT 方程式,證明移除種族後預測力未減損(C-statistic:女性 0.794,男性 0.757),且校準準確性大幅優於 PCE。
關鍵文獻深讀
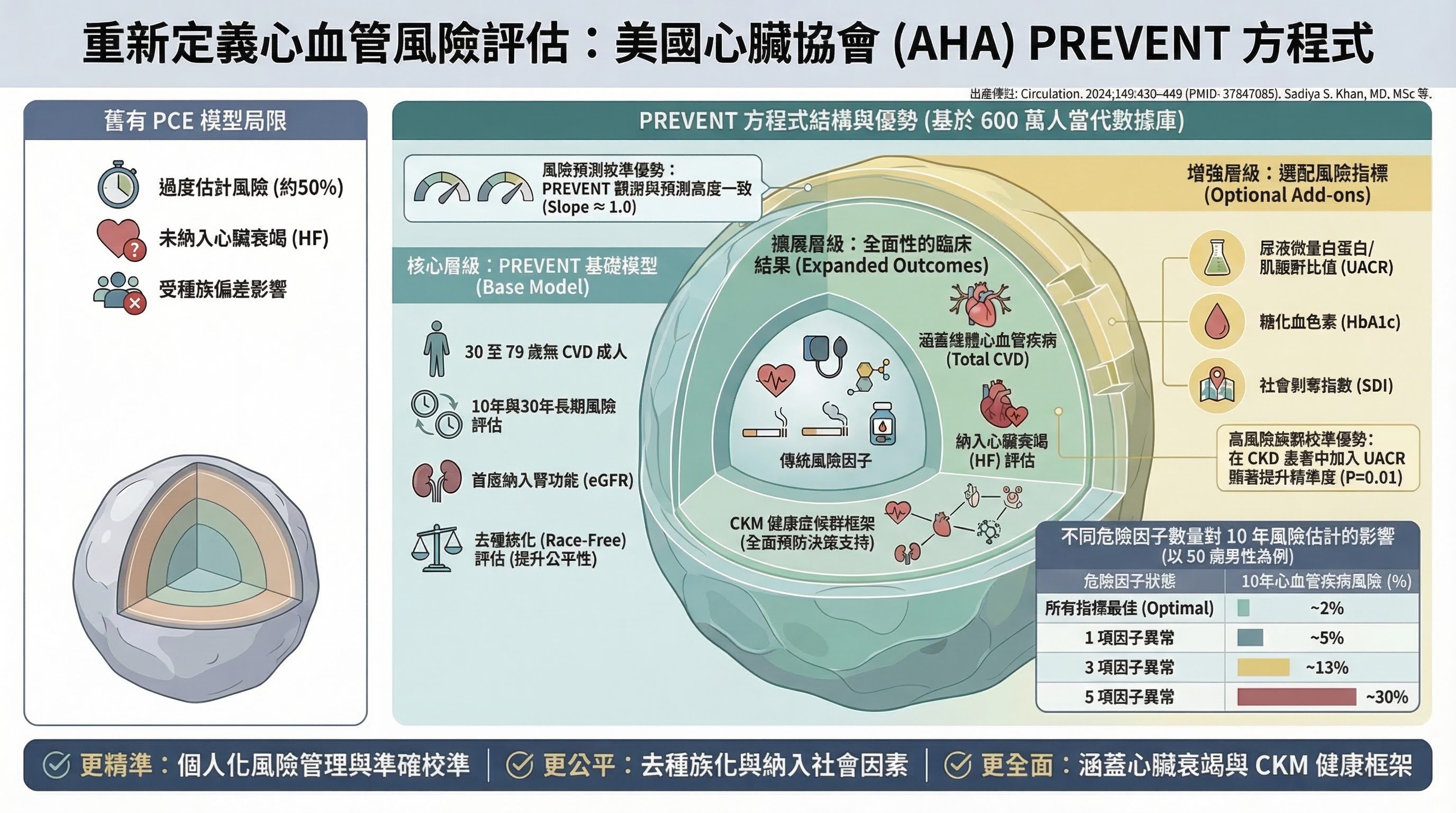
PREVENT 方程式開發研究 (Khan SS et al., Circulation 2024, PMID 37947085)
- 研究設計:橫斷面隊列推導 + 驗證研究
- PICO:P = 美國成人 30–79 歲;I = PREVENT-ASCVD 方程式;C = PCE;O = ASCVD 事件預測準確性
- 主要發現:N = 330 萬推導,N = 170 萬驗證;C-statistic 0.794(女性)/ 0.757(男性)——與 PCE 相當;校準準確性大幅優於 PCE;移除種族後預測力未減損;納入 eGFR 改善 CKD 患者風險分層
- 為什麼重要:解決 PCE 系統性高估的問題,同時在公平性上移除種族變量
- 主要限制:基於美國 EHR 數據,非美國人群的外部驗證尚未完成;SDI 為選擇性輸入
臨床意義
同一患者的 PREVENT 估算值通常較 PCE 低 40–50%(校準修正,非患者族群改變)。重要數學等效:PCE ≥20% ≈ PREVENT ≥10%(同等高風險群體)。所有使用 PCE 的既有患者需重新評估,確保溝通框架正確。
實務建議
- 立即在臨床系統中更換為 PREVENT-ASCVD 計算器(https://prevent.heart.org)
- 重新評估所有曾使用 PCE 評估的患者,特別是邊界/中等風險者
- 向患者說明:風險數字降低不代表「風險改善了」,而是「計算更準確了」
- 利用 30 年風險功能評估 30–39 歲年輕成人的終生風險(這是 PREVENT 新增功能)
- 注意新閾值:低 <3%、邊界 3–5%、中等 5–10%、高 ≥10%
證據層級與限制
- COR 1(B-NR)
- Tier 分類:Tier 1 (direct_guideline) + Tier 2 (trial_supported — Khan 2024)
- 限制:基於美國人群推導;亞洲、歐洲、非洲人群的外部驗證待完成
#6 Lp(a) 全體成人強制一次性篩查(COR 1)🆕
變更概述
Lp(a) 從 2018 年的「選擇性風險強化因子」大幅升格為 2026 年的「所有成人至少一次測量」(COR 1),是預防心血管疾學領域最重要的篩檢策略變更之一。
2018 怎麼寫
Lp(a) 列為可選擇性測量的風險強化因子之一,主要對象為有 ASCVD 家族史的高風險族群;無明確 COR;閾值未統一。
2026 怎麼寫
"Measurement of Lp(a) at least once in all adults is recommended" (COR 1, LOE B-NR)。閾值:≥125 nmol/L(≥50 mg/dL)→ 風險強化因子;≥250 nmol/L(≥100 mg/dL)→ ≥2 倍 ASCVD 風險。ASCVD 患者若 Lp(a) ≥125 nmol/L 且 LDL-C 未達標 → PCSK9 mAb(COR 1)。
為什麼改
三方面證據匯聚:(1) Mendelian randomization 研究確認 Lp(a) 與 ASCVD 的因果關聯(非僅關聯性),(2) Lp(a) 水平 80% 由遺傳決定、終生穩定(一次測量即足),(3) PCSK9 mAb 可降 Lp(a) ~27%,且高 Lp(a) 患者從 PCSK9 mAb 獲得更大 CV 獲益。EAS 2022 Consensus 綜合上述證據,建議全體成人篩查,2026 年 ACC/AHA 正式採納。
關鍵文獻深讀
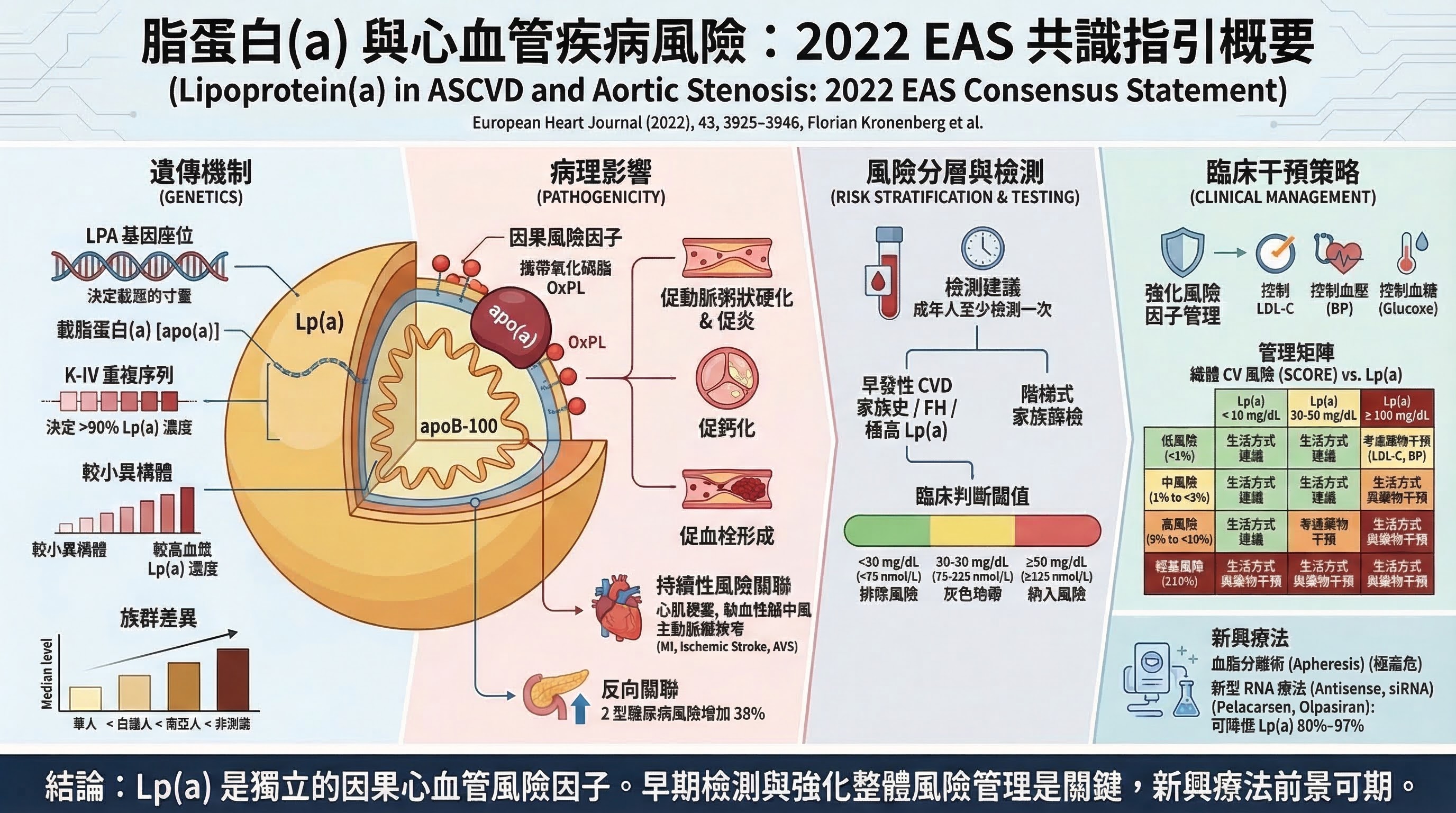
EAS 2022 Consensus (Kronenberg F et al., Eur Heart J 2022, PMID 36036785)
- 研究設計:系統性文獻回顧 + 專家共識聲明
- 主要發現:Lp(a) 水平 80% 由遺傳決定;終生穩定(一次測量即足);Mendelian randomization 確認因果關聯;≥125 nmol/L 為風險升高閾值
- 為什麼重要:提供 Lp(a) 全體篩查的完整理論框架
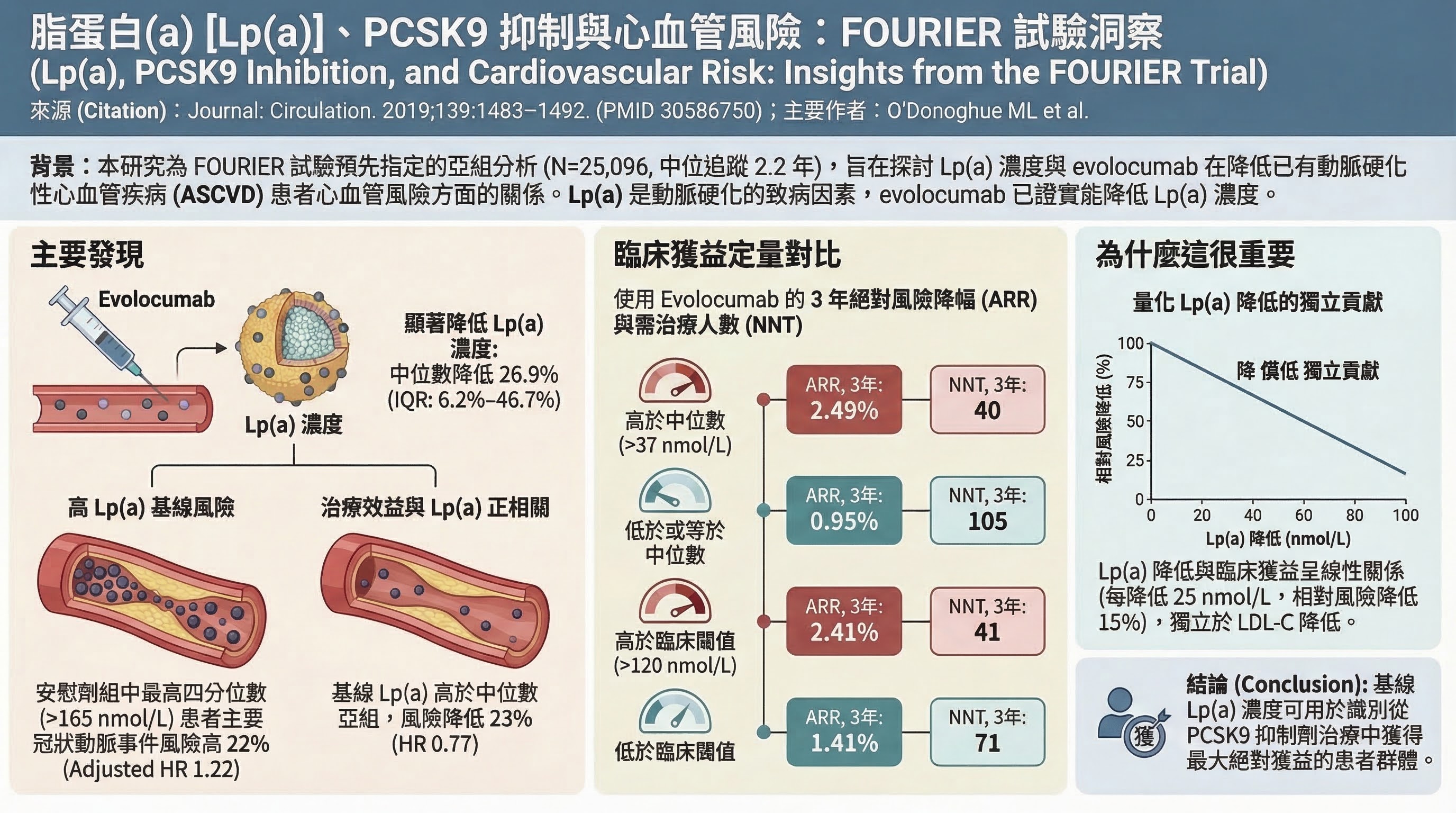
FOURIER Lp(a) 子研究 (O'Donoghue ML et al., Circulation 2019, PMID 30586750)
- 研究設計:FOURIER 試驗預先指定的 Lp(a) 亞組分析
- 主要發現:evolocumab 降 Lp(a) ~27%;高 Lp(a) 四分位亞組 MACE HR 0.77(ARR 2.49%,NNT 40)
- 為什麼重要:量化 Lp(a) 降低對 CV 事件的獨立貢獻
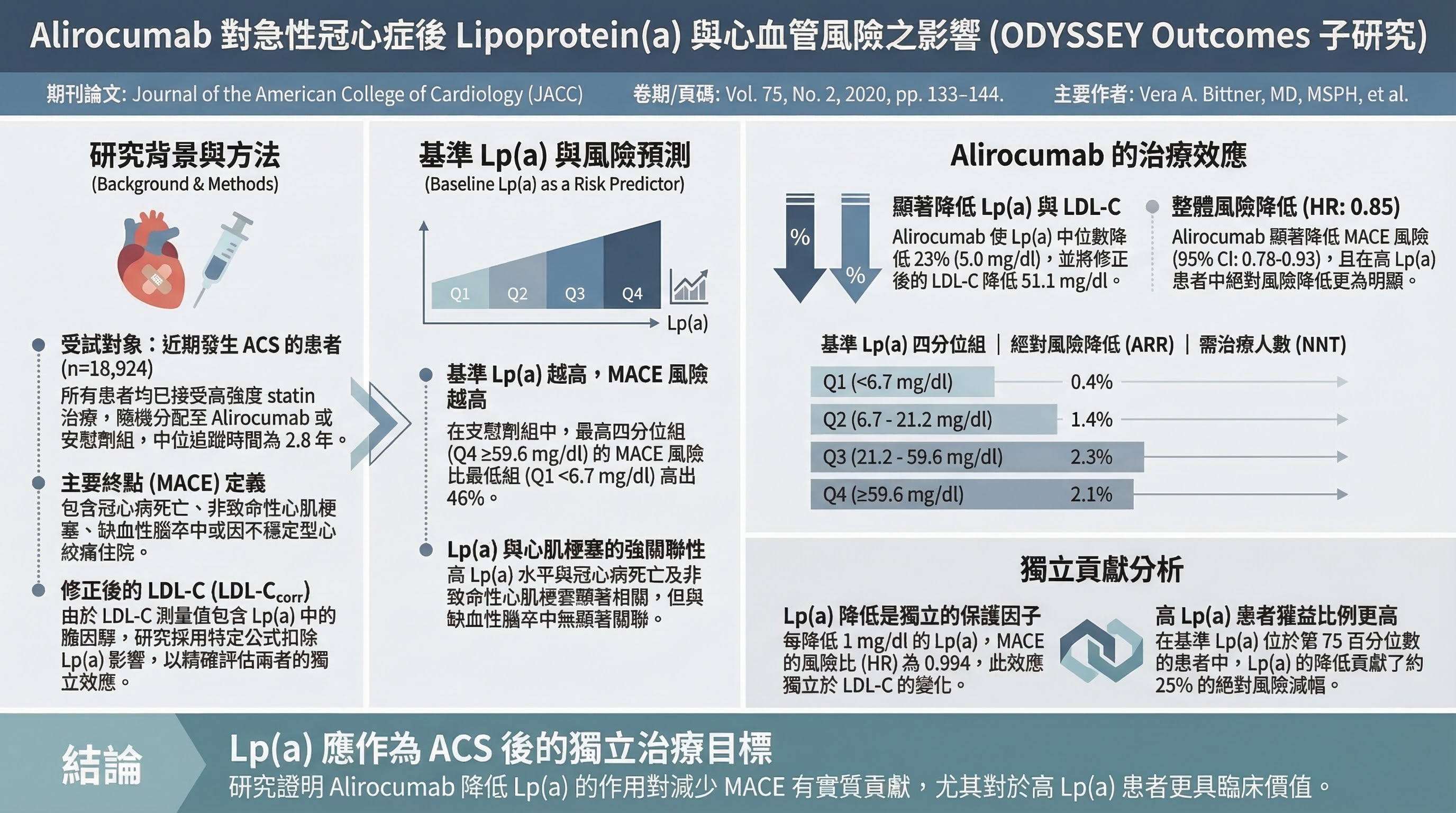
ODYSSEY Lp(a) 子研究 (Bittner VA et al., JACC 2020, PMID 31948641)
- 主要發現:alirocumab CV 獲益約 25% 可歸因於 Lp(a) 降低
- 為什麼重要:跨藥物驗證 Lp(a) 降低的獨立 CV 效益
臨床意義
美國成人約 20%(>6,000 萬人)有 Lp(a) ≥125 nmol/L。目前尚無 Lp(a) 特異性療法獲批(pelacarsen、olpasiran、lepodisiran 均在第三期試驗),但高 Lp(a) 應觸發更積極的 LDL-C 目標和全面風險因子管理。
實務建議
- 對所有成人開立一次性 Lp(a) 檢測(無需空腹)
- 結果報告以 nmol/L 為標準單位(不同實驗室方法間 mg/dL 換算不一致)
- Lp(a) ≥125 nmol/L:列為風險強化因子,升級風險分層
- Lp(a) ≥250 nmol/L:視同 ≥2 倍 ASCVD 風險
- ASCVD 患者 + Lp(a) ≥125 nmol/L + LDL-C 未達標:PCSK9 mAb(COR 1)
證據層級與限制
- COR 1(B-NR)用於篩查
- Tier 分類:Tier 1 (direct_guideline — 篩查) + Tier 4 (future_direction — Lp(a) 特異性降脂藥物)
- 限制:目前可行動的治療選項有限(僅降 LDL-C + 全面風險管理);Lp(a) 特異性療法 CVOT 尚未完成
#7 CAC 評分升格為 COR 1,並建立 CAC 分層 LDL-C 目標 📊
變更概述
CAC 從 2018 年的「決策輔助工具(Class IIa)」升格為 2026 年的「推薦使用(COR 1)」,並首次建立 CAC 分層與 LDL-C 數值目標的對應關係。CAC ≥1000 AU 被視為等同 VHR ASCVD 的風險層級。
2018 怎麼寫
"If risk decision is uncertain, it is reasonable to measure a CAC score" (Class IIa)。用於中等風險決策輔助;無明確 LDL-C 目標連結;CAC=0 重新評估間隔 5–10 年。
2026 怎麼寫
決策不確定的中等/邊界風險患者 COR 1(推薦);首次建立 CAC 分層 LDL-C 目標(CAC 1–99 → <100;CAC ≥100 → <70;CAC ≥1000 → <55 mg/dL 等同 VHR);偶然 CT 發現 CAC:COR 1 納入治療決策;CAC=0 → 暫緩藥物治療並於 3–7 年重新評估(COR 2a, LOE B-NR);新增性別特異性年齡閾值(男 ≥40,女 ≥45 歲)。
為什麼改
MESA 長期追蹤和 CAC Consortium 大型隊列數據持續累積,證明 CAC 提供獨立於傳統風險因子的預後資訊。特別關鍵的是 CAC ≥1000 AU 的發現:此族群的年化 CVD 死亡率接近 FOURIER 試驗安慰劑組(已確診高風險 ASCVD),支持以二級預防 VHR 強度治療。此外,AI 演算法在偶然 CT(如肺癌篩查)上偵測 CAC 的技術成熟,使得 CAC 資訊的可得性大幅提升。
關鍵文獻深讀
MESA 及 CAC Consortium 長期隊列
- 研究設計:多中心前瞻性隊列研究(MESA:N = 6,814,追蹤 >15 年)
- 主要發現:CAC ≥1000 AU 的 10 年 ASCVD 事件率 >20%(等同高風險二級預防);CAC = 0 的 10 年 ASCVD 事件率 <2%(即使有多重風險因子)
- 為什麼重要:為 CAC 分層目標提供流行病學基礎
- 主要限制:觀察性數據外推為治療目標,無以 CAC 分層為隨機化設計特徵的 RCT
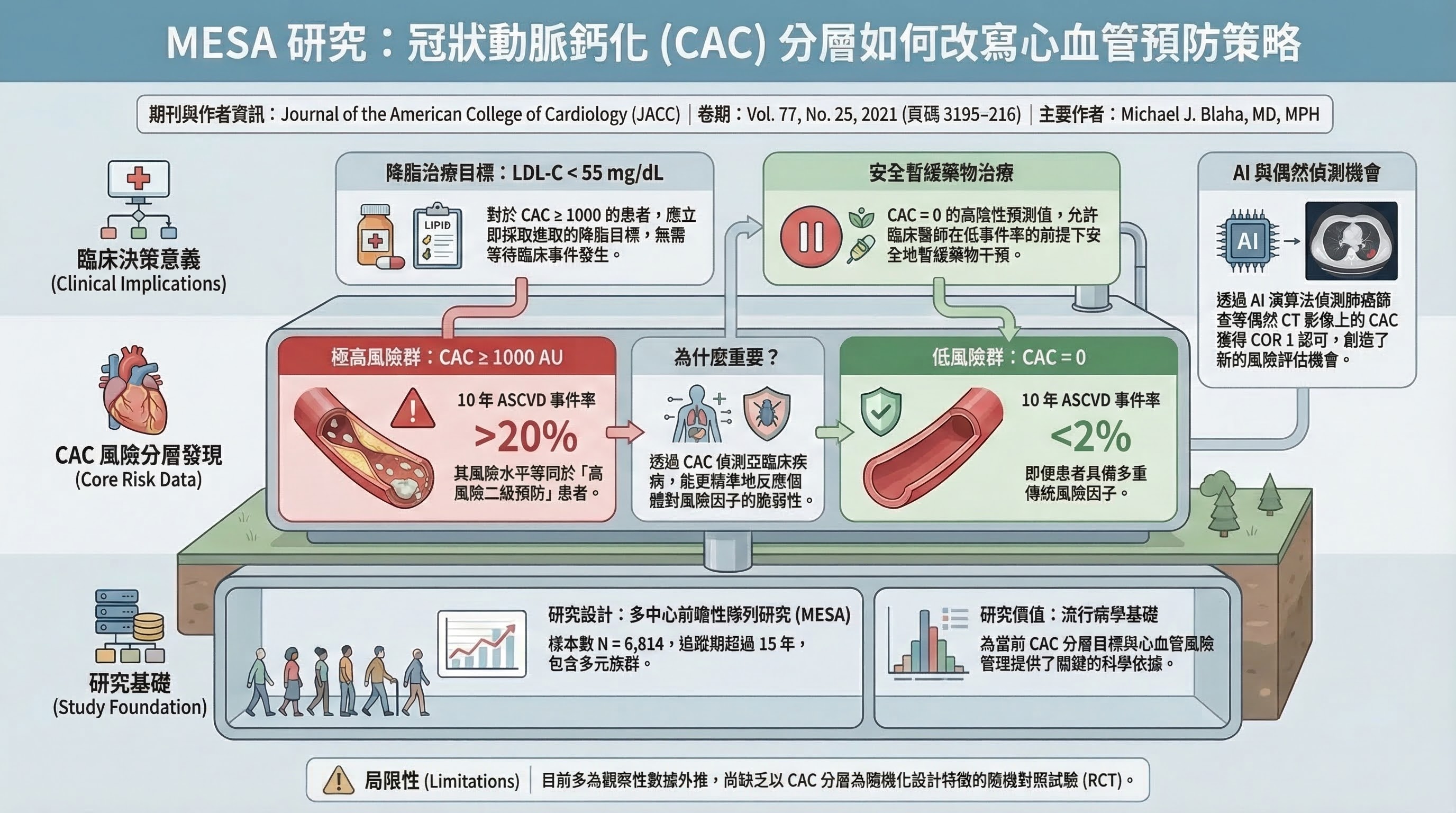
臨床意義
CAC ≥1000 患者現在應以 <55 mg/dL 為 LDL-C 目標,無需等待臨床 ASCVD 事件。AI 演算法偵測偶然 CT 上的 CAC 獲 COR 1 認可,為肺癌篩查 CT 等創造心血管風險評估機會。CAC = 0 的高陰性預測值允許安全暫緩藥物治療。
實務建議
- 風險決策不確定時(邊界/中等風險),CAC 現為 COR 1 推薦(非僅「合理」)
- CAC ≥1000 AU:目標 LDL-C <55 mg/dL(等同 VHR ASCVD 強度)
- CAC = 0:可暫緩藥物治療,3–7 年後重新評估(COR 2a, LOE B-NR)
- 偶然 CT 發現的 CAC(如肺癌篩查、胸部 CT):COR 1 納入治療決策
- 注意性別特異性年齡閾值:男性 ≥40 歲、女性 ≥45 歲方可使用 CAC 評分
證據層級與限制
- COR 1(B-NR)用於 CAC 使用推薦
- COR 2a(B-NR)用於 CAC = 0 暫緩治療及 3–7 年重新評估
- Tier 分類:Tier 1 (direct_guideline — CAC 使用) + Tier 3 (observational_extrapolation — CAC 連結的數值目標)
- 限制:CAC 分層 LDL-C 目標為觀察性外推(LOE B-NR),無以 CAC 分層為隨機化設計特徵的 RCT
#8 HFrEF 無 ASCVD 共病者:Statin 從「可考慮」降格為「不推薦」 ❌
變更概述
2026 指引明確將 HFrEF 無臨床 ASCVD 的 statin 治療從 2018 年的 Class IIb(可考慮)降格為 COR 3: No Benefit,是指引罕見的「主動否定」一個有生物學合理性的療法。
2018 怎麼寫
"In patients with NYHA class II-IV ischemic systolic heart failure who have a reasonable life expectancy (3-5 y), who are already on a statin for an ASCVD indication, it may be reasonable to continue statin therapy." (Class IIb, LOE B-R)
2026 怎麼寫
HFrEF 無臨床 ASCVD:COR 3: No Benefit(LOE B-R)——不推薦單純以改善 HF 預後為目的啟動 statin。
HFrEF 合併缺血性病因/ASCVD——新啟動 statin:COR 2b(LOE B-R);已在使用 statin 者繼續:COR 1(LOE A)。
為什麼改
CORONA 和 GISSI-HF 兩大 RCT(合計 N = 9,642)對 HFrEF 患者使用 rosuvastatin 均得出一致陰性結果,確認 statin 無法改善 HFrEF 預後。這兩項試驗在 2018 年即已發表,但 2018 指引僅給予 Class IIb。2026 指引在 8 年無新支持性證據的情況下,正式降格為 COR 3: No Benefit,同時精細化依 ASCVD 共病狀態分層。
關鍵文獻深讀
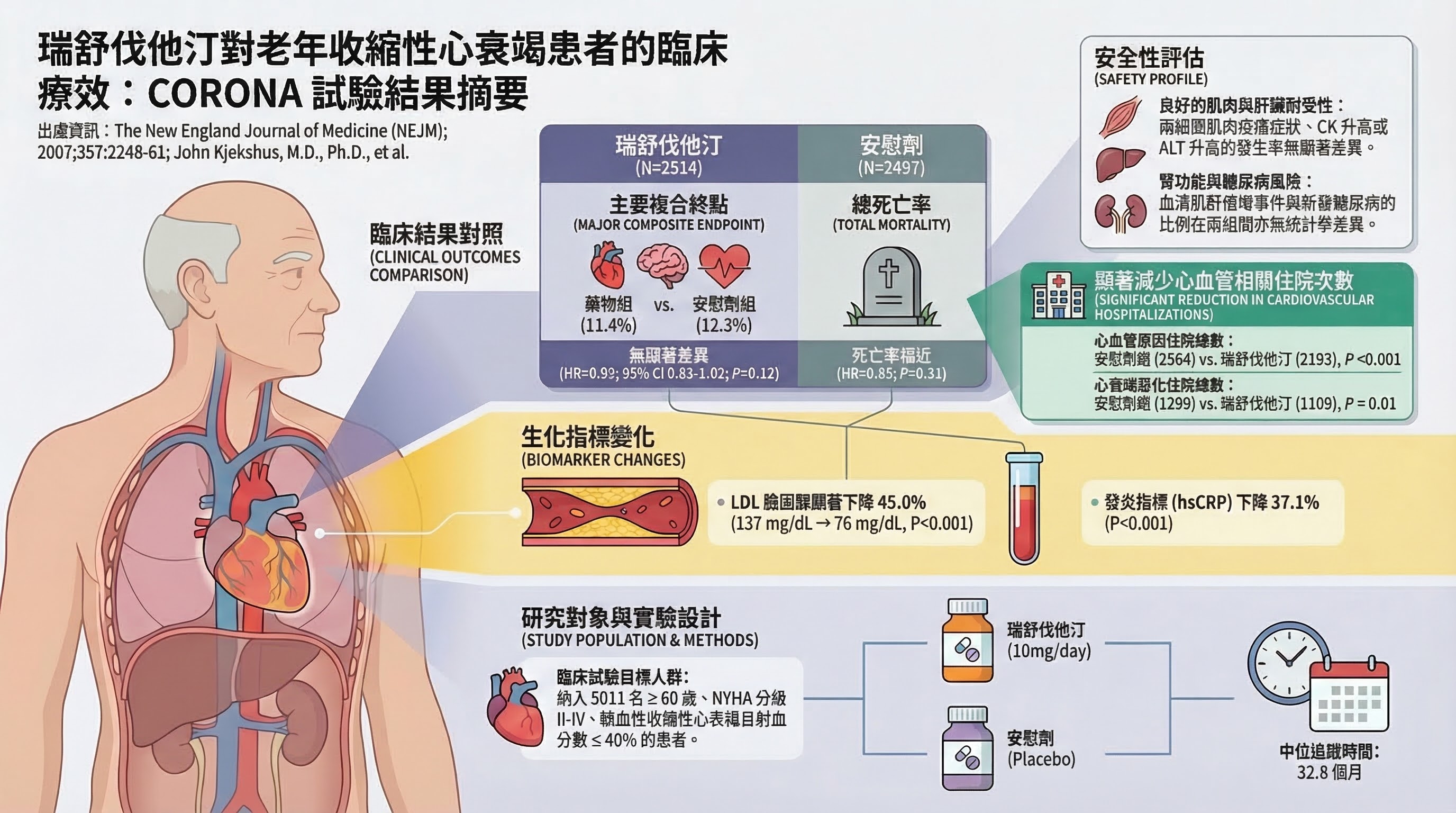
CORONA (Kjekshus J et al., NEJM 2007, PMID 17984166)
- 研究設計:多中心、隨機、雙盲、安慰劑對照 RCT
- PICO:P = 缺血性 HFrEF(NYHA II–IV,EF ≤40%,年齡 ≥60)N = 5,011;I = rosuvastatin 10 mg;C = 安慰劑;O = CV 死亡、非致命 MI、非致命中風
- 主要發現:主要終點 HR 0.92(95% CI 0.83–1.02,P = 0.12)——未達統計意義
- 為什麼重要:首次在大型 RCT 中證明 statin 對 HFrEF 無 CV 事件獲益
- 主要限制:僅含缺血性病因;rosuvastatin 10 mg(非高強度)
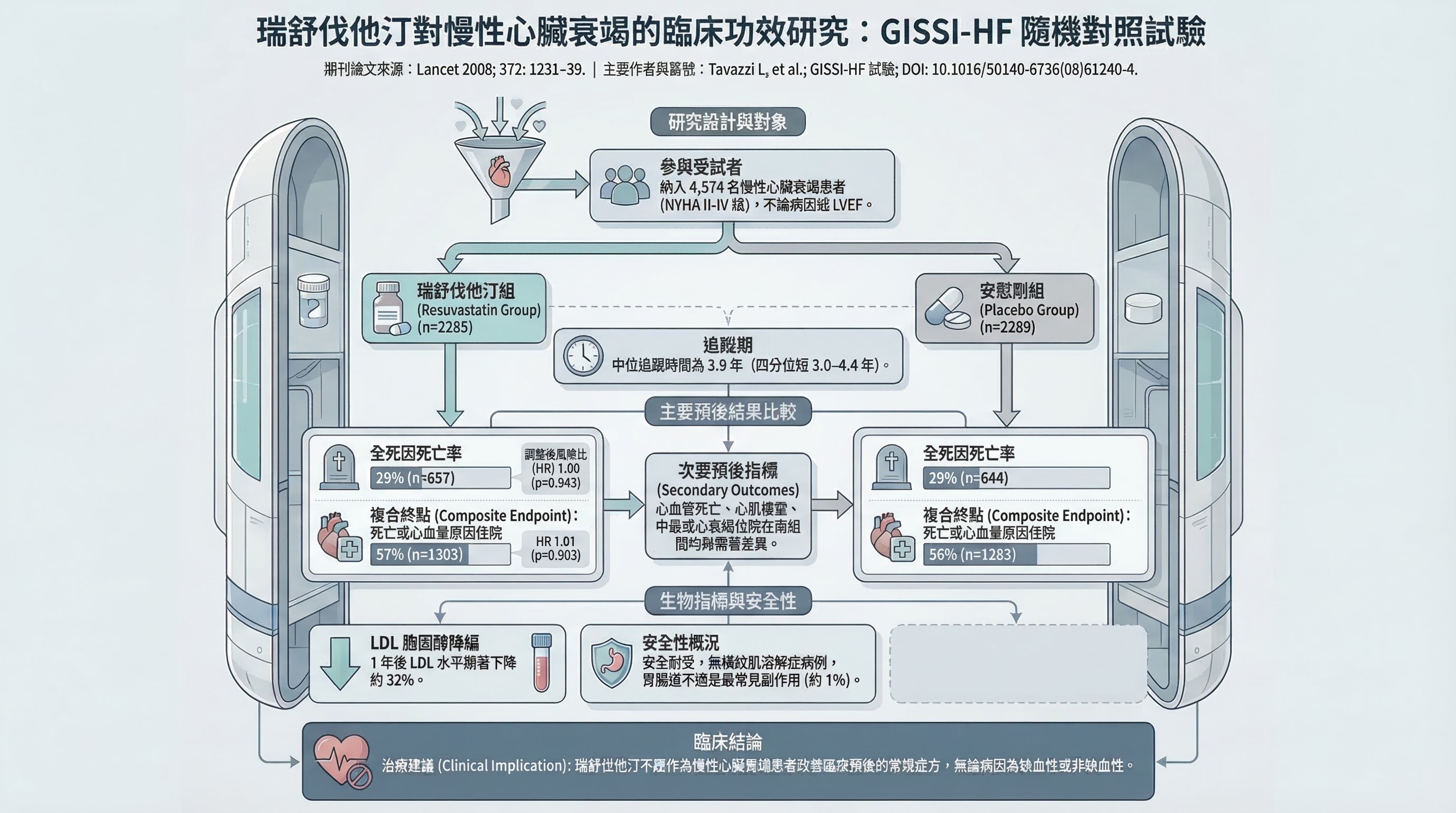
GISSI-HF (Tavazzi L et al., Lancet 2008, PMID 18757089)
- 研究設計:多中心、隨機、雙盲、安慰劑對照 RCT
- PICO:P = 各病因 HF(不限缺血性)N = 4,574;I = rosuvastatin 10 mg;C = 安慰劑;O = 全因死亡
- 主要發現:全因死亡 HR 1.00(95% CI 0.898–1.122,P = 0.943)——完全陰性
- 為什麼重要:擴大至所有病因 HF,仍確認 statin 無效
臨床意義
臨床關鍵:停止以「HFrEF」本身作為啟動 statin 的適應症。但需精細分層:若患者有明確缺血性病因/ASCVD 共病(如 HFrEF 由冠心病引起),新啟動 statin 為 COR 2b(B-R),已在使用者繼續為 COR 1(A)。
實務建議
- 檢視所有 HFrEF 患者的 statin 處方——若無明確 ASCVD 共病,重新評估是否繼續
- HFrEF 無 ASCVD:不應新啟動 statin(COR 3: No Benefit)
- HFrEF + 缺血性病因/ASCVD:已在使用者繼續(COR 1);新啟動為 COR 2b
- 注意:HFpEF 的 statin 推薦與 HFrEF 不同,需另行評估
證據層級與限制
- COR 3: No Benefit(B-R)用於 HFrEF 無 ASCVD
- COR 1(A)用於已在使用 statin 的 HFrEF + ASCVD 患者繼續治療
- Tier 分類:Tier 1 (direct_guideline) + Tier 2 (trial_supported — CORONA/GISSI-HF)
- 限制:CORONA 和 GISSI-HF 均使用 rosuvastatin 10 mg,高強度 statin 在 HFrEF 的效果未被測試
#9 HIV 患者(PLHIV)40–75 歲接受 statin 治療升格為 COR 1 🆕
變更概述
HIV 感染者(PLHIV)40–75 歲的 statin 治療從 2018 年的「風險強化因子(無明確 COR)」大幅升格為 2026 年的 COR 1(B-R),這是基於單一決定性 RCT(REPRIEVE)的重大推薦變更。
2018 怎麼寫
HIV 列為「慢性發炎疾病」風險強化因子之一;可作為中等風險決策的參考因素;無特定 COR 推薦 statin 治療。
2026 怎麼寫
"Statin therapy is recommended for people living with HIV (PLHIV) aged 40–75 years on stable antiretroviral therapy to reduce the risk of ASCVD." (COR 1, LOE B-R)
為什麼改
REPRIEVE 是第一個也是唯一一個專門針對 HIV 族群的 statin CVOT。此前,HIV 患者的 statin 使用建議僅基於流行病學觀察(HIV 患者 ASCVD 風險升高 1.5–2 倍)和一般人群 statin 試驗的外推。REPRIEVE 以 7,769 名 PLHIV 為入組人群,證明 pitavastatin 4 mg 降低 MACE 35%(HR 0.65),且因有效性提前停止。
關鍵文獻深讀
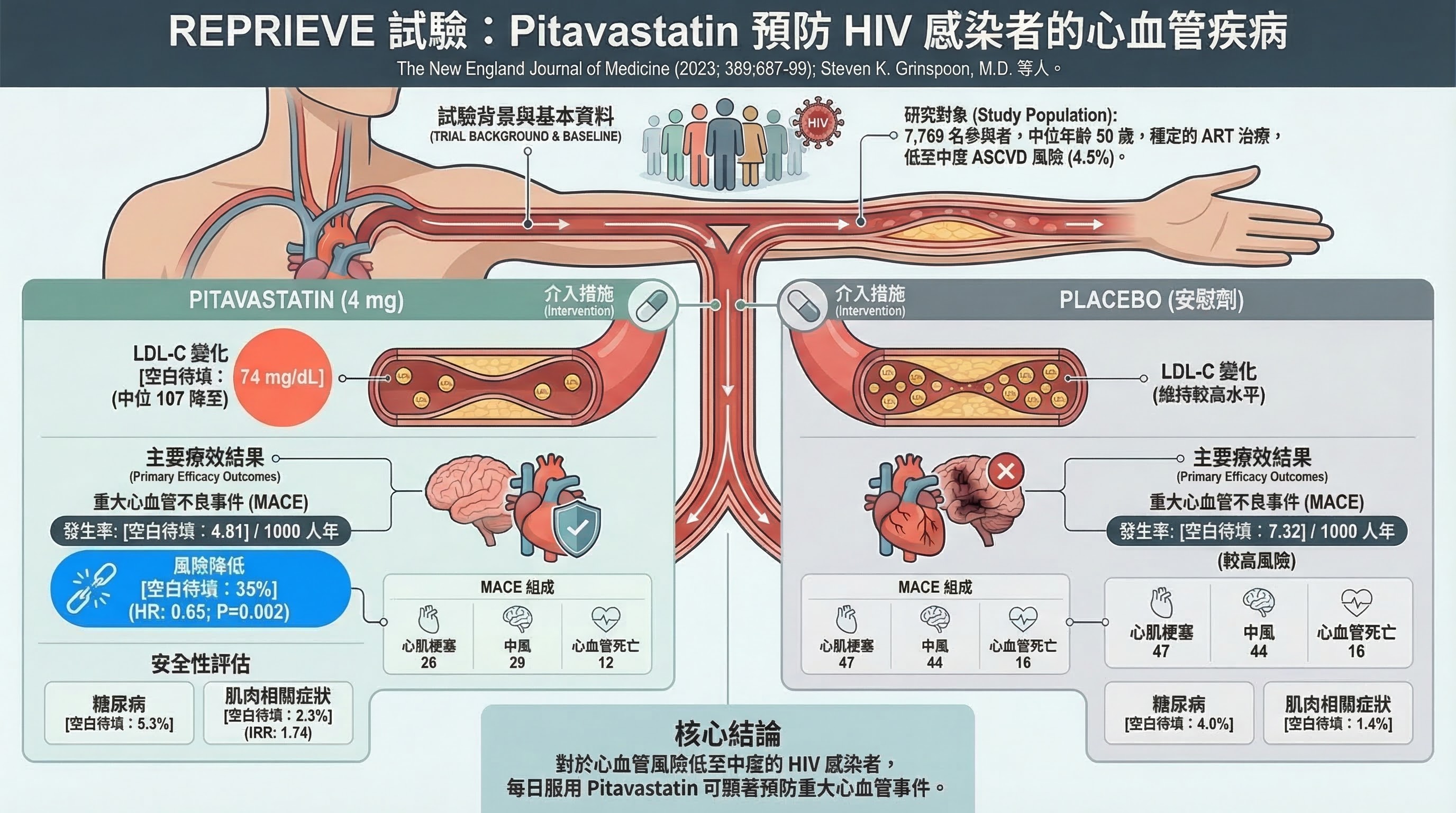
REPRIEVE (Grinspoon SK et al., NEJM 2023, PMID 37486775)
- 研究設計:多中心、隨機、雙盲、安慰劑對照 Phase 3 RCT
- PICO:P = PLHIV 40–75 歲,穩定 ART ≥6 個月,10 年 CV 風險中位數 4.5%(低至中等風險),N = 7,769;I = pitavastatin 4 mg/day;C = 安慰劑;O = MACE(CV 死亡、MI、UA 住院、中風、TIA、PCI/CABG、周邊動脈事件)
- 主要發現:MACE HR 0.65(95% CI 0.48–0.90,P = 0.002)——35% MACE 降低;因有效性提前停止(中位追蹤 5.1 年)
- 為什麼重要:(1) 首個 HIV 專屬 statin CVOT,(2) 即使估算 CV 風險「低至中等」仍顯著獲益(HR 0.65 vs 一般人群 FOURIER HR 0.85),反映慢性發炎促進動脈粥樣硬化的特殊機制,(3) Pitavastatin 不經 CYP3A4 代謝,避免與 ART 藥物(特別是蛋白酶抑制劑、NNRTI)的相互作用
- 主要限制:單一試驗;pitavastatin 專屬(其他 statin 的交互作用需另行評估);PLHIV 特有的代謝異常(脂肪萎縮、胰島素阻抗)可能影響 generalizability
臨床意義
REPRIEVE 以明確 RCT 證據確立 HIV 族群的 statin 治療建議,解決長期懸而未決的臨床疑問。HIV 患者即使估算 CV 風險「低至中等」仍獲益顯著(HR 0.65 vs FOURIER HR 0.85),反映慢性發炎促進動脈粥樣硬化的特殊機制。
實務建議
- 所有穩定 ART 治療的 PLHIV 40–75 歲,主動考慮啟動 statin
- 首選 pitavastatin 4 mg(REPRIEVE 使用藥物,且不經 CYP3A4 代謝,避免 ART 交互作用)
- 若 pitavastatin 不可得,rosuvastatin 為次選(CYP3A4 代謝最少的 statin 之一)
- 避免使用 simvastatin 和 lovastatin(與蛋白酶抑制劑有嚴重交互作用)
證據層級與限制
- COR 1(B-R)
- Tier 分類:Tier 1 (direct_guideline) + Tier 2 (trial_supported — REPRIEVE)
- 限制:單一 RCT;pitavastatin 專屬數據;PLHIV <40 歲或 >75 歲未被涵蓋
#10 Olezarsen(apoC-III ASO)為家族性乳糜血症(FCS)獲 COR 1 推薦 💊
變更概述
Olezarsen 成為首個有 RCT 支持的 FCS 藥物治療選項,填補了此罕見遺傳疾病長期缺乏有效藥物的空白。
2018 怎麼寫
FCS 無特定藥物推薦;生活方式加 fibrates/omega-3,但因 FCS 患者缺乏 LPL 活性,這些藥物效果甚微。
2026 怎麼寫
"Olezarsen 80 mg subcutaneously monthly is recommended for patients with genetically confirmed FCS and TG ≥1000 mg/dL." (COR 1, LOE B-R)
為什麼改
BALANCE 試驗首次在 FCS 患者中證明 olezarsen(apoC-III 反義寡核苷酸)可顯著降低 TG(43.5%)並大幅減少急性胰臟炎發作。FCS 的機制特殊:LPL 完全缺失,傳統降 TG 藥物(fibrates、omega-3)均依賴 LPL 活性,因此對 FCS 無效。Olezarsen 透過抑制 apoC-III 增強 LPL 以外的 TG 清除途徑,在 LPL 缺失的 FCS 中仍能發揮作用。
關鍵文獻深讀
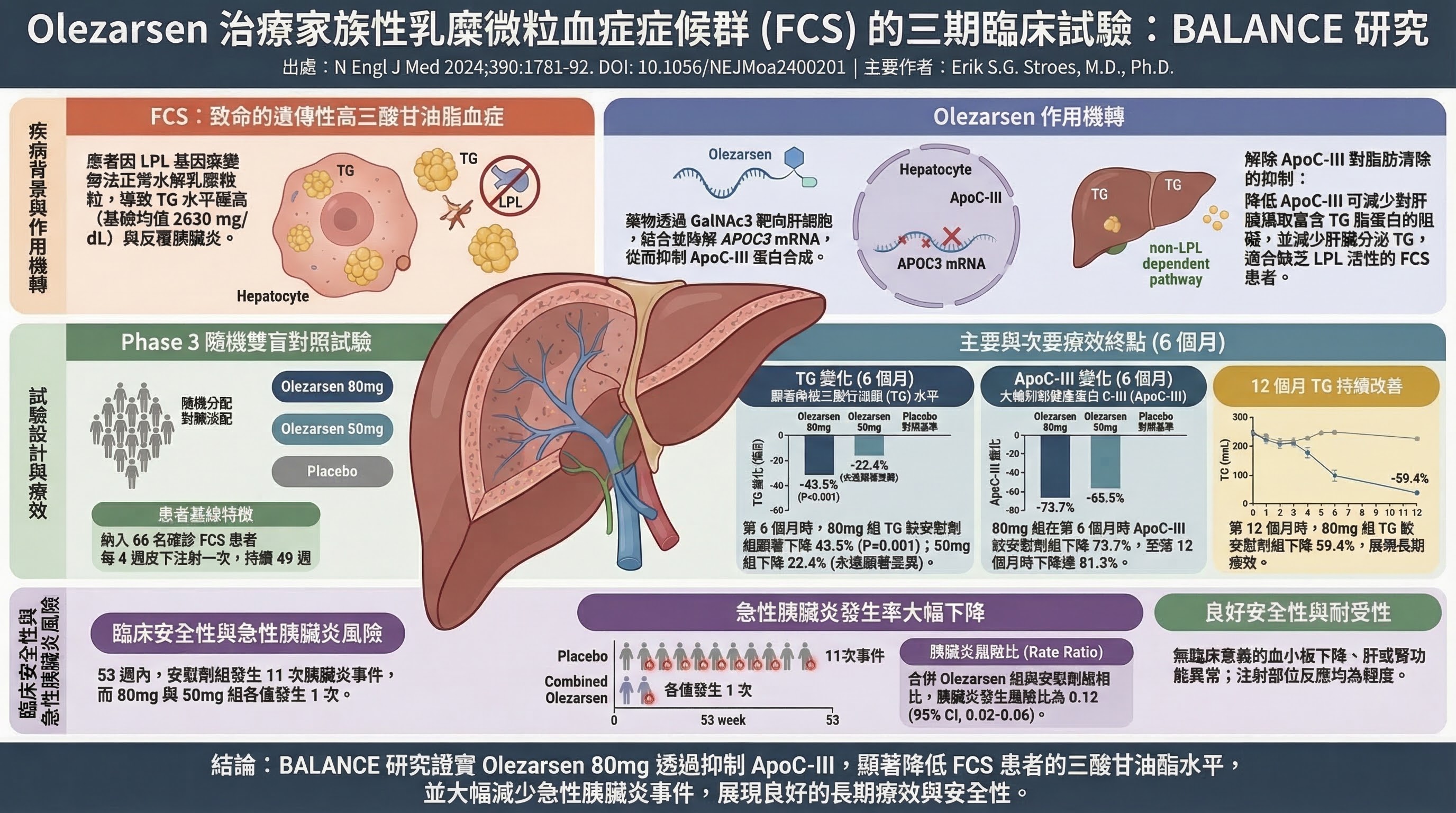
BALANCE (Stroes ESG et al., NEJM 2024, PMID 38587247)
- 研究設計:多中心、隨機、雙盲、安慰劑對照 Phase 3 RCT
- PICO:P = 基因確認 FCS + TG ≥1000 mg/dL,N = 57(FCS 罕見疾病);I = olezarsen 50 mg 或 80 mg SC Q4W;C = 安慰劑;O = TG 百分比降幅
- 主要發現:olezarsen 80 mg 降 TG 43.5%(95% CI -69.1 to -17.9,P < 0.001);急性胰臟炎:rate ratio 0.12(95% CI 0.02–0.66)——olezarsen 組 1 次 vs 安慰劑組 11 次
- 為什麼重要:FCS 年胰臟炎復發率高(可致死或嚴重殘疾),olezarsen 提供首個有 RCT 支持的藥物治療
- 主要限制:樣本量極小(N = 57,罕見疾病);短期追蹤;industry sponsored(Ionis)
臨床意義
FCS 年胰臟炎復發率高(可致死或嚴重殘疾),olezarsen 提供首個有 RCT 支持的藥物治療選項。此推薦僅適用基因確認 FCS,不適用多基因型高三酸甘油酯血症。
實務建議
- 確認 FCS 診斷需基因檢測(雙等位基因 LPL、GPIHBP1、APOC2、APOA5 或 LMF1 變異)
- TG ≥1000 mg/dL 的基因確認 FCS 患者:啟動 olezarsen 80 mg SC 每月一次
- 繼續極低脂飲食(<10–15% 熱量來自脂肪)
- 多基因型高 TG 血症不適用 olezarsen
證據層級與限制
- COR 1(B-R)
- Tier 分類:Tier 1 (direct_guideline) + Tier 2 (trial_supported — BALANCE)
- 限制:極小樣本 RCT(N = 57);僅適用基因確認 FCS;長期安全性數據有限
3. 綜合比較表
3.1 風險評估工具對照(PCE vs PREVENT-ASCVD)
| 特性 | PCE(2018) | PREVENT-ASCVD(2026) |
|---|---|---|
| 推導樣本 | ~25,000 人(1960–1980 年代隊列) | 330 萬現代美國人 |
| 適用年齡 | 40–79 歲 | 30–79 歲(擴大) |
| 種族變量 | 是(白人/黑人二元) | 否(種族移除) |
| eGFR 納入 | 否 | 是 |
| 社會剝奪指數(SDI) | 否 | 是(選擇性輸入) |
| 30 年終生風險 | 部分 | 是 |
| 風險估算偏差 | 高估 40–50% | 校準良好 |
| COR/LOE | 未明確 COR(默認使用) | COR 1, LOE B-NR |
| 風險層次閾值 | 低 <5%;邊界 5–7.5%;中等 7.5–20%;高 ≥20% | 低 <3%;邊界 3–5%;中等 5–10%;高 ≥10% |
3.2 各風險族群 LDL-C/Non-HDL-C/ApoB 目標值
| 風險族群 | 2018 方式 | 2026 LDL-C | 2026 Non-HDL-C | 2026 ApoB | 2026 COR/LOE |
|---|---|---|---|---|---|
| VHR ASCVD(≥2 次大事件,或 1+≥2 高風險條件) | ≥70 mg/dL 觸發加藥 | <55 mg/dL | <85 mg/dL | <55 mg/dL | COR 1, LOE A |
| ASCVD(非 VHR) | ≥50% 降幅 | <70 mg/dL | <100 mg/dL | <70 mg/dL | COR 1, LOE A |
| ASCVD 非 VHR(選擇性強化) | 無 | <55 mg/dL | <85 mg/dL | <55 mg/dL | COR 2a, LOE B-R |
| 一級預防,高風險(PREVENT ≥10%) | ≥50% 降幅 | <70 mg/dL | <100 mg/dL | <70 mg/dL | COR 2a, LOE B-R |
| 一級預防,中等/邊界(PREVENT 3–10%) | ≥30% 降幅 | <100 mg/dL | <130 mg/dL | <90 mg/dL | COR 2a, LOE B-NR |
| 糖尿病(標準,40–75 歲) | ≥30% 降幅 | <100 mg/dL | <130 mg/dL | <90 mg/dL | COR 1, LOE A |
| 糖尿病(多重危險因素或 PREVENT ≥10%) | ≥50% 降幅 | <70 mg/dL | <100 mg/dL | <70 mg/dL | COR 2a, LOE B-R |
| FH 無 ASCVD | LDL-C <100 觸發 ezetimibe 閾值 | <70 mg/dL | <100 mg/dL | <70 mg/dL | COR 1, LOE B-R |
| FH + ASCVD | VHR 標準 | <55 mg/dL | <85 mg/dL | <55 mg/dL | COR 1, LOE B-R |
| CAC 1–99 AU | 考慮啟動 statin(無目標) | <100 mg/dL | <130 mg/dL | <90 mg/dL | COR 2a, LOE B-R |
| CAC 100–299 AU | 推薦啟動 statin(無目標) | <70 mg/dL | <100 mg/dL | <70 mg/dL | COR 1, LOE B-R |
| CAC 300–999 AU | 推薦啟動 statin(無目標) | <70 mg/dL(標準);選擇性強化 <55 | <100 mg/dL(標準);選擇性強化 <85 | <70 mg/dL(標準);選擇性強化 <55 | COR 1, LOE B-R |
| CAC ≥1000 AU(VHR 等同) | 無先前建議 | <55 mg/dL | <85 mg/dL | <55 mg/dL | COR 1, LOE B-NR |
3.3 藥物治療推薦變化(含 COR/LOE)
| 藥物/類別 | 2018 最強 COR | 2026 最強 COR | 主要改變 |
|---|---|---|---|
| Statin(ASCVD) | Class I, LOE A | COR 1, LOE A | LDL-C 數值目標新增 |
| Statin(HFrEF 無 ASCVD) | Class IIb, LOE B-R | COR 3: No Benefit, LOE B-R;合併缺血性/ASCVD——新啟動:COR 2b(B-R),繼續:COR 1(A) | 無 ASCVD 降格;合併 ASCVD 分層 |
| Statin(HIV PLHIV 40–75y) | 無明確 COR | COR 1, LOE B-R | 全新強推薦 |
| Ezetimibe(VHR ASCVD) | Class IIa, LOE B-R | COR 2a, LOE B-R | 序貫要求廢除 |
| Ezetimibe(LDL-C ≥190 mg/dL) | Class IIa, LOE B-R | COR 1, LOE A | 大幅升格 |
| Ezetimibe(CKD 未達標) | 未明確推薦 | COR 2a, LOE B-R | 全新推薦 |
| PCSK9 mAb(VHR ASCVD) | Class IIa, LOE A-SR(需先用 ezetimibe) | COR 2a, LOE A(無序貫要求) | 序貫廢除;費用說明移除 |
| PCSK9 mAb(HeFH + ASCVD) | Class IIb, LOE B-R | COR 1, LOE B-R | 大幅升格 |
| Bempedoic acid(SAMS + ASCVD) | 不存在 | COR 1, LOE B-R | 全新藥物 |
| Bempedoic acid(二級預防 add-on) | 不存在 | COR 2a, LOE B-R | 全新藥物 |
| Inclisiran(VHR 替代選項) | 不存在 | COR 2a, LOE B-NR | 全新藥物(二線 PCSK9i) |
| Icosapent ethyl(ASCVD + TG 150–499) | 未在指引 | COR 2b, LOE B-R | 新增(謹慎推薦) |
| Fibrates(ASCVD 事件預防) | 不推薦 | 不推薦(措辭更強) | PROMINENT 進一步否定 |
| Olezarsen(FCS, TG ≥1000) | 不存在 | COR 1, LOE B-R | 全新藥物(罕見病) |
| Evinacumab(HoFH) | 不存在 | COR 2b, LOE B-R | 全新選項 |
| 膳食補充劑(魚油、植物固醇、紅麴米) | 無 COR(中立) | COR 3: No Benefit, LOE B-R | 首次明確反對 |
3.4 特殊族群主要改變
| 族群 | 2018 主要推薦 | 2026 主要改變 | 驅動證據 |
|---|---|---|---|
| 糖尿病(40–75 歲) | 中強度 statin(Class I);高強度:Class IIa | 恢復數值目標(<100 或 <70 mg/dL);bempedoic acid + IPE 新增;PREVENT ≥10% 取代 PCE ≥20% 閾值 | IMPROVE-IT DM 亞組;CLEAR Outcomes;REDUCE-IT |
| CKD 非透析 | Class IIa(中/高強度 statin) | COR 1, LOE A;LDL-C <100;CKD + ASCVD → <55 mg/dL(COR 1) | SHARP(PMID 21663949)+ CTT |
| 透析患者 | Class IIa(合理) | 新啟動:COR 3: No Benefit(B-R)(一級預防不常規啟動);轉入透析者繼續既有 statin:COR 2b(C-LD) | SHARP 透析亞組陰性;4D;AURORA |
| HFrEF(無 ASCVD) | Class IIb(缺血性 HFrEF) | 無 ASCVD:COR 3: No Benefit(B-R);合併缺血性/ASCVD——新啟動:COR 2b(B-R),繼續:COR 1(A) | CORONA + GISSI-HF |
| ≥75 歲(一級預防新啟動) | Class IIa(合理) | COR 2b(B-NR);CAC 可輔助決策(COR 2b, B-NR) | 一級預防新啟動為 2b,非 2a |
| ≥75 歲(二級預防繼續) | Class IIa(合理) | COR 1(源自一般 ASCVD 推薦;需生命預期 ≥2.5 年) | 二級預防繼續升格 |
| ≥75 歲(去處方化) | 未提及 | COR 2b(B-R)(生命預期有限者可考慮停 statin) | 全新推薦;COR 為 2b,非 2a |
| HIV(PLHIV 40–75y) | 風險強化因子(無 COR) | COR 1(B-R):statin 推薦 | REPRIEVE(PMID 37486775) |
| 女性(生殖風險因子) | 2 項(Class IIb):子癲前症、早產 | 7–8 項(COR 2a):新增 PCOS、妊娠期糖尿病、早發停經 <45y、反覆流產;閾值從 <40y → <45y | CARDIA;Nurses' Health Study;AHA 2021 聲明 |
| FH(HeFH 無 ASCVD) | LDL-C <100 觸發 PCSK9i(Class IIb) | 目標 LDL-C <70 mg/dL(COR 1);基因檢測 COR 1;一般風險方程式 COR 3: Harm(禁用) | FOURIER/ODYSSEY;FH 流行病學研究 |
| MASLD(原 NAFLD) | 未明確提及 | 新增為風險強化因子;statin COR 2a;不需基線 LFT | 更名與文獻更新 |
| FCS(家族性乳糜血症) | 無特定藥物 | COR 1:olezarsen | BALANCE(PMID 38587247) |
3.5 監測與生物標誌物改變
| 項目 | 2018 | 2026 | COR/LOE | 符號 |
|---|---|---|---|---|
| LDL-C 計算方式 | Friedewald(Class IIa,限 LDL-C <70 或 TG ≥200 mg/dL 時用直接法) | Martin/Hopkins 或 Sampson 方程式(所有高風險患者) | COR 1, LOE B-NR | 📊 |
| 空腹 vs 非空腹 | 空腹推薦;非空腹可接受 | 非空腹適合大多數;空腹僅需 TG ≥400 mg/dL | COR 1, LOE B-NR | ✏️ |
| 後續監測頻率 | 每 3–12 個月 | 每 6–12 個月 | COR 1, LOE A | ✏️ 📊 |
| 重複 CAC 評估 | 未提及 | CAC=0 患者暫緩治療,3–7 年後重複 CAC 評估 | COR 2a, LOE B-NR | 🆕 |
| Lp(a) 篩查 | 選擇性(無 COR) | 所有成人至少一次 | COR 1, LOE B-NR | 🆕 📊 |
| ApoB 治療目標 | 風險強化因子(無目標值) | 按風險分層:<90(中等以下);<70(高/非 VHR 二級);<55 mg/dL(VHR/CAC ≥1000) | COR 2a, LOE B-NR | 🆕 |
| hsCRP 行動閾值 | Class IIb(可考慮) | COR 2a:邊界風險 + hsCRP ≥2 mg/L x 2 → 高強度 statin | COR 2a, LOE B-R | 📊 |
| Non-HDL-C 回報 | 選擇性 | 所有患者強制回報 | COR 1, LOE B-NR | ✏️ |
| 偶然 CT 發現的 CAC | 未提及 | COR 1:納入治療決策(含 AI 演算法) | COR 1, LOE B-NR | 🆕 |
| 藥物基因體學(SLCO1B1) | 未提及 | COR 2b:考慮用於 SAMS 風險分層 | COR 2b, LOE B-NR | 🆕 |
4. 證據與推薦交叉矩陣
| 關鍵試驗 | PMID | 影響的推薦變動 | 涉及章節 |
|---|---|---|---|
| PREVENT 方程式開發研究 | 37947085 | PCE → PREVENT(COR 1);種族移除;閾值重新校準;年齡擴大 30–79 歲 | 風險分層、特殊族群、生活方式 |
| CTT 2010 meta-analysis | 21067804 | LDL-C 數值目標恢復;「越低越好」原則;VHR <55 mg/dL 依據 | LDL 目標、所有藥物治療 |
| CTT 2012 meta-analysis | 22607822 | 低風險族群 statin 正當性;每 1 mmol/L 降低獲益量化 | 一級預防、LDL 目標 |
| CTT 肌肉症狀 meta-analysis | 36049498 | SAMS 多為 nocebo;rechallenge 策略依據 | SAMS 管理 |
| FOURIER(evolocumab) | 28304224 | PCSK9 mAb 在 VHR;HeFH COR 1 依據;Lp(a) 效應確立 | PCSK9 藥物、FH、LDL 目標 |
| FOURIER-OLE | 36031810 | PCSK9 mAb ≥8 年安全性確認;序貫規定廢除依據之一;費用聲明移除 | PCSK9 藥物、監測 |
| ODYSSEY OUTCOMES(alirocumab) | 30403574 | PCSK9 mAb 在 ACS 後;全因死亡獲益;Lp(a) 效應(25% CV 獲益源自 Lp(a) 降低) | PCSK9 藥物、Lp(a)、LDL 目標 |
| IMPROVE-IT(ezetimibe) | 26039521 | Ezetimibe 在 LDL-C ≥190 升格 COR 1;高風險亞組更大獲益 | 藥物治療(ezetimibe)、嚴重高膽固醇 |
| CLEAR Outcomes(bempedoic acid) | 36876740 | Bempedoic acid 全新加入(COR 1–2a);SAMS 管理 COR 1;一級預防亞組 30% RRR | 藥物治療(bempedoic)、SAMS、糖尿病 |
| ORION-10/11(inclisiran) | 32187462 | Inclisiran COR 2a(二線 PCSK9i);Q6M 給藥選項 | 藥物治療(inclisiran) |
| REDUCE-IT(icosapent ethyl) | 30415628 | IPE COR 2b;特定適應症:TG 150–499 + LDL-C <100 + statin | 藥物治療(TG)、糖尿病 |
| PROMINENT(pemafibrate,陰性) | 36342116 | Fibrates 不推薦更強確立;TG 降低未降 CV 事件;LDL-C/ApoB 降低優先原則 | 藥物治療(TG)、LDL 目標概念 |
| REPRIEVE(pitavastatin,HIV) | 37486775 | HIV PLHIV statin COR 1 | 特殊族群(HIV) |
| BALANCE(olezarsen,FCS) | 38587247 | Olezarsen COR 1 for FCS | 藥物治療(TG)、特殊族群(FCS) |
| CORONA(rosuvastatin,HFrEF,陰性) | 17984166 | HFrEF statin COR 3: No Benefit | 特殊族群(HF)、藥物治療 |
| GISSI-HF(rosuvastatin,HFrEF,陰性) | 18757089 | HFrEF statin COR 3: No Benefit | 特殊族群(HF)、藥物治療 |
| SHARP(simvastatin+ezetimibe,CKD) | 21663949 | CKD 非透析 COR 1;透析 COR 3: No Benefit | 特殊族群(CKD) |
| SAMSON(nocebo,SAMS) | 33196154 | Statin nocebo 確認(90% 症狀為安慰劑效應);「drucebo」概念;rechallenge 策略 | SAMS 管理 |
| EAS Lp(a) Consensus 2022 | 36036785 | Lp(a) 全體普篩 COR 1 的主要依據 | 生物標誌物(Lp(a))、風險分層 |
| FOURIER Lp(a) 子研究 | 30586750 | PCSK9 mAb 在高 Lp(a) ASCVD 患者 COR 1;Lp(a) 降低 CV 效益量化 | Lp(a)、藥物治療(PCSK9) |
| Martin/Hopkins 方程式驗證 | 24240933 | LDL-C 計算方式升格 COR 1(取代 Friedewald) | 監測、LDL 計算 |
| Ference BA MR 研究 | 23083789 | 早期介入終生獲益 3 倍;支持 30 年風險框架和 30–39 歲評估 | 風險分層、年輕族群 |
5. 臨床決策流程比較
5.1 二級預防(ASCVD)流程
2018 流程——嚴格序貫
已確診 ASCVD
├── 非極高風險(VHR)
│ ├── 年齡 ≤75:高強度 statin(Class I)
│ │ └── LDL-C ≥70 mg/dL → 可考慮 ezetimibe(Class IIb)
│ └── 年齡 >75:中或高強度 statin(Class IIa)
└── 極高風險(VHR)(≥2 大事件 或 1 事件+多項高風險條件)
└── 高強度 statin(Class I)
└── LDL-C ≥70 mg/dL → 加 ezetimibe(Class IIa)【必須先用!】
└── LDL-C 仍 ≥70 mg/dL → 加 PCSK9i(Class IIa)
(ezetimibe 必須在 PCSK9i 之前——Class I 強制規定)
2026 流程——目標導向,廢除強制序貫
已確診 ASCVD → 評估 VHR 標準(≥2 大事件,或 1 事件 + ≥2 高風險條件)
├── 極高風險(VHR)
│ └── 高強度或最大耐受 statin(COR 1, LOE A)
│ 目標:≥50% LDL-C 降幅 + LDL-C <55 mg/dL + Non-HDL-C <85 mg/dL
│ ↓ 若未達目標
│ 加 ezetimibe 和/或 PCSK9 mAb【無序貫要求】(COR 1, LOE A)
│ ↓ 若無法取得/耐受 PCSK9 mAb 或偏好每半年給藥
│ 加 inclisiran(COR 2a, LOE B-NR)
│ ↓ 若仍未達目標
│ 加 bempedoic acid(COR 2a, LOE B-R)
│
└── 非極高風險 ASCVD
└── 高強度 statin(COR 1, LOE A)
目標:≥50% 降幅 + LDL-C <70 mg/dL + Non-HDL-C <100 mg/dL
↓ 若未達目標
加 ezetimibe、PCSK9 mAb 或 bempedoic acid(COR 2a, LOE B-R)
可選:更積極目標 LDL-C <55 mg/dL(COR 2a)
5.2 一級預防流程
2018 流程(PCE 基礎)
成人 40–75 歲,無 ASCVD → 計算 PCE 10 年風險
├── 低風險(<5%):生活方式;無 statin
├── 邊界風險(5–7.5%):有風險強化因子可考慮 statin(Class IIb)
│ └── 不確定 → CAC(Class IIa,reasonable)
├── 中等風險(7.5–<20%):中強度 statin(Class I, LOE A)
│ └── 不確定 → CAC(Class IIa)
└── 高風險(≥20%):statin,LDL-C ≥50% 降幅(Class I)
2026 流程(PREVENT + CPR 框架)
成人 30–79 歲,無 ASCVD → 計算 PREVENT-ASCVD 10 年風險
CPR 框架:Calculate(計算)→ Personalize(個人化)→ Reclassify(重新分層)
├── 低風險(<3%):生活方式;通常不啟動 statin
│ 例外:LDL-C 160–189 mg/dL 或 30 年風險 ≥10%
│ → 考慮中強度 statin(COR 2a, LOE C-LD)
│
├── 邊界風險(3–<5%):
│ ├── 無強化因子 → 醫病共享決策(可不啟動)
│ ├── 有風險強化因子 → 中強度 statin(COR 2a)
│ └── hsCRP ≥2 mg/L(兩次確認)→ 高強度 statin(COR 2a, LOE B-R)
│
├── 中等風險(5–<10%):
│ ├── 至少中強度 statin(COR 1, LOE A)
│ │ 目標 LDL-C <100 mg/dL + Non-HDL-C <130 mg/dL
│ ├── 決策不確定 → CAC(COR 1,升格)
│ │ ├── CAC = 0 → 暫緩;3–7 年重新評估(COR 2a, B-NR)
│ │ ├── CAC 1–99 → 考慮 statin;目標 LDL-C <100
│ │ ├── CAC ≥100 → 推薦 statin;目標 LDL-C <70
│ │ └── CAC ≥1000 → 目標 LDL-C <55(等同 VHR 強度)
│ └── 偶然 CT 發現 CAC → COR 1 納入治療決策
│
└── 高風險(PREVENT ≥10%):
└── 高強度 statin(COR 1)
目標 LDL-C <70 mg/dL + Non-HDL-C <100 mg/dL(COR 2a)
↓ 若未達目標
加 ezetimibe(COR 2a);考慮 PCSK9 mAb
5.3 嚴重高膽固醇血症(LDL-C ≥190 mg/dL)流程
2018 流程
LDL-C ≥190 mg/dL → 排除繼發原因 → 高強度 statin(Class I)
├── LDL-C 仍 ≥100 或降幅 <50%
│ → 加 ezetimibe(Class IIa)
│ → 仍 ≥100 + HeFH:加 PCSK9i(Class IIb)
│ → 仍 ≥130(基線 ≥220):加 PCSK9i(Class IIb)
└── 無明確 LDL-C 終點目標
2026 流程(大幅升格,三層目標分級)
LDL-C ≥190 mg/dL + 排除繼發原因
【Sub-group 1】無 ASCVD + 無 HeFH + 無額外風險 + 無亞臨床硬化:
目標 LDL-C <100 mg/dL + Non-HDL-C <130 mg/dL
→ Max statin + ezetimibe + PCSK9 mAb + bempedoic acid(COR 1, LOE A)
【Sub-group 2】有 HeFH 或額外風險因子 或 CAC 亞臨床硬化:
目標 LDL-C <70 mg/dL + Non-HDL-C <100 mg/dL
→ Max statin + ezetimibe + PCSK9 mAb + bempedoic acid(COR 1, LOE A)
【Sub-group 3】有臨床 ASCVD:
目標 LDL-C <55 mg/dL + Non-HDL-C <85 mg/dL
→ Max statin + ezetimibe + PCSK9 mAb + bempedoic acid(COR 1, LOE A)
【HoFH 最難治型(LDL-C 仍 ≥100 on max)】:
→ 加 evinacumab(ANGPTL3 抑制劑,COR 2b, LOE B-R)
5.4 高三酸甘油酯血症流程
【共同原則(2026 新增強調)】:
所有 TG 升高患者,首先確保 LDL-C/ApoB 達標(COR 1)
【TG 150–499 mg/dL(ASCVD 高風險)】:
LDL-C 先達標後:
├── ASCVD(或 DM + ≥1 CVD 危險因素)+ TG 150–499 + LDL-C 41–100 on statin
│ + 年齡 ≥45y(ASCVD)或 ≥50y(DM):
│ → IPE 4g/天(COR 2b, LOE B-R)【謹慎;mineral oil 爭議】
└── 一般 TG 降低:fibrates 不推薦(PROMINENT 確認無 ASCVD 事件獲益)
【TG 500–999 mg/dL(胰臟炎風險)】:
→ Fibrates 或 omega-3(降 TG 以預防胰臟炎,非 ASCVD 預防)
【TG ≥1000 mg/dL(嚴重)】:
├── FCS(基因確認,LPL 缺失):olezarsen 80 mg/月(COR 1, BALANCE trial)
└── 非 FCS:fibrates + omega-3 + 極低脂飲食(<10–15% 熱量來自脂肪)
6. 關鍵解讀釐清案例
以下保留三個最具教育意義的案例,說明跨領域審查如何糾正或釐清指引解讀上的關鍵分歧。
案例 A:CAC 300–999 AU 的 ApoB 目標——兩層式結構釐清
爭議焦點: CAC 300–999 AU 對應的 ApoB 目標值在初稿中被誤列為單一的 <55 mg/dL,此與指引的兩層式目標結構不一致。
正確值: 2026 指引對 CAC 300–999 AU 採兩層式目標:
| 風險層級 | 標準目標 | 選擇性強化目標 |
|---|---|---|
| CAC 100–299 AU 或 ≥75th 百分位 | LDL-C <70, non-HDL-C <100, ApoB <70 mg/dL | — |
| CAC 300–999 AU | LDL-C <70, non-HDL-C <100, ApoB <70 mg/dL | LDL-C <55, non-HDL-C <85, ApoB <55 mg/dL(選擇性強化) |
| CAC ≥1000 AU(VHR 等同) | LDL-C <55, non-HDL-C <85, ApoB <55 mg/dL | — |
依據: 2026 指引 Figure 1 及 Section 4.2.7:CAC 300–999 AU 標準目標等同非 VHR 二級預防(LDL-C <70, ApoB <70 mg/dL),但可選擇性強化至 VHR 等級目標(LDL-C <55, ApoB <55 mg/dL)。ApoB <55 mg/dL 作為唯一目標僅適用 VHR ASCVD 或 CAC ≥1000 AU。
案例 B:HFrEF Statin 推薦——依 ASCVD 共病分層
爭議焦點: HFrEF statin 推薦在初稿中列為「Class IIb(維持不變)」,未正確反映 2026 指引依 ASCVD 狀態進行的分層處理。
正確值: 2026 指引對 HFrEF statin 區分 ASCVD 狀態:HFrEF 無 ASCVD:COR 3: No Benefit(LOE B-R)(非 Class IIb);HFrEF 合併缺血性病因/ASCVD——新啟動:COR 2b(B-R),繼續既有 statin:COR 1(A)。此分層反映 CORONA 和 GISSI-HF 兩大陰性試驗(合計 N = 9,642)的一致陰性結果。
案例 C:透析患者——啟動 vs 繼續的區分
爭議焦點: 透析患者 statin 推薦在初稿中未區分「新啟動」與「轉入透析前已在使用者繼續」,導致 COR 描述混淆。
正確值: 新啟動:COR 3: No Benefit(B-R)——不推薦透析患者常規啟動 statin 一級預防(SHARP 透析亞組、4D、AURORA 均陰性);轉入透析者繼續既有 statin:COR 2b(C-LD)——"it may be reasonable to continue statin therapy"。此區分的臨床意義在於避免對所有透析患者一律停藥。
7. 今天該改變臨床實務的推薦 vs 仍屬未來方向
立即可行動(Tier 1 + Tier 2:指引明文 + RCT 支持)
- VHR ASCVD 目標 <55 mg/dL
- 廢除 ezetimibe-first 序貫
- HIV 患者 pitavastatin COR 1
- Lp(a) 全體成人篩查一次
- HFrEF 無 ASCVD 不啟動 statin
- Bempedoic acid 用於 statin 不耐受
- CKD 非透析 statin COR 1
- 改用 PREVENT-ASCVD 方程式
- 改用 Martin/Hopkins 計算 LDL-C
- 膳食補充劑無效(COR 3: No Benefit)
建議行動但部分證據為觀察性外推(Tier 1 + Tier 3)
- CAC 分層 LDL-C 數值目標(CAC ≥1000 → <55 mg/dL)
- 高齡者生命預期閾值(<2.5 年避免啟動;<1 年去處方化)
- 生殖風險標誌擴大至 7 項
- 30–39 歲早期介入(Mendelian randomization 支持)
仍屬未來方向,現階段不可行動(Tier 4)
- Lp(a) 特異性降脂藥物(pelacarsen/olpasiran/lepodisiran — 第三期試驗進行中)
- Inclisiran 的 CV 結局數據(ORION-4 待報告)
- AI/數位健康(指引承認但無 COR)
8. 證據缺口與未來研究方向
(a) 已納入 2026 指引的關鍵證據(供參考,非缺口)
以下試驗的結果已被 2026 指引充分納入並形成推薦:FOURIER、ODYSSEY OUTCOMES、CLEAR Outcomes、REDUCE-IT、REPRIEVE、BALANCE、CORONA、GISSI-HF、SHARP、IMPROVE-IT、SAMSON、ORION-10/11。完整分析見第 4 節(證據矩陣)及 04_evidence_key_trials.md。
(b) 指引發布後新出爐、但尚未納入 2026 指引的重要新證據
1. VESALIUS-CV(evolocumab 用於高風險一級預防)
- 狀態:已報告但未納入 2026 指引(結果於 2025 年底發表,2026 指引撰寫截止日前後)
- 試驗概述:N = 13,000+,evolocumab vs 安慰劑用於高心血管風險但無既往 MI/中風的一級預防患者
- 主要結果:3-point MACE RRR 25%;4-point MACE RRR 19%
- 意義:這是首個 PCSK9 mAb 在高風險一級預防族群中的正式 CVOT 陽性結果。2026 指引在撰寫時 VESALIUS-CV 結果尚不確定,因此 PCSK9 mAb 用於一級預防的推薦仍相對保守。未來指引更新可能據此進一步擴大 PCSK9 mAb 在一級預防中的適應症和 COR 等級
- 臨床啟示:對於高風險一級預防患者(高 LDL-C、高 PREVENT 風險、高 Lp(a)),VESALIUS-CV 結果支持更積極地考慮 PCSK9 mAb,但需等待正式指引更新以獲得明確 COR
(c) 真正仍未完成的試驗與知識缺口
高優先度缺口(關鍵試驗進行中)
1. Lp(a) 特異性療法的 CV 事件降低效益
- 缺口:無完成的 Lp(a) 特異性療法 CVOT
- 問題:降低 Lp(a) 本身是否降低 ASCVD 事件?最佳治療閾值?
- 預期試驗:Lp(a) HORIZON(pelacarsen, N = 8,323)→ H1 2026;OCEAN(a)-OUTCOMES(olpasiran, N = 7,297)→ 2026–2027
2. Inclisiran 的 CVOT 數據
- 缺口:ORION-4 及 VICTORION-2P 尚未完成(截至 2026 年 3 月)
- 問題:Inclisiran 的 MACE 降低效益是否等同 PCSK9 mAb?
- 預期:ORION-4 → 2026;VICTORION-2P → 2027
3. PCSK9 mAb 在一級預防的更廣泛適應症
- 缺口:雖然 VESALIUS-CV 已報告陽性結果(見 (b) 節),但尚未被正式指引納入
- 問題:哪些一級預防亞族群(高 LDL、高 Lp(a)、高 CAC)獲益最大?
- 預期:VICTORION-1 PREVENT(inclisiran)招募中
臨床重要但缺乏 RCT 的缺口
4. CAC 分層 LDL-C 目標的事件降低依據
- CAC ≥1000 → LDL-C <55 mg/dL 為觀察性外推(LOE B-NR),無 RCT 以 CAC 分層目標作為設計特徵
5. ApoB 作為主要治療目標的 RCT 驗證
- 無 RCT 比較「ApoB 導向」vs「LDL-C 導向」策略;ApoB 目標推薦(COR 2a)為外推
6. 年輕成人(30–39 歲)早期 statin 的長期 RCT
- Mendelian randomization 支持早期介入效益 3 倍,但無 RCT 直接驗證 30 多歲啟動的硬終點
7. 生殖風險因子作為 LLT 啟動觸發點的 RCT
- 無 RCT 測試「子癲前症後啟動 statin」是否降低 ASCVD 事件
8. Icosapent Ethyl 的「真實」CV 獲益
- 礦物油安慰劑爭議未解;STRENGTH(omega-3 carboxylic acid vs 玉米油)陰性
新興及方法論缺口
9. 多基因風險評分(PRS)的臨床應用框架
- 僅列為「未來可能工具」(無 COR);缺乏多元族群驗證
10. 跨性別者的脂質風險
- 性別確認激素療法對脂質代謝和 ASCVD 風險的影響,研究極為有限;2026 指引明確指出此為知識缺口
11. PREVENT-ASCVD 在非美國人群的外部驗證
- 基於美國 EHR 數據;亞洲、歐洲、非洲人群的校準準確性未知
12. 透析患者的最佳降脂策略
- 雖然 4D、AURORA 和 SHARP 透析亞組均陰性,但透析族群是否有其他降脂途徑仍未確立
9. 附錄:完整關鍵試驗參考文獻
風險評估
- Khan SS, Matsushita K, Sang Y, et al. Development and validation of the American Heart Association's PREVENT equations. Circulation 2024;149:430–449. PMID: 37947085
- Ference BA, Yoo W, Alesh I, et al. Effect of long-term exposure to lower LDL-C beginning early in life on risk of CHD. J Am Coll Cardiol 2012;60:2631–2639. PMID: 23083789
- Ference BA, Ray KK, Catapano AL, et al. Mendelian randomization study of ACLY and cardiovascular disease. N Engl J Med 2019;380:1033–1042. PMID: 30865797
Statin 療效(CTT)
- Baigent C, Blackwell L, Emberson J, et al. (CTT). Efficacy and safety of more intensive lowering of LDL cholesterol: 26 trials, 170,000 participants. Lancet 2010;376:1670–1681. PMID: 21067804
- Mihaylova B, Emberson J, Blackwell L, et al. (CTT). Effects of lowering LDL cholesterol with statin therapy in low-risk individuals: 27 trials. Lancet 2012;380:581–590. PMID: 22607822
- Cholesterol Treatment Trialists Collaboration. Effect of statin therapy on muscle symptoms. Lancet 2022;400:832–845. PMID: 36049498
LDL-C 計算方式
- Martin SS, Blaha MJ, Elshazly MB, et al. Comparison of a novel method vs the Friedewald equation for estimating LDL cholesterol levels. JAMA 2013;310:2061–2068. PMID: 24240933
- Sampson M, Ling C, Sun Q, et al. A new equation for the calculation of low-density lipoprotein cholesterol. JAMA Cardiology 2020;5:540–548. PMID: 32101259
Ezetimibe
- Cannon CP, Blazing MA, Giugliano RP, et al. (IMPROVE-IT). Ezetimibe added to statin therapy after acute coronary syndromes. N Engl J Med 2015;372:2387–2397. PMID: 26039521
PCSK9 抑制劑
- Sabatine MS, Giugliano RP, Keech AC, et al. (FOURIER). Evolocumab and clinical outcomes in patients with cardiovascular disease. N Engl J Med 2017;376:1713–1722. PMID: 28304224
- Schwartz GG, Steg PG, Szarek M, et al. (ODYSSEY OUTCOMES). Alirocumab and cardiovascular outcomes after acute coronary syndrome. N Engl J Med 2018;379:2097–2107. PMID: 30403574
- O'Donoghue ML, Giugliano RP, Wiviott SD, et al. (FOURIER-OLE). Long-term evolocumab in patients with established ASCVD. Circulation 2022;146:1109–1119. PMID: 36031810
Lp(a) 與 PCSK9 mAb
- O'Donoghue ML, Fazio S, Giugliano RP, et al. Lipoprotein(a), PCSK9 inhibition, and cardiovascular risk. Circulation 2019;139:1483–1492. PMID: 30586750
- Bittner VA, Szarek M, Aylward PE, et al. Effect of alirocumab on lipoprotein(a) and cardiovascular risk after ACS. J Am Coll Cardiol 2020;75:133–144. PMID: 31948641
- Kronenberg F, Mora S, Stroes ESG, et al. Lipoprotein(a) in ASCVD and aortic stenosis: EAS consensus statement. Eur Heart J 2022;43:3925–3946. PMID: 36036785
Bempedoic Acid
- Nissen SE, Lincoff AM, Brennan D, et al. (CLEAR Outcomes). Bempedoic acid and cardiovascular outcomes in statin-intolerant patients. N Engl J Med 2023;388:1353–1364. PMID: 36876740
- Nissen SE, Menon V, Nicholls SJ, et al. Bempedoic acid for primary prevention in statin-intolerant patients. JAMA 2023;330:131–140. PMID: 37354546
Inclisiran
- Ray KK, Wright RS, Kallend D, et al. (ORION-10 and ORION-11). Two phase 3 trials of inclisiran in patients with elevated LDL cholesterol. N Engl J Med 2020;382:1507–1519. PMID: 32187462
Icosapent Ethyl
- Bhatt DL, Steg PG, Miller M, et al. (REDUCE-IT). Cardiovascular risk reduction with icosapent ethyl for hypertriglyceridemia. N Engl J Med 2019;380:11–22. PMID: 30415628
Fibrates(陰性試驗)
- Das Pradhan A, Glynn RJ, Fruchart JC, et al. (PROMINENT). Triglyceride lowering with pemafibrate to reduce cardiovascular risk. N Engl J Med 2022;387:1923–1934. PMID: 36342116
Olezarsen(FCS)
- Stroes ESG, Alexander VJ, Karwatowska-Prokopczuk E, et al. (BALANCE). Olezarsen, acute pancreatitis, and familial chylomicronemia syndrome. N Engl J Med 2024;390:1452–1462. PMID: 38587247
Statin 肌肉症狀(Nocebo)
- Wood FA, Howard JP, Finegold JA, et al. (SAMSON). N-of-1 trial of a statin, placebo, or no treatment to assess side effects. N Engl J Med 2020;383:2182–2184. PMID: 33196154
HIV
- Grinspoon SK, Fitch KV, Zanni MV, et al. (REPRIEVE). Pitavastatin to prevent cardiovascular disease in HIV infection. N Engl J Med 2023;389:687–699. PMID: 37486775
心臟衰竭(陰性試驗)
- Kjekshus J, Apetrei E, Barrios V, et al. (CORONA). Rosuvastatin in older patients with systolic heart failure. N Engl J Med 2007;357:2248–2261. PMID: 17984166
- Tavazzi L, Maggioni AP, Marchioli R, et al. (GISSI-HF). Effect of rosuvastatin in patients with chronic heart failure. Lancet 2008;372:1231–1239. PMID: 18757089
慢性腎臟病
- Baigent C, Landray MJ, Reith C, et al. (SHARP). The effects of lowering LDL cholesterol with simvastatin plus ezetimibe in patients with chronic kidney disease. Lancet 2011;377:2181–2192. PMID: 21663949
心血管結構性研究
- Kronenberg F et al. Mendelian randomization studies confirming causal role of Lp(a) in ASCVD. See EAS 2022 Consensus (PMID: 36036785) for systematic review.
