從自動化到智能化:一場人工胰臟的典範轉移
神經網路人工胰臟 (NAP) 的技術深度解析、臨床實證與戰略未來
說明: 核心主題:自動化胰島素輸送(AID)技術正在經歷一場重大的演進。維吉尼亞大學(UVA)開發的神經網路人工胰臟(NAP)不僅是一個新演算法,更代表了技術從「基於規則的自動化」向「基於數據驅動的智能化」跨越 。背景的神經元連結圖示象徵著人工神經網路(ANN)在模擬生物胰臟功能中的核心地位,即透過學習複雜的非線性模式來實現更精準的血糖控制。
現代奇蹟下的隱形天花板
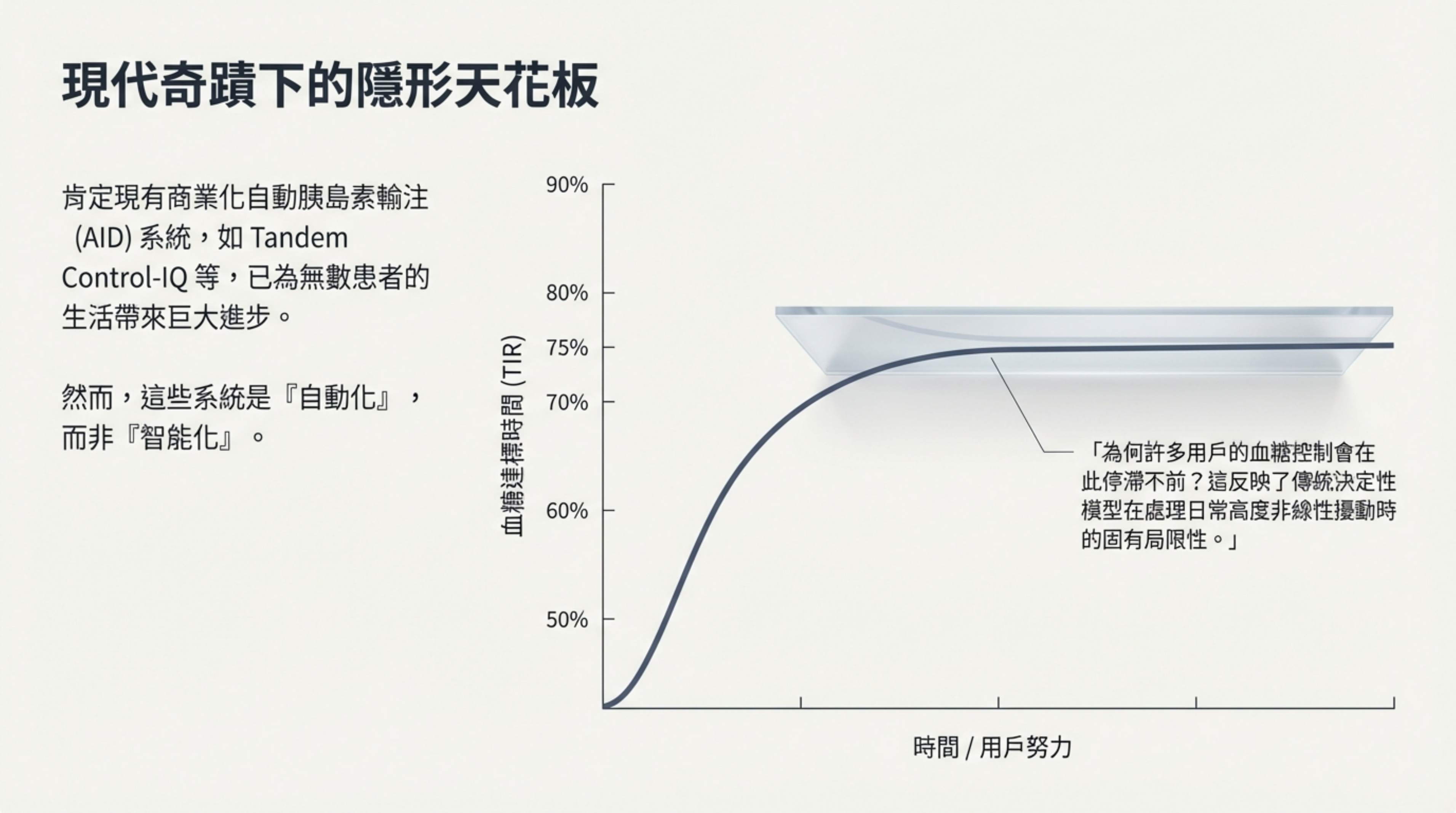
視覺內容: 一個血糖達標時間(TIR)隨時間/努力提升的曲線圖,但在 75% 處碰觸到一塊隱形的玻璃天花板。
說明: 目前的商業化 AID 系統(如 Tandem Control-IQ)雖然極大改善了患者生活,但它們主要依賴決定性控制模型 。
現狀瓶頸: 即便使用混合閉環(HCL)系統,許多用戶的血糖控制(TIR)往往卡在 70% 至 75% 之間,難以突破 。
原因分析: 這些系統被稱為「自動化」而非真正的「智能化(AI)」。傳統模型在面對日常生活中高度非線性且不可預測的擾動(如未告知的零食、壓力或激素波動)時,受限於預設的數學結構,無法像真正的人類大腦那樣靈活適應 。
當前 AID 系統的演算法核心
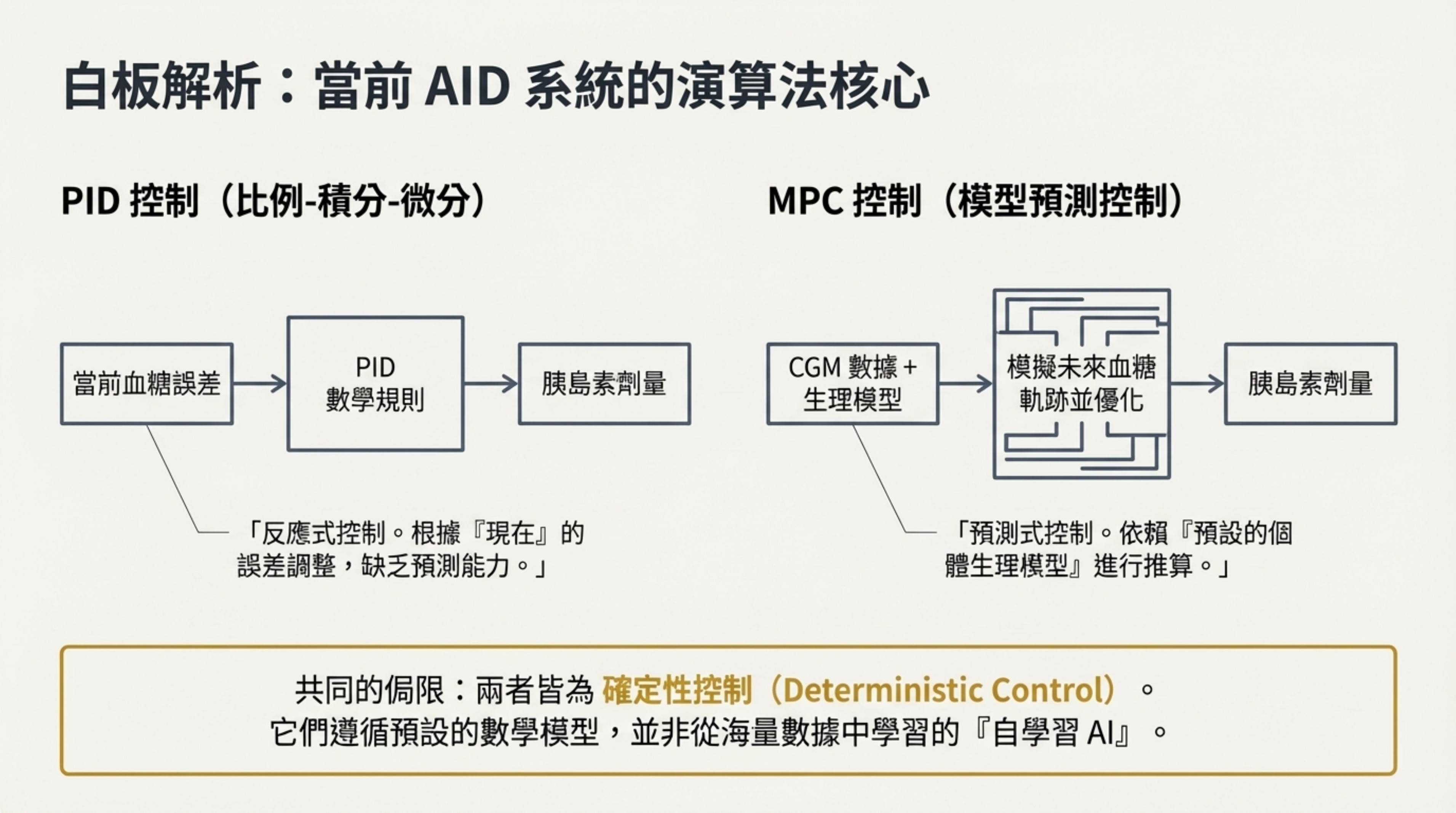
視覺內容: 左右對比 PID 控制與 MPC 控制的流程圖。
說明: 此頁深入探討現有技術的局限性:
-
PID 控制(比例-積分-微分): 屬於「反應式控制」。它根據「現在」的血糖誤差進行調整,缺乏對未來的預測能力,僅依照預設數學規則運作 。
-
MPC 控制(模型預測控制): 屬於「預測式控制」。雖然比 PID 進步,能模擬未來軌跡,但它依賴於「預設的個體生理模型」 。
-
共同侷限: 兩者皆為確定性控制(Deterministic Control)。它們需要根據個體的總日胰島素劑量(TDD)或碳水化合物比率(CF)進行參數化,並非真正從海量數據中自我學習的 AI 。
核心瓶頸:受困於個人歷史的數據孤島
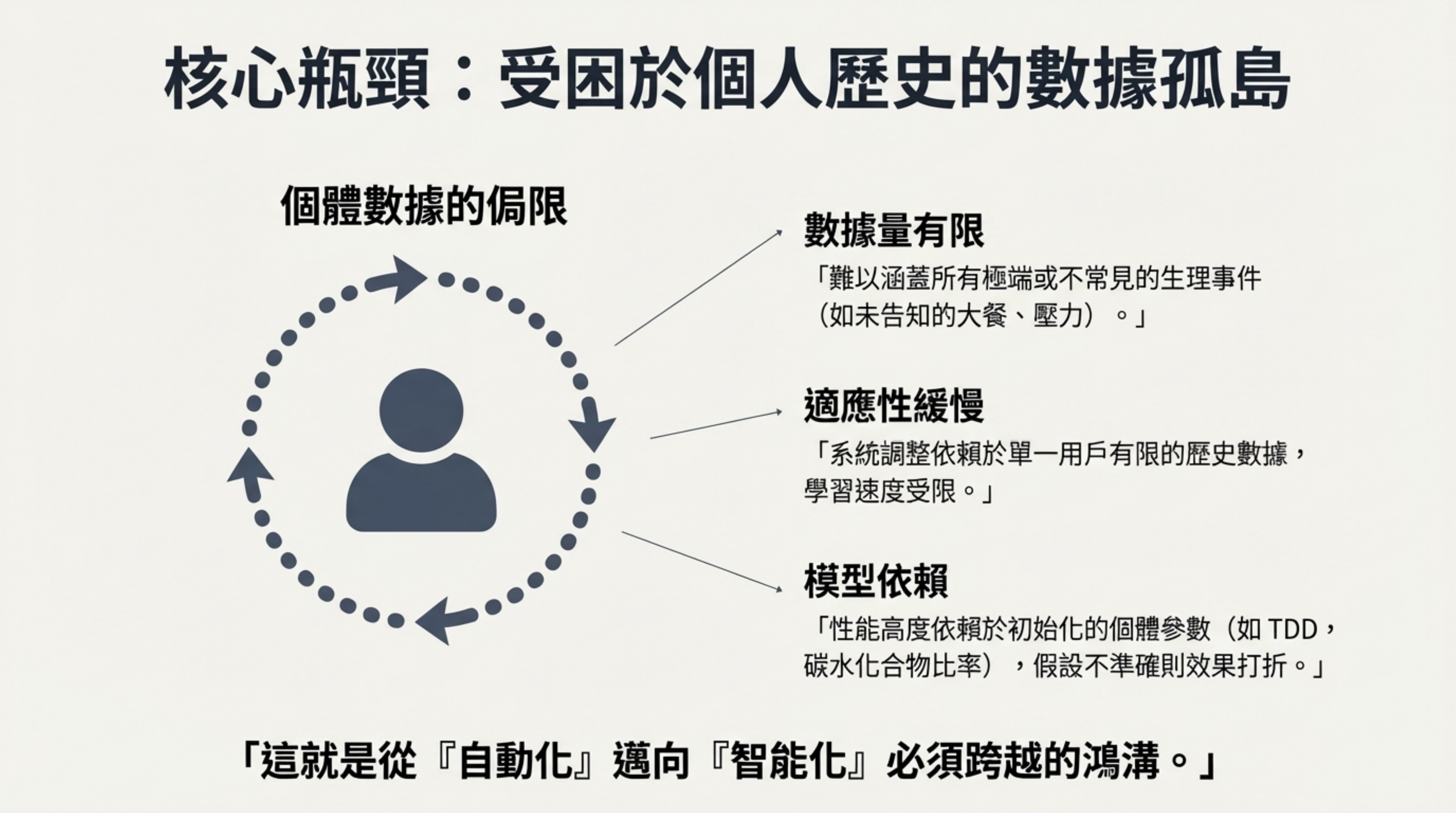
視覺內容: 一個人被困在自我數據的循環中,標示出數據量有限、適應性緩慢等問題。
說明: 傳統系統的設計哲學是基於單一個體的生理參數:
數據量有限: 單一患者的歷史數據難以涵蓋所有極端或不常見的生理事件(如偶發的暴飲暴食),導致模型在面對新情況時魯棒性不足 。
適應性緩慢: 系統調整依賴於單一用戶有限的歷史反饋 。
模型依賴: 性能高度依賴於初始化參數(如 TDD)的準確性,若假設不準,效果即打折 。這就是阻礙系統從單純「自動化」邁向真正「智能化」的鴻溝。
典範轉移:從個人歷史到群體智慧
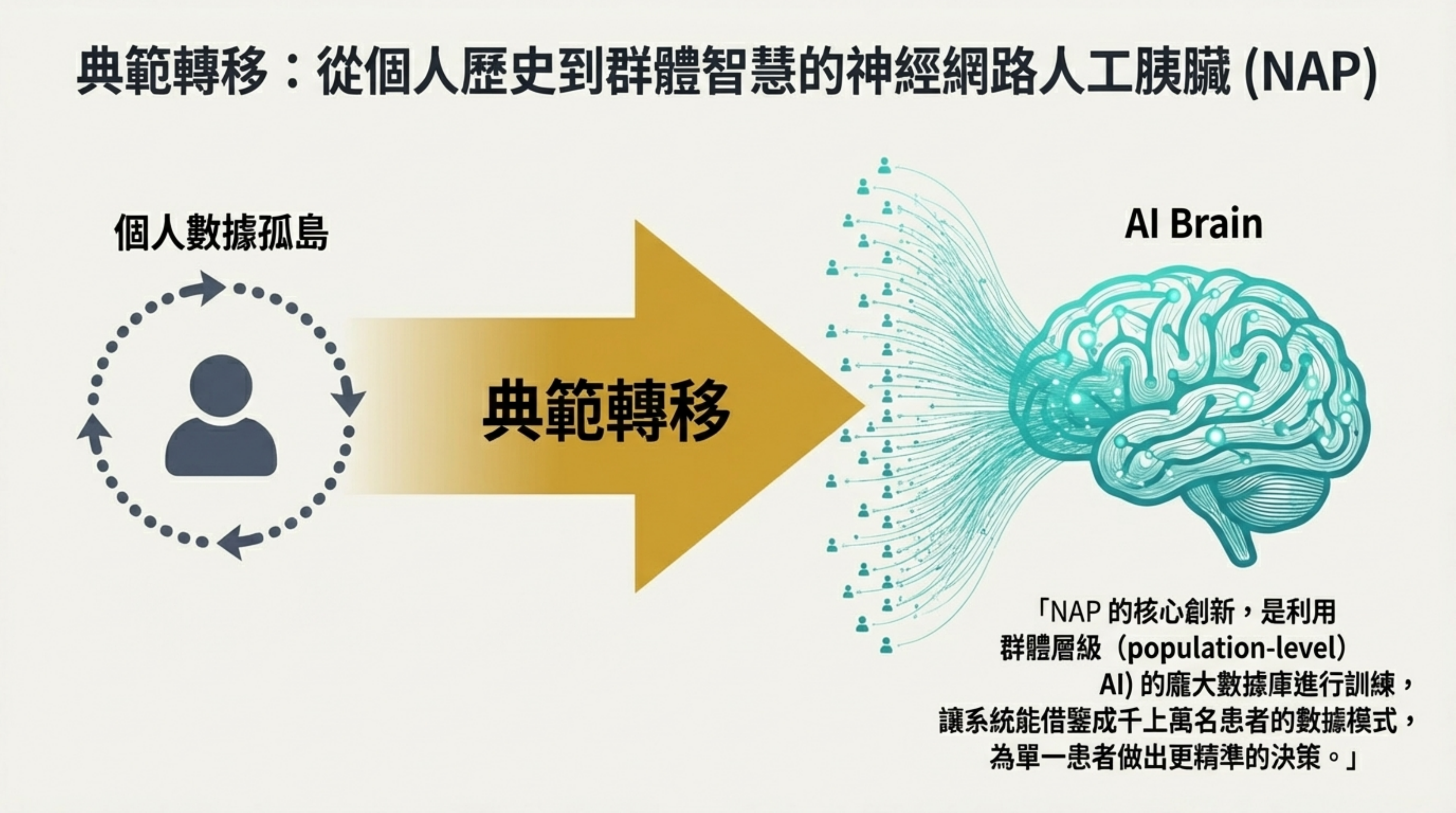
視覺內容: 左側是個人數據孤島,右側是一個由無數人臉組成的發光大腦(AI Brain),中間是一個巨大的轉變箭頭。
詳細說明: NAP 帶來了根本性的典範轉移:
群體智慧: NAP 不再依賴對個體生理學的參數化假設,而是利用人工神經網路(ANN)從大規模群體數據中學習 。
非參數化模式識別: 系統利用數千名用戶的歷史記錄訓練決策模型,捕捉廣泛的胰島素反應曲線。這使得 NAP 即使面對單一患者未曾遇過的極端狀況,也能借鑑群體經驗做出穩健決策 。這標誌著從「基於假設」過渡到「基於大數據經驗」的時代 。
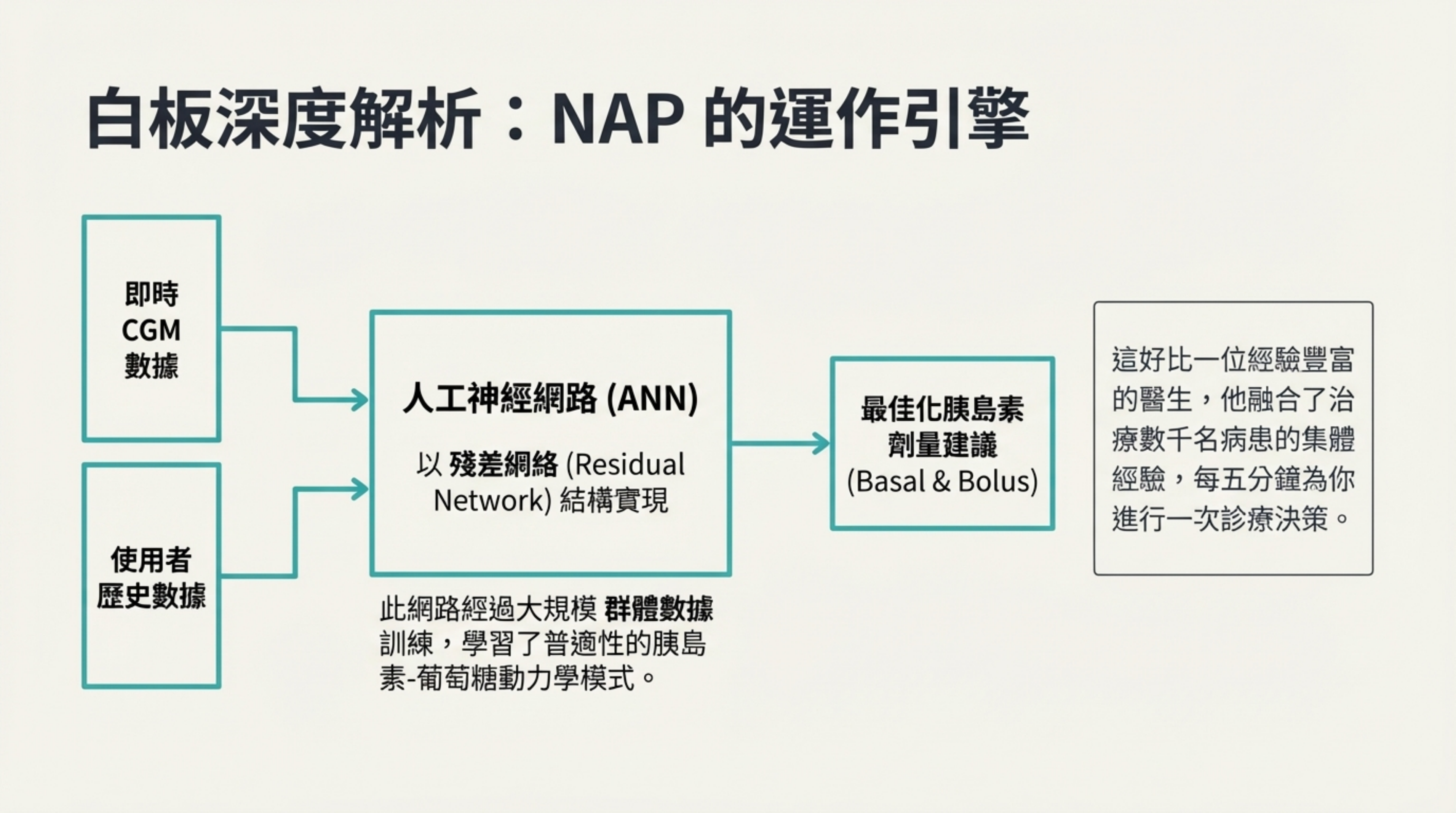
NAP 的運作引擎
視覺內容: 顯示即時 CGM 數據與歷史數據輸入到 ANN(殘差網絡結構),最後輸出最佳化胰島素劑量的流程。
詳細說明: NAP 的技術精髓在於其神經網路架構:
輸入與處理: 結合即時 CGM 數據與使用者歷史,輸入到深度神經網路中 。
殘差網絡(ResNet): 採用這種結構來實現高效的運算。
5 分鐘醫生: 投影片將其比喻為一位「融合了數千名病患治療經驗的醫生」,每五分鐘為患者進行一次診療決策,預測未來的血糖波動並給出基礎(Basal)與餐食(Bolus)胰島素建議 。
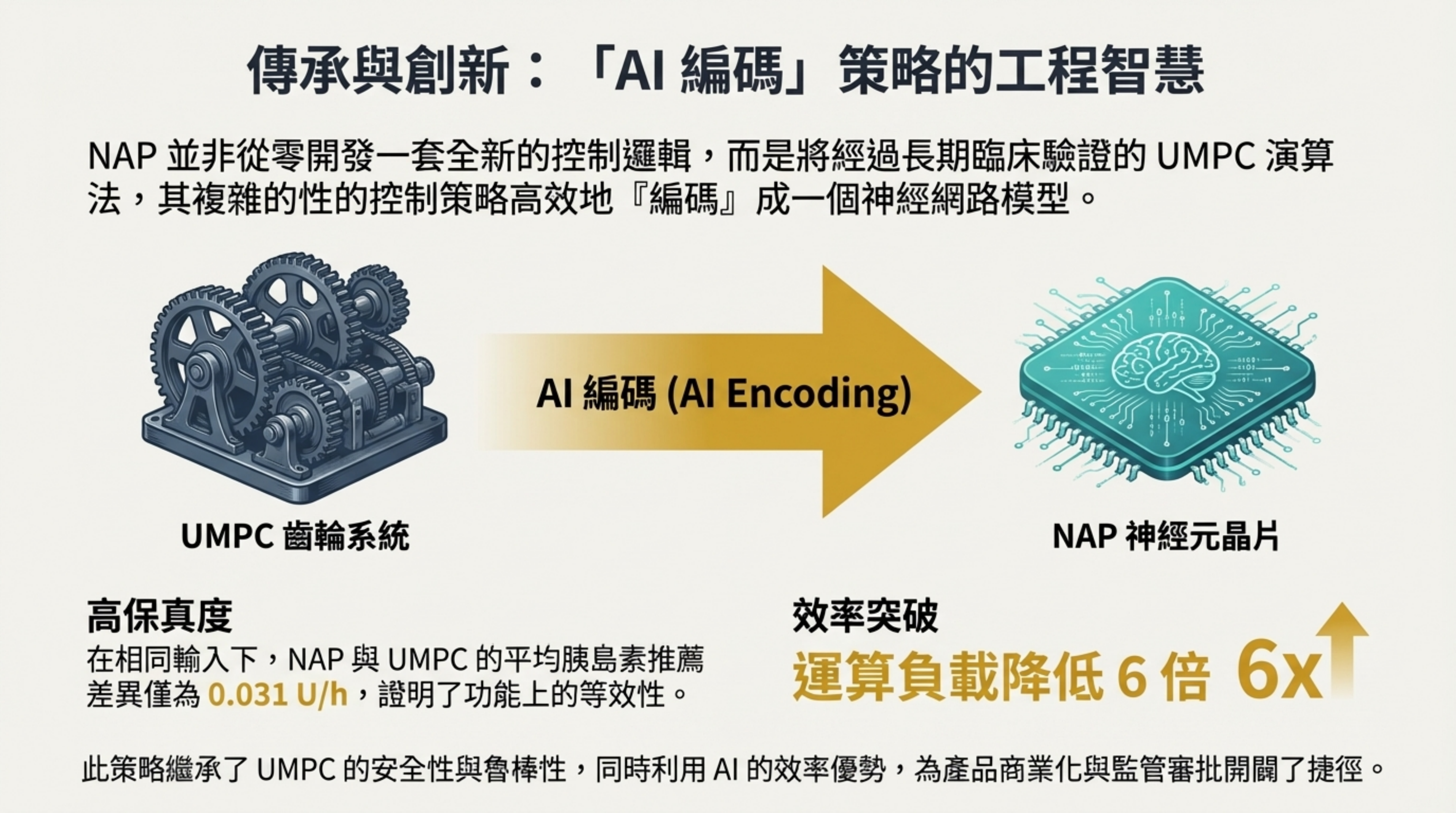
傳承與創新:「AI 編碼」策略的工程智慧
視覺內容: 左側是複雜的 UMPC 齒輪系統,經過「AI 編碼」箭頭,變成了右側的 NAP 神經元晶片。強調「運算負載降低 6 倍」。
詳細說明: 這是一個極具戰略意義的技術路線:
AI 編碼(AI Encoding): NAP 並非從零創造控制邏輯,而是將經過長期臨床驗證、計算複雜的 UMPC 演算法「編碼」進神經網路模型中 。
高保真度: 在相同輸入下,NAP 與 UMPC 的推薦差異僅為 0.031 U/h,證明了功能上的等效性 。
效率突破: 最關鍵的成就是將運算需求降低了 6 倍 。這既繼承了傳統模型的安全性,又獲得了 AI 的極致效率,加速了商業化與監管審批 。
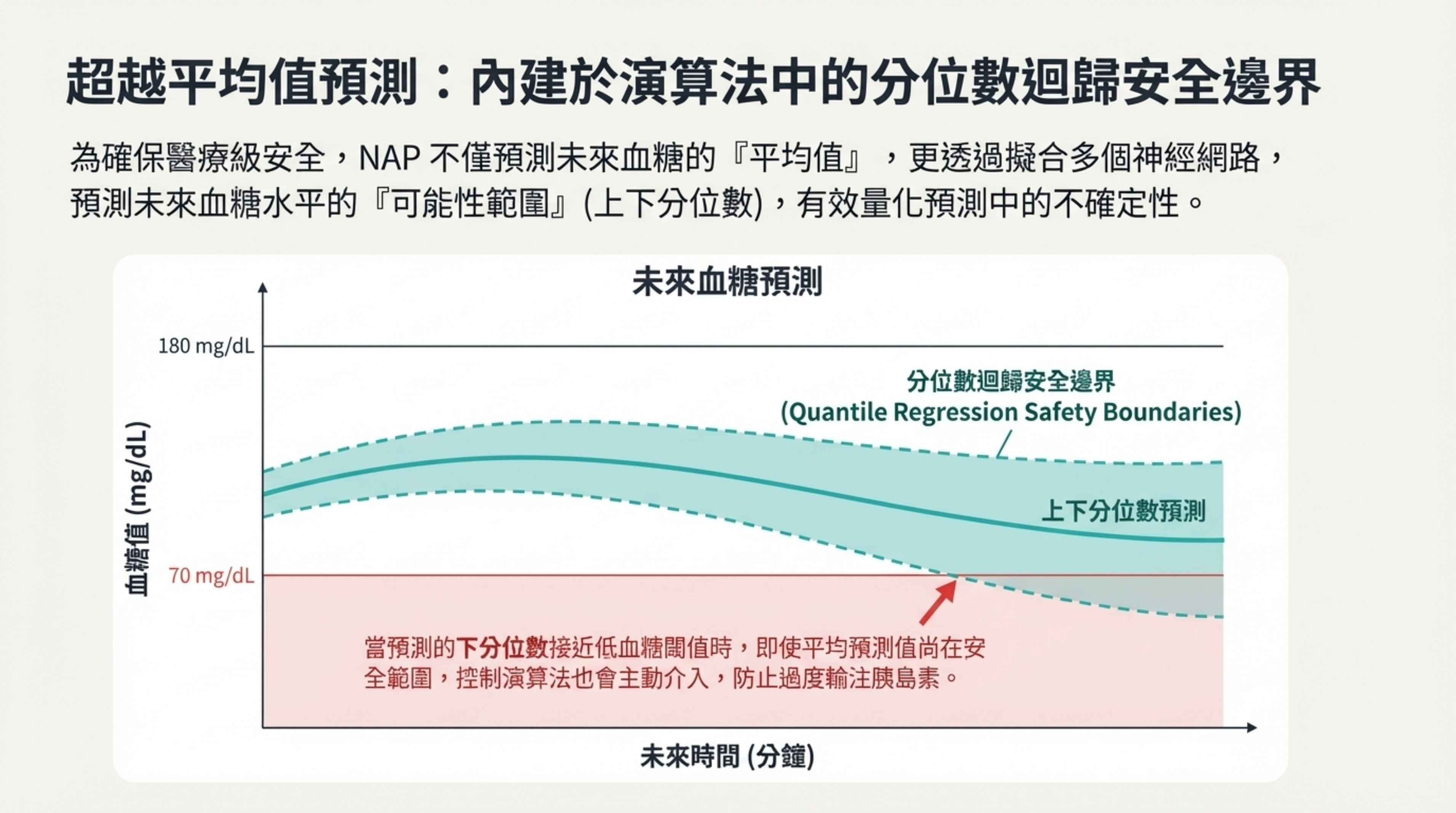
超越平均值預測:內建於演算法中的分位數迴歸安全邊界
視覺內容: 血糖預測曲線圖,顯示除了中間的平均預測線外,還有上下分位數的陰影範圍(安全邊界)。
詳細說明: 為了符合醫療級安全標準,NAP 採用了**分位數迴歸(Quantile Regression)
技術:
量化不確定性: 模型不僅預測未來血糖的「平均值」,還擬合神經網路來預測「可能性範圍」(上下分位數)
主動介入: 當預測的下分位數接近低血糖閾值(70 mg/dL)時,即使平均預測值尚在安全範圍,控制演算法也會強制介入,減少胰島素輸注 。這是保障 AI 決策安全性的核心機制。
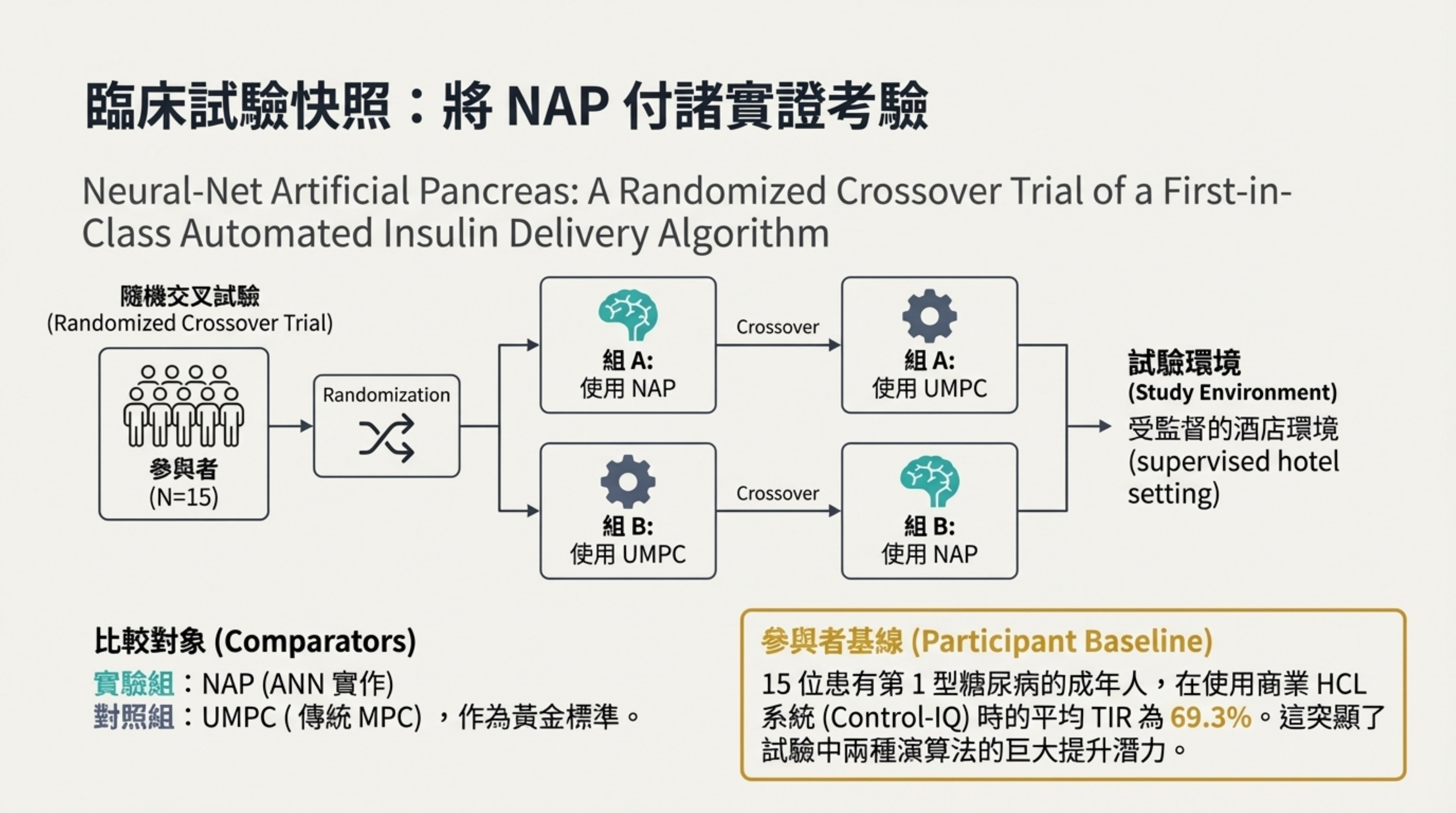
臨床試驗快照:將 NAP 付諸實證考驗
視覺內容: 隨機交叉試驗(Randomized Crossover Trial)的流程圖。N=15,分為 NAP 組與 UMPC 組進行交叉比對。
詳細說明: 這是 NAP 概念驗證的關鍵臨床試驗:
設計: 針對 15 位第 1 型糖尿病成年人進行的隨機交叉試驗 。
比較對象: 實驗組為 NAP(ANN 實作),對照組為被視為黃金標準的 UMPC(傳統 MPC) 。
基線數據: 參與者在使用商業 HCL 系統(Control-IQ)時的基線 TIR 為 69.33%,這為新演算法提供了改進空間的參考 。
環境: 在受監督的酒店環境中進行 。
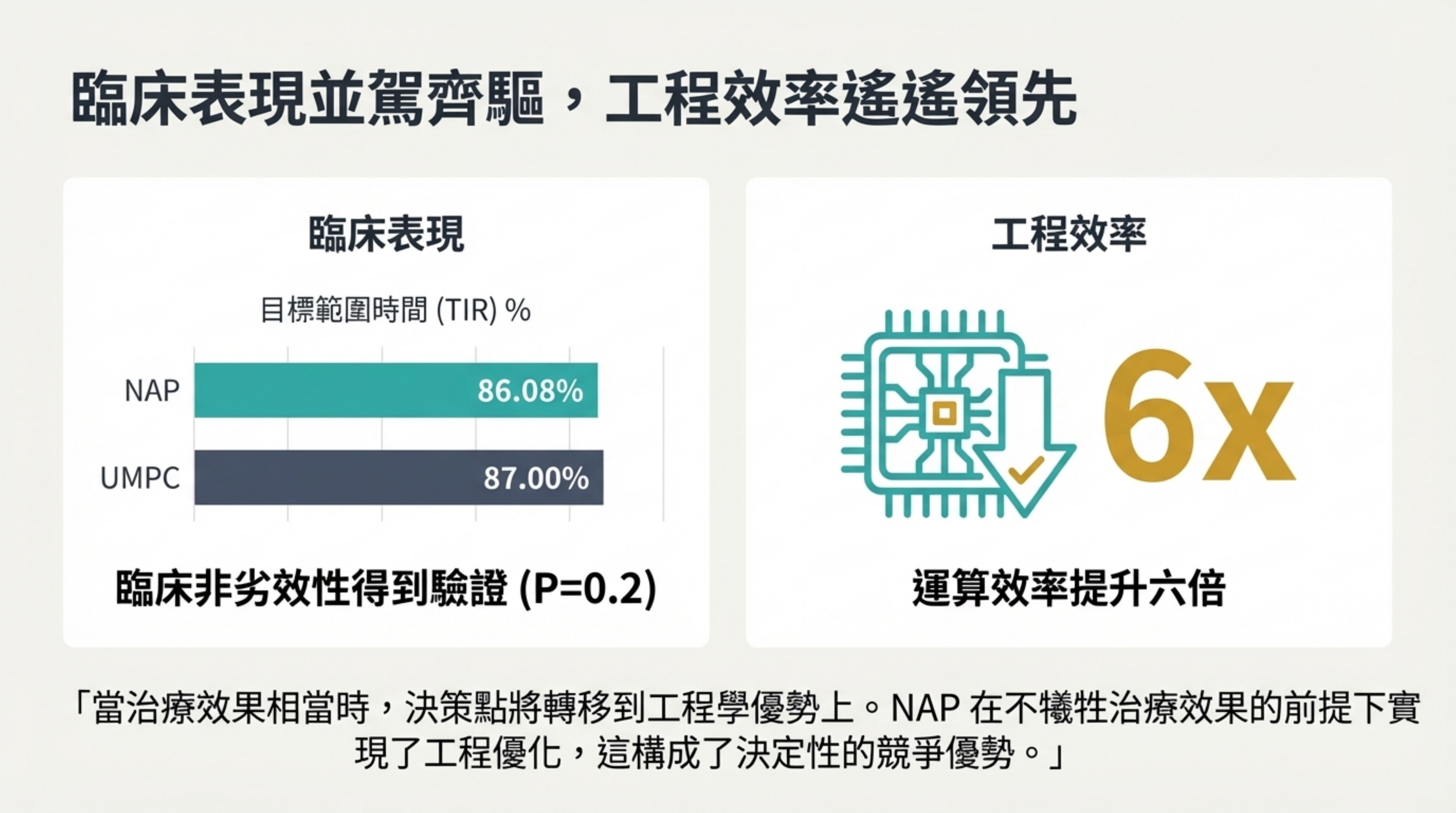
臨床表現並駕齊驅,工程效率遙遙領先
視覺內容: 左側長條圖顯示 TIR 數據(NAP 86.08% vs UMPC 87.00%),右側顯示晶片圖示強調 6 倍效率。
詳細說明: 這是本研究最重要的結論之一:
非劣效性驗證: NAP 的 TIR 達到 86.08%,與 UMPC 的 87.00% 相比,統計學上無顯著差異(P=0.2) 。
戰略意義: 當兩種療法的治療效果相當(臨床表現並駕齊驅)時,決策點就會轉移到工程優勢上。NAP 在不犧牲療效的前提下,實現了 6 倍 的運算效率提升 。這構成了產品從實驗室走向商業化設備(如貼片泵)的決定性競爭優勢。
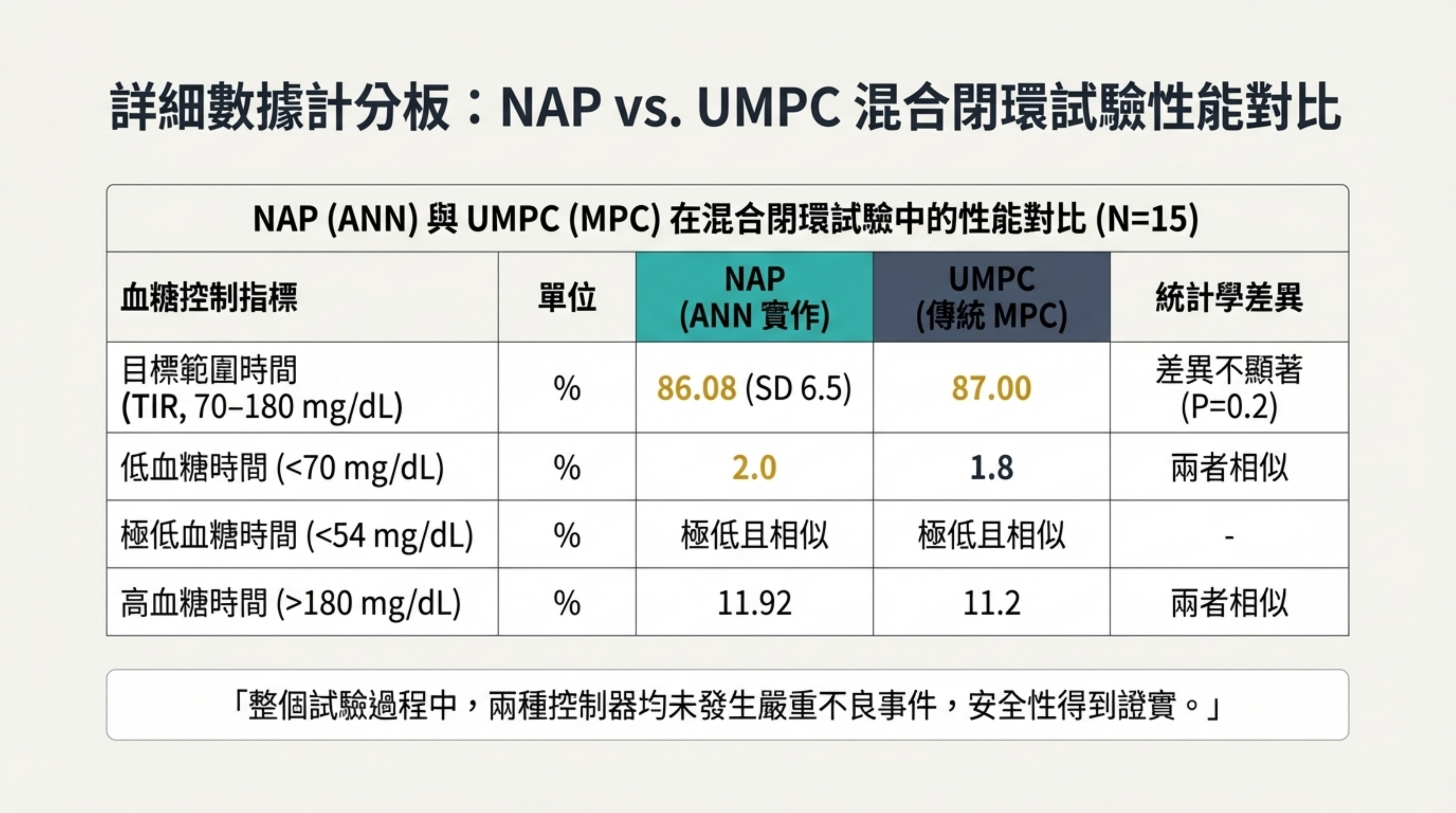
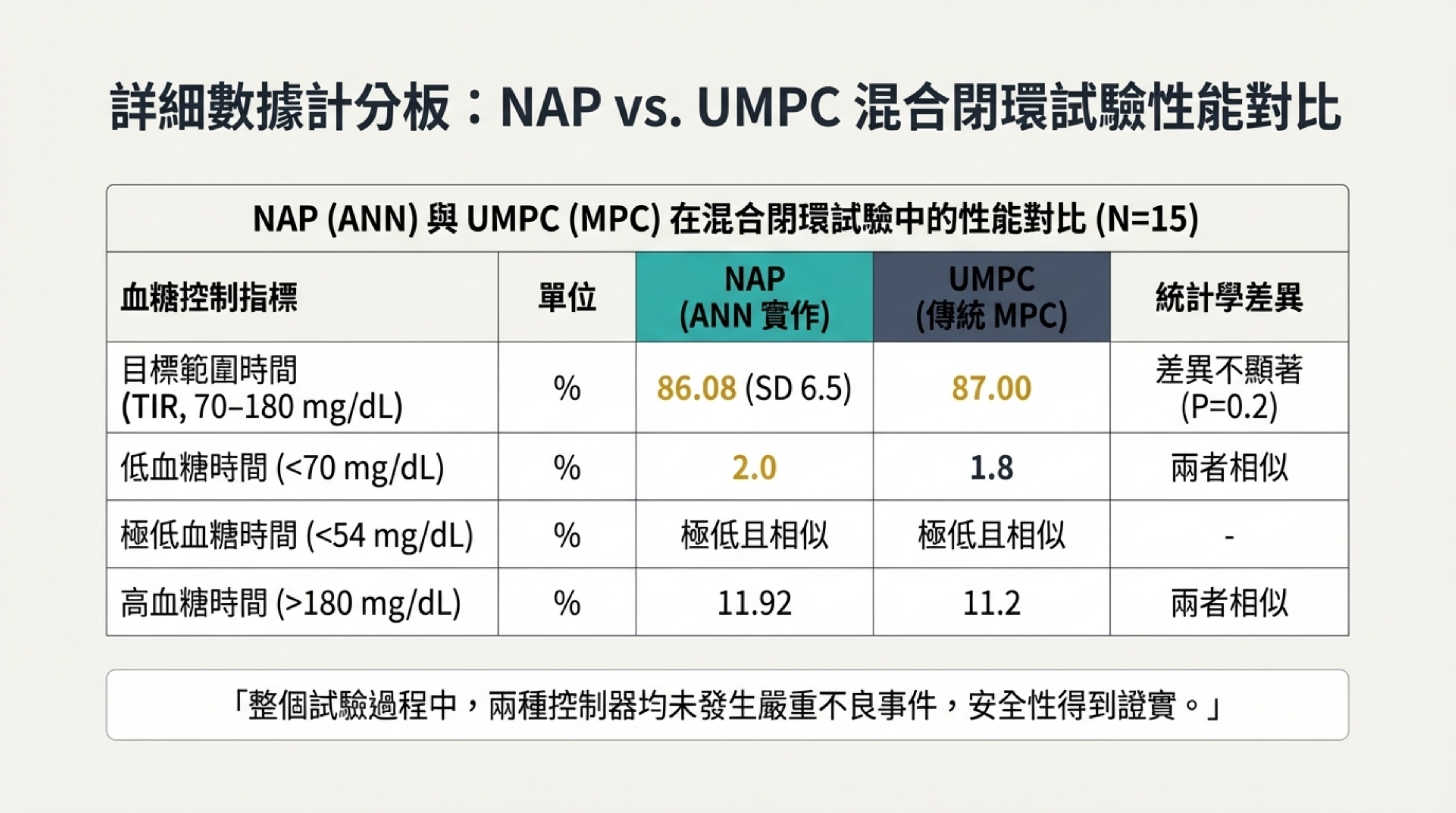
詳細數據計分板:NAP vs. UMPC 混合閉環試驗性能對比
視覺內容: 詳細的數據表格,列出 TIR、低血糖時間、極低血糖時間等指標。
詳細說明: 詳細數據進一步證實了 NAP 的安全性與有效性:
TIR: NAP (86.08%) vs UMPC (87.00%),差異不顯著 。
低血糖 (<70 mg/dL): NAP (2.0%) vs UMPC (1.8%),兩者相似且處於安全範圍
安全性: 整個試驗過程中,兩種控制器均未發生嚴重不良事件 。這張表為 NAP 作為醫療級演算法提供了堅實的數據支撐。

向終極目標:挑戰全閉環 (FCL) 的重要里程碑
視覺內容: HCL(需手動輸入餐食)與 FCL(完全自動化)的圖示對比。強調 NAP 在 FCL 模式下達到 75% TIR。
詳細說明:
HCL vs. FCL: 現有 HCL 系統仍需用戶手動「宣告」餐食;FCL 則追求完全無感知的自動化 。
FCL 的挑戰: 缺乏餐食預告會導致血糖控制難度劇增。
關鍵成就: NAP 在 FCL 模式下(無餐食宣告)仍實現了 75% 的 TIR 。這是一個重大里程碑,證明了 NAP 基於 AI 的模式識別能力,能夠實時推斷餐食影響並進行補償,縮小了 HCL 與 FCL 之間的性能差距 。
效率的戰略價值:驅動系統去中心化與微型化
視覺內容: 對比「當前模式(中心化/手機依賴)」與「未來模式(去中心化/泵上 AI)」。
詳細說明: NAP 的高效率解鎖了硬體形態的變革:
當前問題: 演算法運行在手機上,藍牙連接是潛在故障點,且耗電量大 。
未來優勢 (NAP Inside): 由於運算負載低,演算法可以直接在胰島素泵的晶片上運行(On-pump AI) 。這消除了通訊延遲風險,延長了電池壽命,並使設備能做得更小(微型化),顯著降低用戶負擔 。

導航未來:監管途徑與倫理考量
視覺內容: 盾牌(監管)與人群(倫理)的圖示。提及 FDA 的 PCCP 計畫。
詳細說明: 作為 AI 醫療設備(SaMD),NAP 面臨獨特的挑戰:
監管 (FDA PCCP): 為了適應 AI 持續學習的特性,需採用 FDA 的「預定變更控制計畫(PCCP)」。這允許製造商在預定範圍內對演算法進行自動優化,而無需每次微調都重新送審
數據公平性: 訓練數據需具備代表性,避免因種族或年齡(如現有數據多為白人)導致的演算法偏差 。
網絡安全: 實時數據傳輸必須加密,防止惡意攻擊導致錯誤的胰島素輸注 。
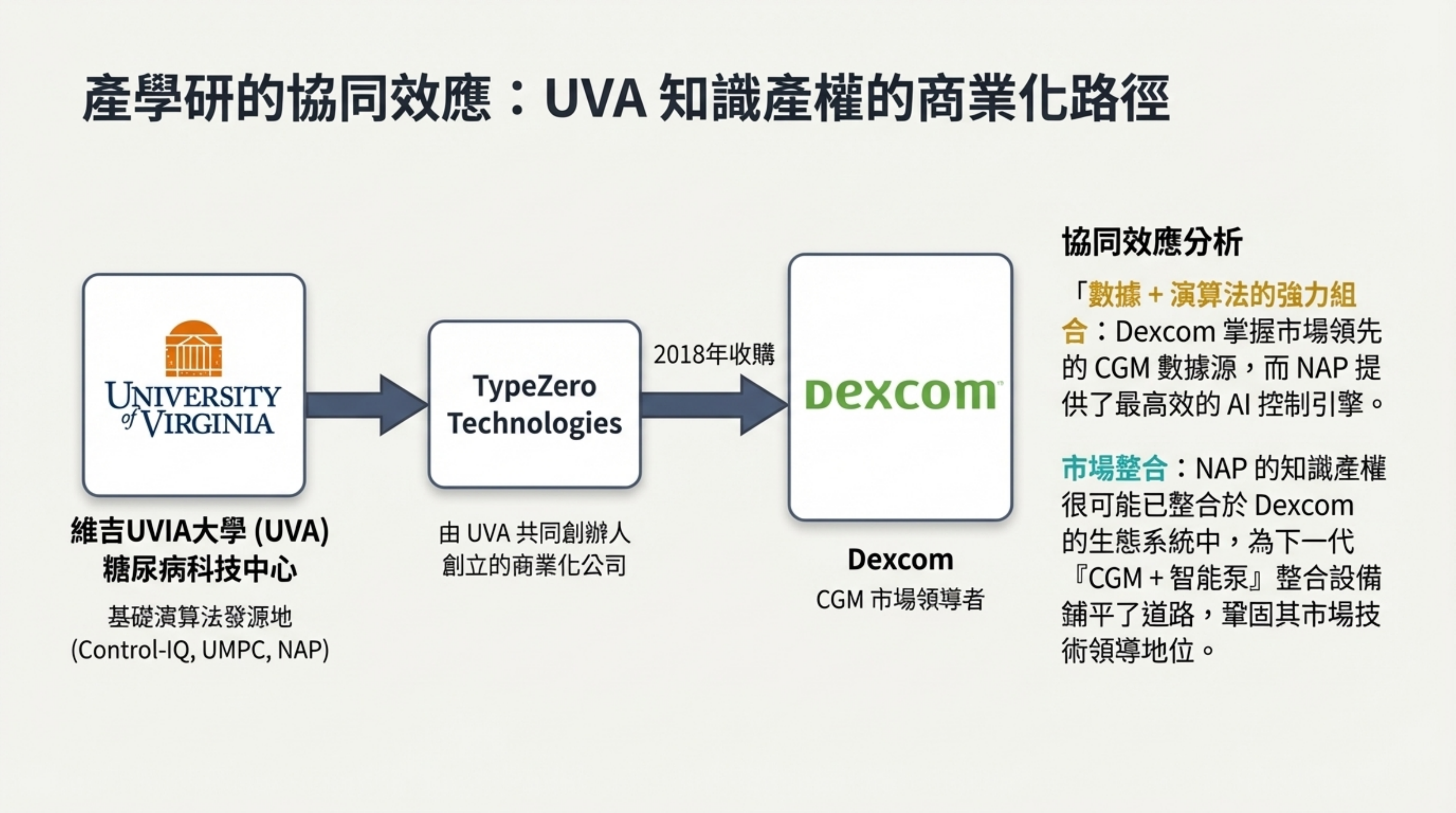
產學研的協同效應:UVA 知識產權的商業化路徑
視覺內容: 流程圖顯示:UVA -> TypeZero -> Dexcom (2018年收購)。
詳細說明: NAP 技術並非孤立存在,而是深深嵌入商業生態系統:
路徑: 源自 UVA 糖尿病科技中心的基礎演算法,透過新創公司 TypeZero Technologies 進行商業化轉化 。
整合: TypeZero 於 2018 年被 CGM 巨頭 Dexcom 收購 。
協同效應: 這意味著 NAP 的高效 AI 引擎很可能已經或即將與 Dexcom 的市場領先 CGM 數據整合,為下一代「CGM + 智能泵」的一體化設備鋪平道路,鞏固其市場領導地位 。
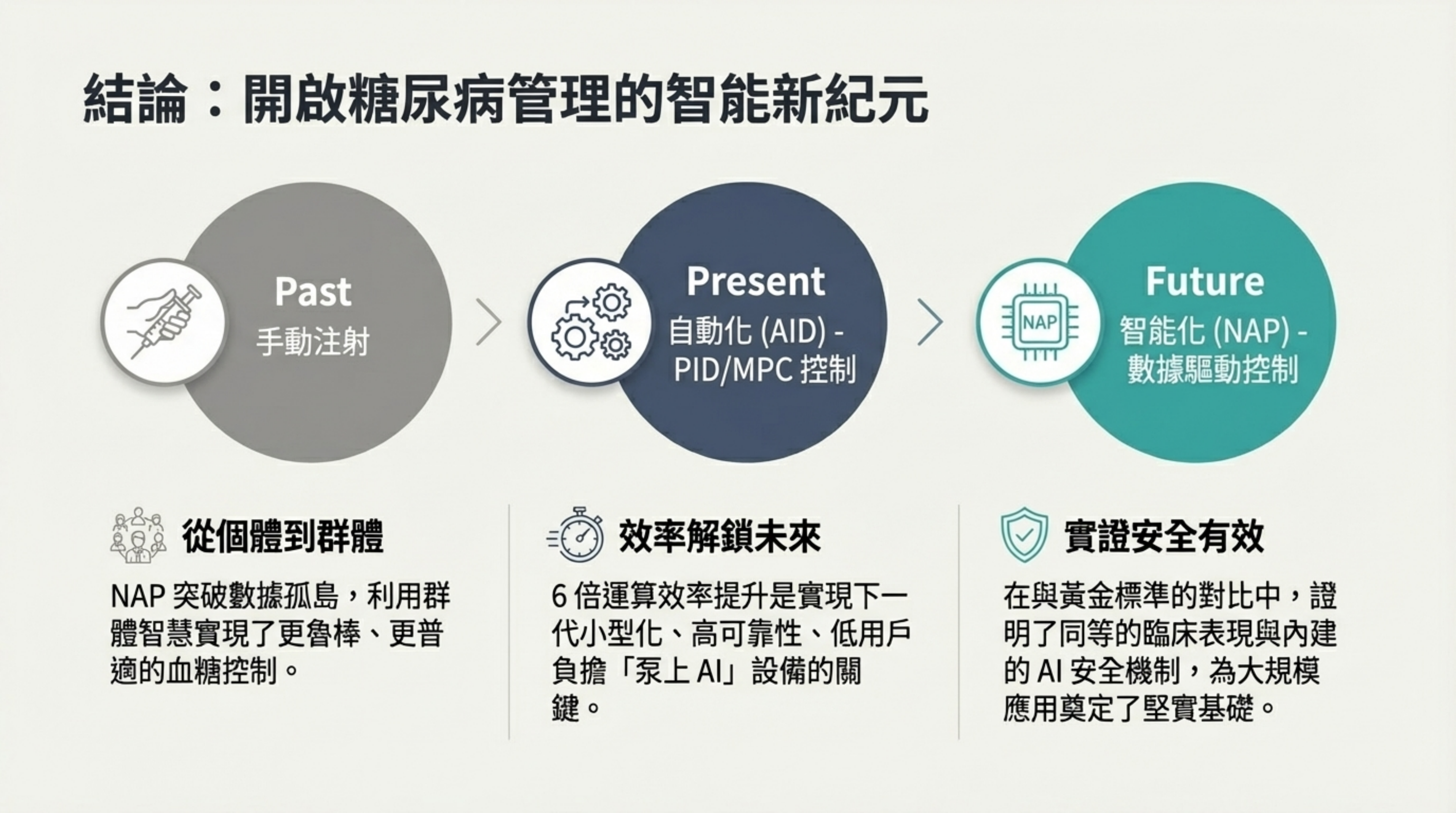
結論:開啟糖尿病管理的智能新紀元
視覺內容: Past(手動)-> Present(自動化 PID/MPC)-> Future(智能化 NAP)的三階段演進圖。
詳細說明: 總結 NAP 的三大貢獻:
-
從個體到群體: 突破數據孤島,利用群體智慧實現更魯棒的控制 。
-
效率解鎖未來: 6 倍運算效率提升是實現下一代小型化、高可靠性「泵上 AI」設備的關鍵
-
實證安全有效: 在與黃金標準的對比中,證明了同等的臨床表現與內建的 AI 安全機制
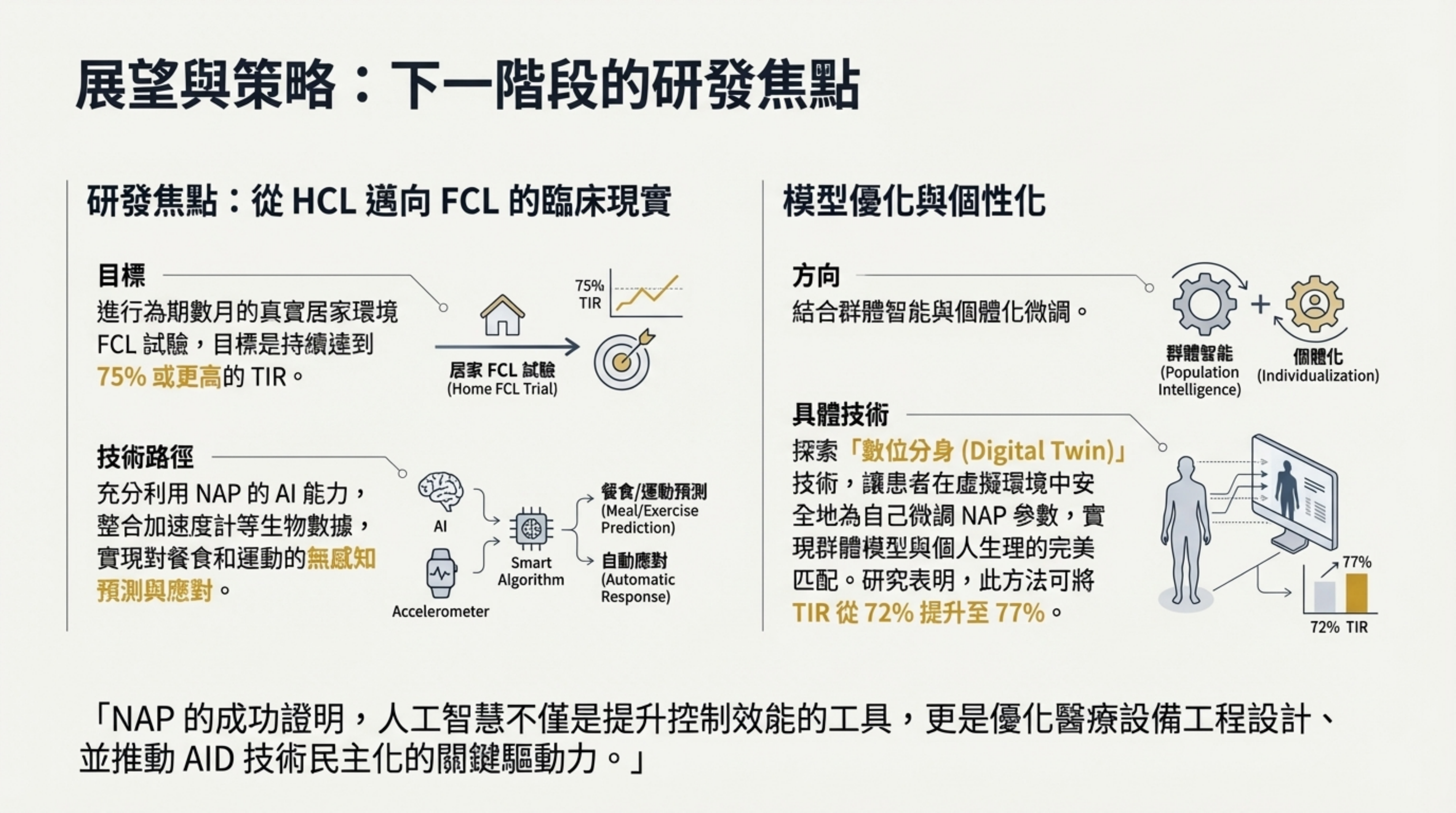
展望與策略:下一階段的研發焦點
視覺內容: 兩大支柱:「從 HCL 邁向 FCL」與「模型優化與個性化(數位分身)」。
詳細說明: 未來的戰略藍圖:
邁向 FCL: 利用 NAP 的 AI 能力整合加速度計等生物數據,實現對餐食和運動的「無感知」預測與應對,目標是在居家 FCL 試驗中維持 75% 或更高的 TIR 。
數位分身(Digital Twin): 結合群體智能與個性化微調。讓患者在虛擬環境中利用數位分身安全地測試參數,研究顯示此方法可將 TIR 從 72% 提升至 77% 。
結語: AI 不僅提升效能,更是優化硬體設計、推動 AID 技術民主化的關鍵驅動力。
References (參考文獻)
- Brown, S. A., et al. (2023). Neural-Net Artificial Pancreas: A Randomized Crossover Trial of a First-in-Class Automated Insulin Delivery Algorithm. PubMed/PMC.
- ClinicalTrials.gov. NCT05876273 | Neural-net Artificial Pancreas (NAP).
- UVA Health. (2023). Adding AI to Artificial Pancreas Enhances Efficiency, Study Finds. Medicine in Motion News.
- Pinsker, J. E., et al. (2016). Randomized Crossover Comparison of Personalized MPC and PID Control Algorithms. Diabetes Care / PMC.
- Kovatchev, B. (2018). The Artificial Pancreas. Diabetes Spectrum. (Contextual support for MPC/PID comparison).
- UVA Health. Interactive Artificial Pancreas Better Controls Type 1 Diabetes Using Digital Twins, Study Finds.
- FDA. (2023). Marketing Submission Recommendations for a Predetermined Change Control Plan for Artificial Intelligence-Enabled Device Software Functions.
- Bipartisan Policy Center. FDA Oversight: Understanding the Regulation of Health AI Tools.
- Global Corporate Venturing. (2018). Dexcom collects TypeZero.
- NIDDK/NIH. Real-World Use of a New Hybrid Closed Loop Improves Glycemic Control in Youth with Type 1 Diabetes.
