Tirzepatide 臨床安全性綜述 — Part 3:延伸議題與全研究整合
綜述類型: 敘述性綜述(Narrative Review) 涵蓋主題: 甲狀腺安全性、心血管效應、癌症風險、特殊族群 文獻截止日: 2026-03-29 證據等級標示: ⬛ Strong | 🟧 Moderate | 🟨 Limited | ⬜ Expert opinion / Knowledge gap
前言
Part 3 為本系統性研究的最終階段,涵蓋四個延伸議題:(1) 甲狀腺安全性——GLP-1 RA 類別最具爭議的黑框警告背後的科學;(2) 心血管效應——SUMMIT 和 SURPASS-CVOT 的里程碑式結果;(3) 癌症風險的全面評估;(4) 六大特殊族群的安全性概覽。至此,全部 10 個預定主題(Part 1–3)研究結束,本綜述同時提供跨 Part 的整合分析與最終優先知識缺口清單。

第一章:甲狀腺安全性
1.1 囓齒類 C-cell 腫瘤——FDA 黑框警告的科學基礎
Tirzepatide(及所有 GLP-1 RA)的處方資訊均帶有 FDA 黑框警告(Black Box Warning):大鼠 2 年致癌性研究顯示劑量依賴性甲狀腺 C-cell 腺瘤及癌發生率增加。Tirzepatide 在最低致癌劑量(雌鼠 0.15 mg/kg)時約為人類最大建議劑量(15 mg/週)的 8 倍暴露量(以 AUC 計)1。
此發現為所有 GLP-1 RA 共有:liraglutide、semaglutide、exenatide 均在大鼠研究中顯示相似結果。
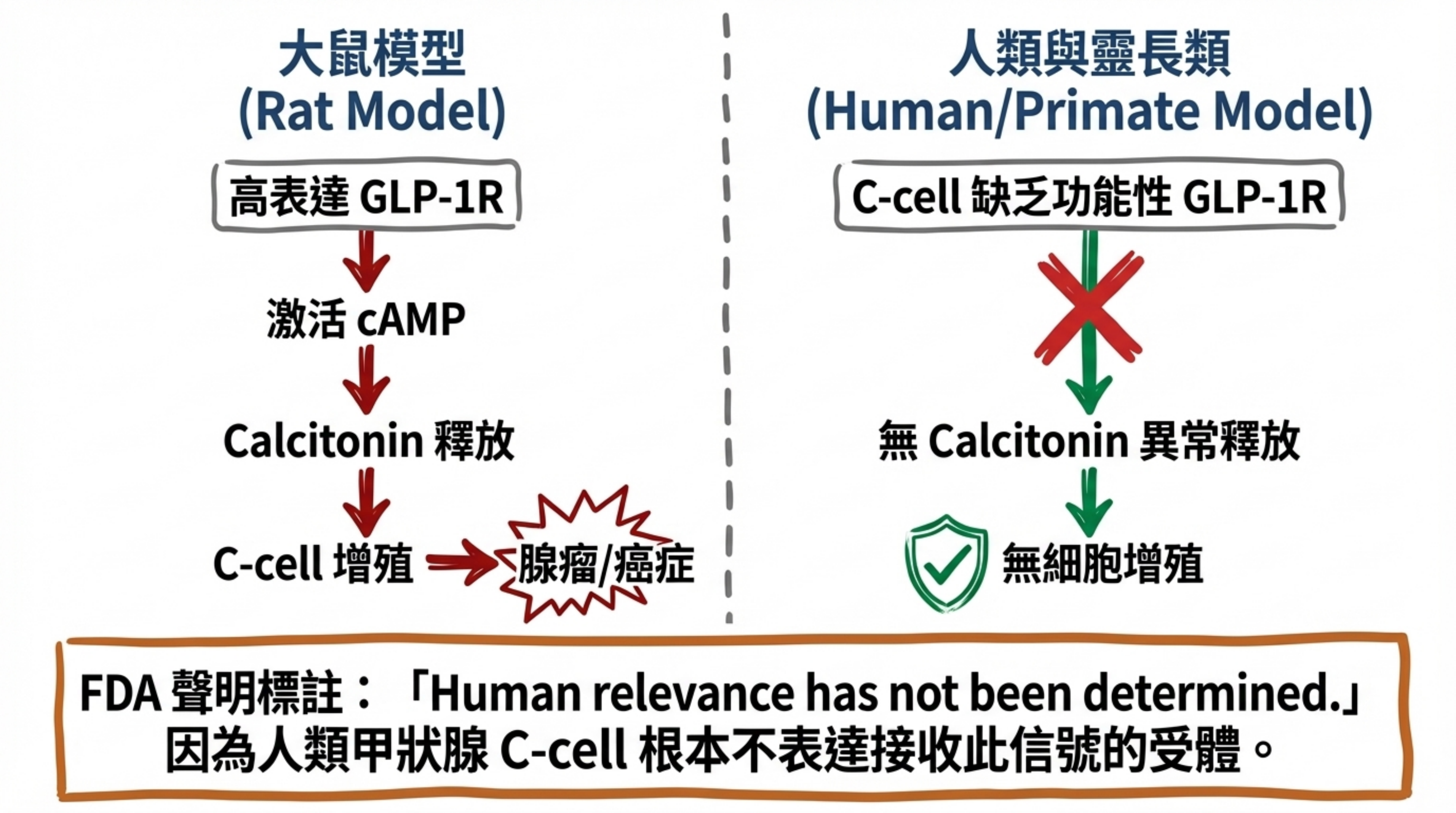
1.2 物種差異——核心科學基礎(⬛ Strong)
人類 C-cell 不表達功能性 GLP-1 受體,這是理解整個甲狀腺安全性爭議的關鍵。
Knudsen et al.(2010)的奠基性研究明確顯示:「Humans and/or cynomolgus monkeys had low GLP-1 receptor expression in thyroid C-cells, and GLP-1 receptor agonists did not activate adenylate cyclase or generate calcitonin release in primates.」2
Boess et al.(2013)更進一步確認:「GLP1R expression was observed in primary rat C-cells but was not detected in primary human C-cells (mRNA and protein levels).」人類甲狀腺培養物對 GLP-1 RA 刺激無任何功能性反應 3。
| 物種 | C-cell GLP-1R 表達 | Calcitonin 釋放反應 | C-cell 增殖 |
|---|---|---|---|
| 大鼠 | +++ 高 | 顯著增加 | 顯著增殖→腫瘤 |
| 獼猴 | +/- 低/無 | 無 | 無 |
| 人類 | 未偵測到 | 無 | 理論上極低 |
基於此物種差異,FDA 的黑框警告措辭為「human relevance has not been determined」——一個審慎而非確定性的聲明。
1.3 臨床試驗數據
Tirzepatide RCT(⬛ Strong): Kamrul-Hasan et al.(2025)基於 13 個 RCT(N=13,761,追蹤 26–72 週)的 meta-analysis 顯示甲狀腺癌整體 RR=0.78(95% CI 0.53–1.16),且全系列試驗中 0 例甲狀腺髓質癌(MTC)報告 4。
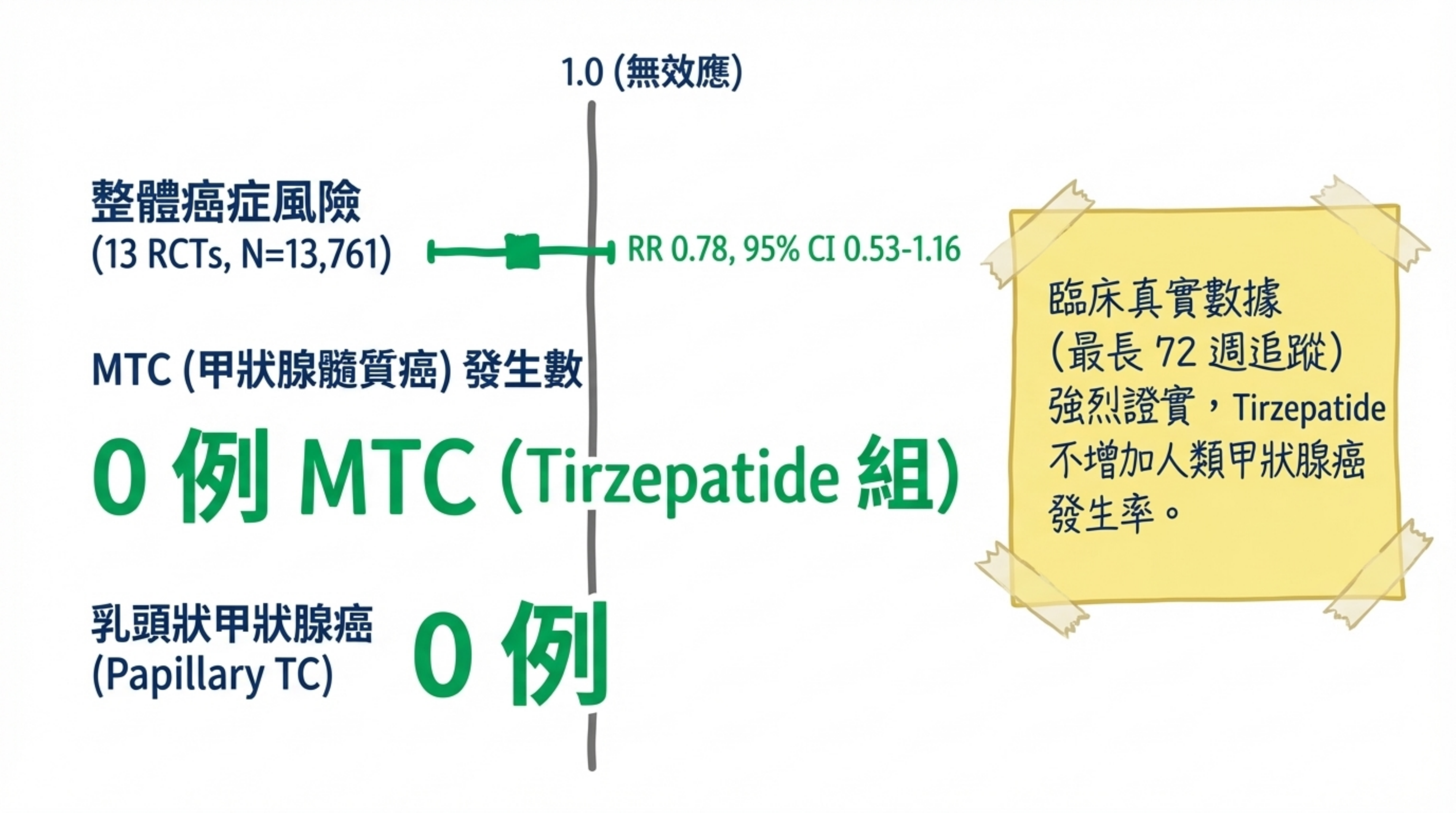
GLP-1 RA 類別 RCT: Silverii et al.(2024)的 64 RCT meta-analysis 顯示 GLP-1 RA 甲狀腺癌整體 MH-OR=1.52(1.01–2.29),此結果具爭議性——大多數試驗追蹤 <2 年、事件數極少、無法區分 MTC vs. 偶發性分化型甲狀腺癌。NNH 約 1,349 人(5 年),絕對風險極低 5。
1.4 大型族群研究——最強安心證據
四項大型族群研究(涵蓋 >300 萬人)一致不支持甲狀腺癌風險增加:
| 研究 | 設計 | N | HR(甲狀腺癌整體) | 結論 | PMID |
|---|---|---|---|---|---|
| Pasternak(Scandinavian) | Cohort | 145,410 | 0.93(0.66–1.31) | 無增加 | 38683947 |
| Baxter(6 國) | Multisite cohort | >200,000 | 0.81(0.59–1.12) | 無增加 | 39772758 |
| Morales | Retrospective cohort | 460,032 | 0.83–0.95 vs. SGLT2i | 無增加 | 40465422 |
| Pollack | Cohort(中位 4.5 年) | 大規模 | 不增加 | 無增加 | PMC12582397 |
證據批判: 一項早期法國 cohort(Bezin et al., 2023)報告 1–3 年 HR=1.58、MTC HR=1.78 6。然而,此研究的設計缺陷被廣泛討論:(a) 使用 DPP-4i 作為對照組(metabolic profile 不同);(b) 短期追蹤中 MTC 事件可能為預存腫瘤的早期偵測(detection bias)而非新發;(c) 後續更大規模研究均未重現此結果。
1.5 FAERS 信號
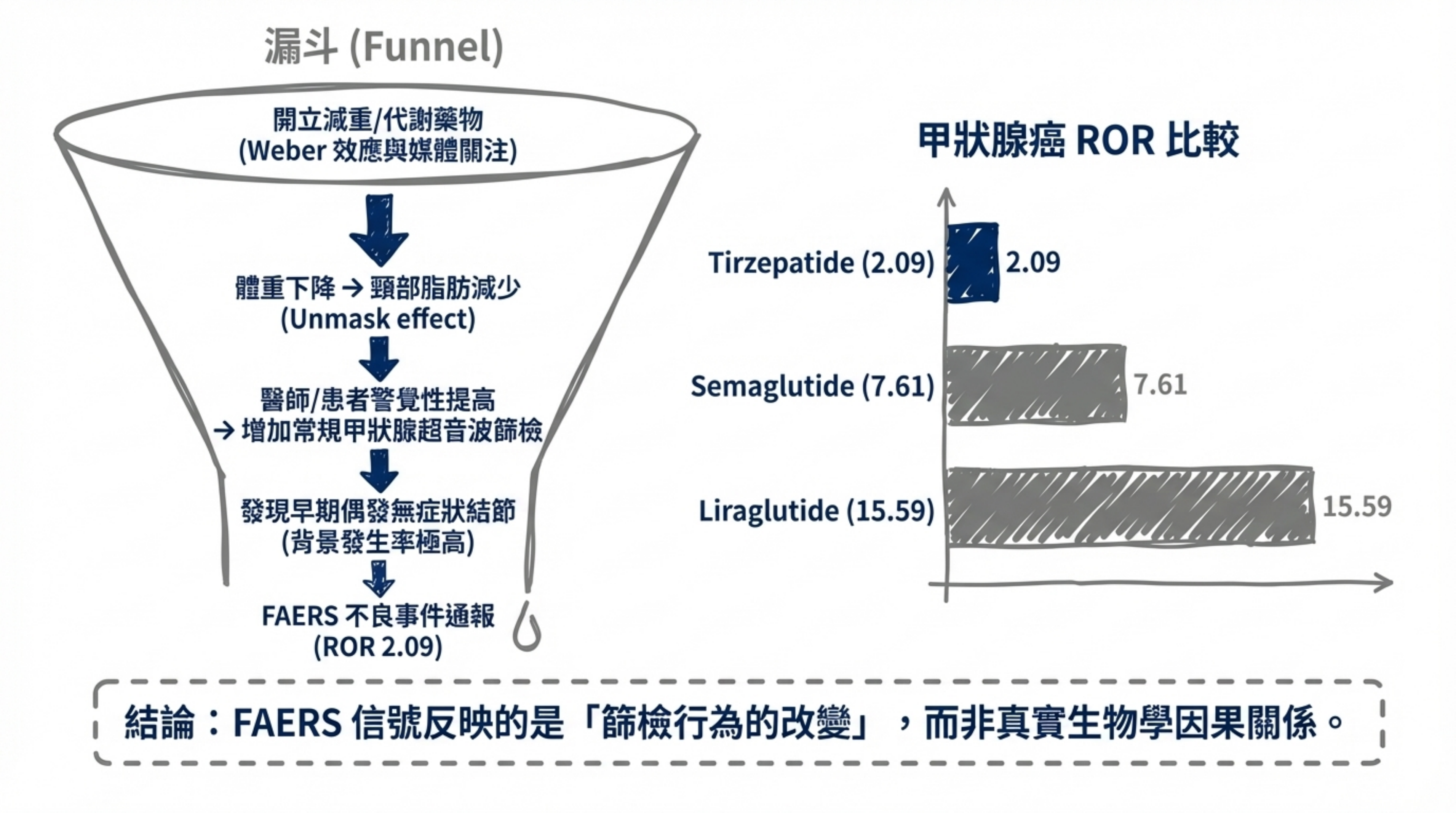
Daou et al.(2025)分析顯示 tirzepatide 的甲狀腺癌 ROR=2.09,在所有 GLP-1 RA 中最低(liraglutide ROR=15.59;semaglutide ROR=7.61)7。整體 GLP-1 RA 類別的 FAERS MTC PRR 為 27.43,但 FAERS 不成比例報告極易受 notoriety bias 和 Weber effect 影響。
1.6 GIP 受體在 MTC 中的表達
一項值得關注的發現:ECE 2022 會議報告顯示 GIPR 在 80% 的 MTC 腫瘤中有表達,且具功能性 cAMP 活化 8。然而,此發現並不意味著 tirzepatide 促進 MTC 增殖——(a) GIPR 表達不等於促增殖;(b) 人類正常 C-cell 不表達 GLP-1R(tirzepatide 的另一靶點);(c) 臨床數據中 0 例 MTC。此議題需要進一步的功能性研究。
1.7 甲狀腺功能影響
TSH 變化(🟨 Limited): 一項 Endocrine Society 2023 會議摘要報告,在使用 tirzepatide 的甲狀腺功能低下患者中,65% 出現 TSH 降低,29% 降至低於正常值 9。可能機制包括體重減輕對甲狀腺素代謝的影響或藥物的直接中樞效應。正在使用 levothyroxine 的患者可能需要調整劑量。
首例 tirzepatide 相關無痛性甲狀腺炎(painless thyroiditis)亦已被報告(PMID 40458348),為極罕見事件。
1.8 臨床建議
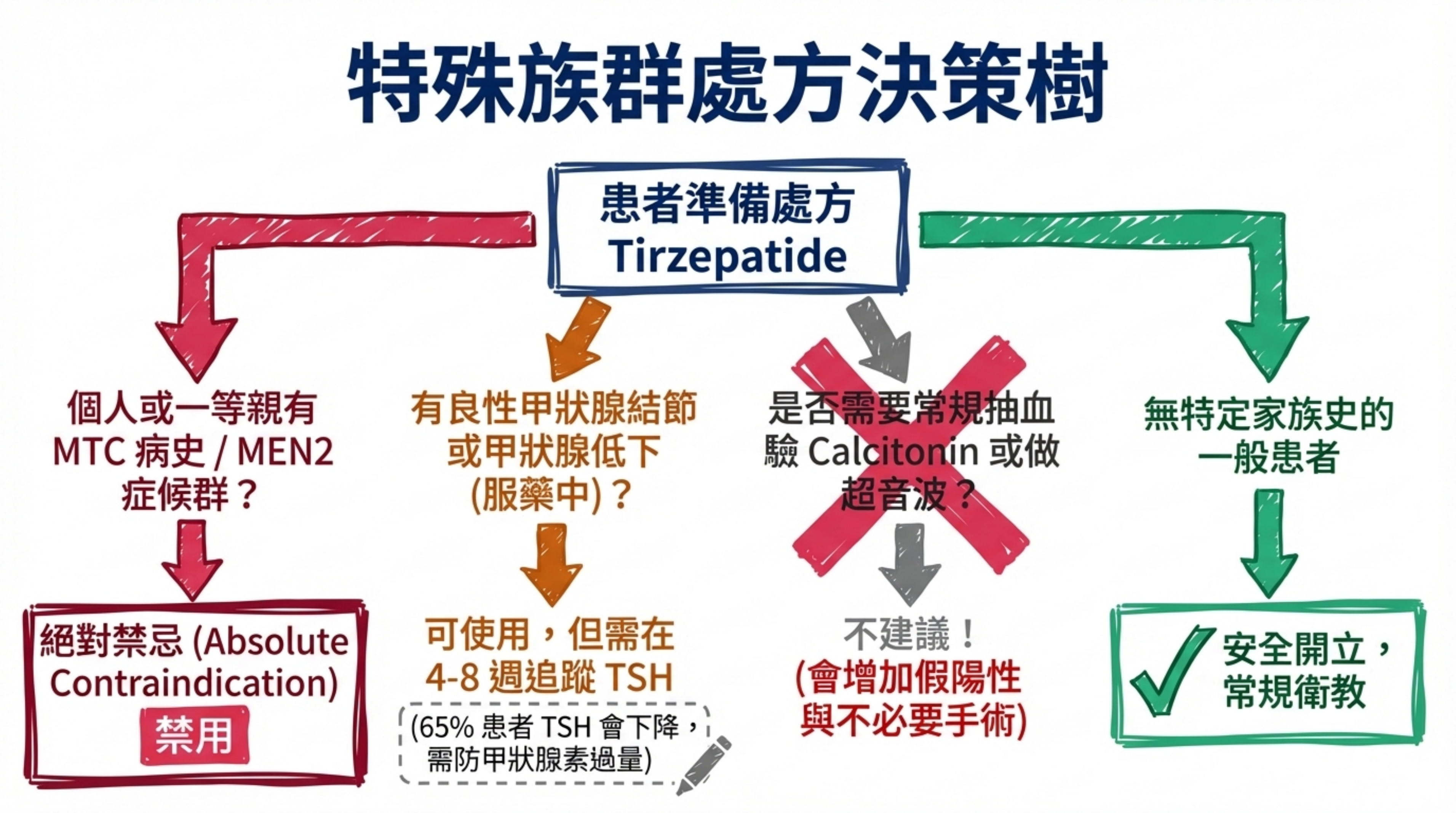
- MTC 病史/家族史、MEN2 仍為絕對禁忌(FDA 黑框警告)。
- 不建議常規甲狀腺超音波篩查——evidence 不支持 GLP-1 RA 增加人類甲狀腺癌風險,且常規篩查可能導致偶發結節的過度診斷和不必要手術。
- 甲狀腺功能低下患者使用 tirzepatide 後建議在 3–6 個月追蹤 TSH。
- 若治療中發現甲狀腺結節,按標準指引處理(FNA 等),不需因 GLP-1 RA 使用而改變管理策略。
第二章:心血管效應
2.1 SUMMIT 試驗——HFpEF 的里程碑
SUMMIT(NCT04847557) 是 tirzepatide 心血管安全性的標誌性試驗,在射出分率保留型心衰竭(HFpEF)合併肥胖(BMI ≥30)患者中評估 tirzepatide 的心血管效益(⬛ Strong)10。
| 終點 | Tirzepatide (n=364) | Placebo (n=367) | HR (95% CI) |
|---|---|---|---|
| CV 死亡 + 惡化心衰竭(主要複合) | 9.9% | 15.3% | 0.62 (0.41–0.95), p=0.026 |
| 惡化心衰竭(單獨) | 8.0% | 14.2% | 0.54 (0.34–0.85) |
| KCCQ-CSS(52 週改善) | +19.5 分 | +12.7 分 | 差 6.9 分, p<0.001 |
| 6MWD(52 週改善) | +26.0 m | +10.1 m | p<0.001 |
| hsCRP(52 週) | −38.8% | −5.9% | p<0.001 |
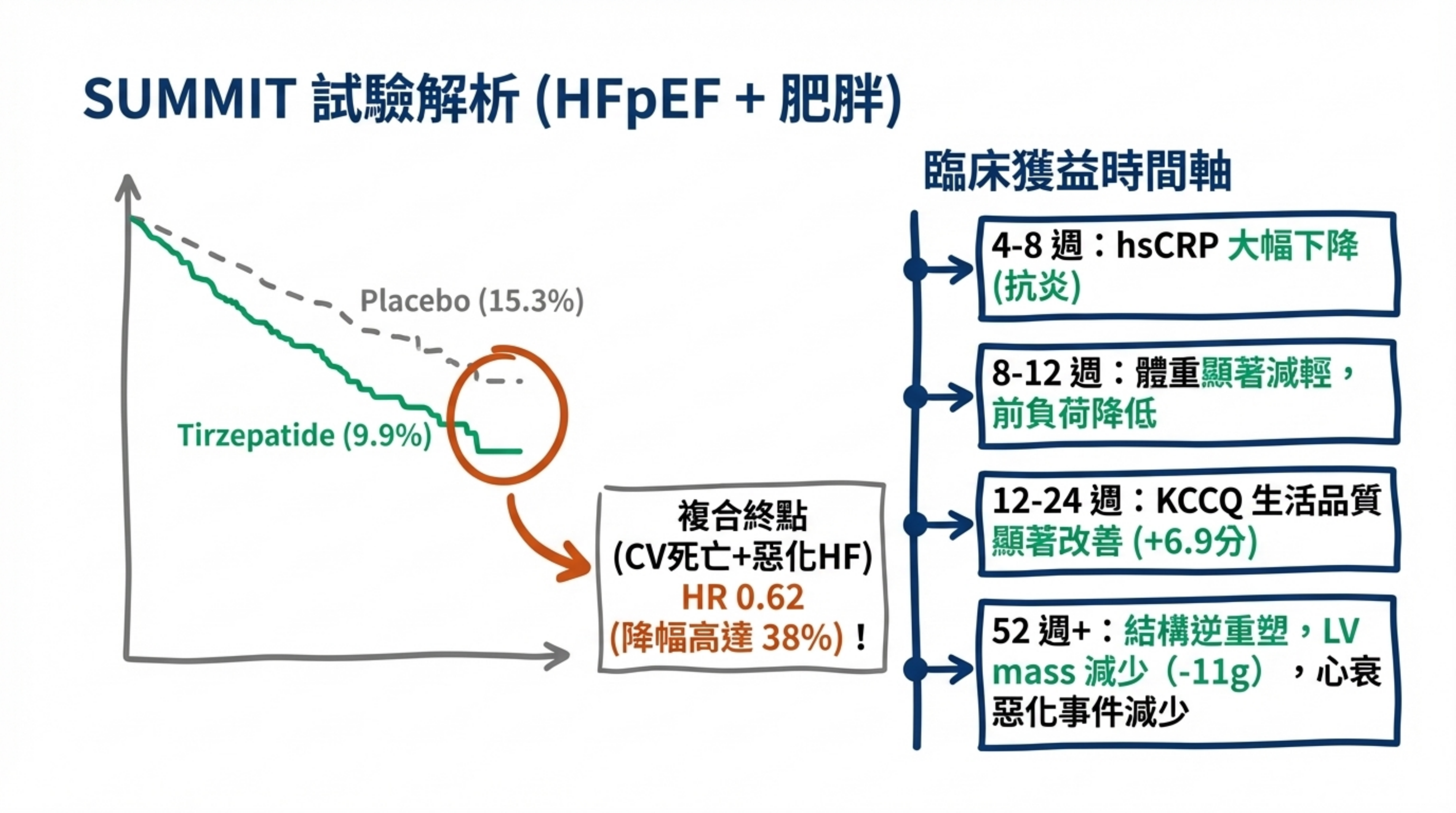
SUMMIT CMR 子研究: 心臟磁共振顯示 tirzepatide 減少左心室質量(−11 g, p=0.004)和心臟旁脂肪組織(−45 mL, p<0.001),提示重要的結構逆重塑機制 11。
臨床意義: SUMMIT 是首個在 HFpEF 族群中顯示 incretin 藥物降低心血管事件的 Phase 3 RCT。46% 的心衰惡化事件相對風險下降,加上具臨床意義的症狀和功能改善,確立了 tirzepatide 在肥胖相關 HFpEF 的治療地位。ACC 2025 科學聲明已將 tirzepatide 納入 HFpEF 合併肥胖的治療選項 12。
2.2 SURPASS-CVOT——完整 MACE 數據
SURPASS-CVOT 是 tirzepatide 的專屬心血管結果試驗(CVOT),在 T2D 合併確立 ASCVD 的患者中比較 tirzepatide vs. dulaglutide 1.5mg,N=13,165,中位追蹤 4 年(⬛ Strong)13。
| 終點 | Tirzepatide | Dulaglutide | HR (95% CI) |
|---|---|---|---|
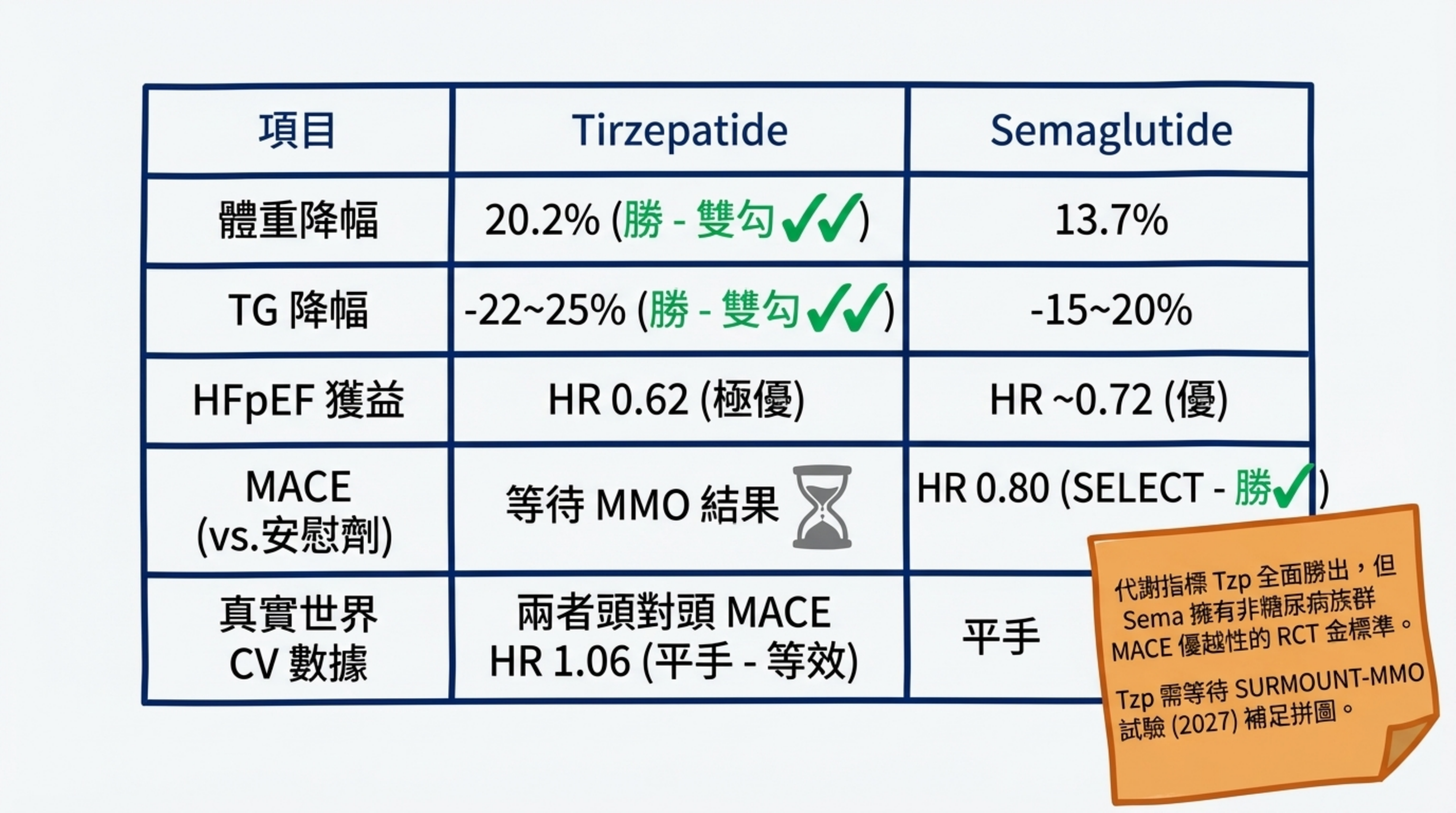
| 3-point MACE(CV 死亡+MI+中風) | 12.2% | 13.1% | 0.92 (0.83–1.01), NI 達到; 優越性 p=0.09 |
| 4-point MACE(+冠狀動脈重建) | — | — | 0.88(顯著) |
| 全因死亡 | 8.6% | 10.2% | 0.84 (0.75–0.94), 顯著 |
關鍵解讀:
- 3-point MACE 對 dulaglutide(本身已有 CV 效益的 GLP-1 RA)達到非劣效性,未達優越性——但比較對象本身很強,無非劣效性即代表 CV 安全性無疑。
- 全因死亡率顯著減少 16%(HR 0.84),主要由非 CV 死亡驅動,可能反映代謝改善的多系統獲益。
- 代謝差異:tirzepatide 體重下降 11.6% vs. dulaglutide 4.5%;HbA1c 差距 −0.78%。

2.3 血壓效應
Tirzepatide 的降壓效果具有臨床意義且劑量依賴(⬛ Strong):
SURMOUNT-1 ABPM 子研究(N=494)14:
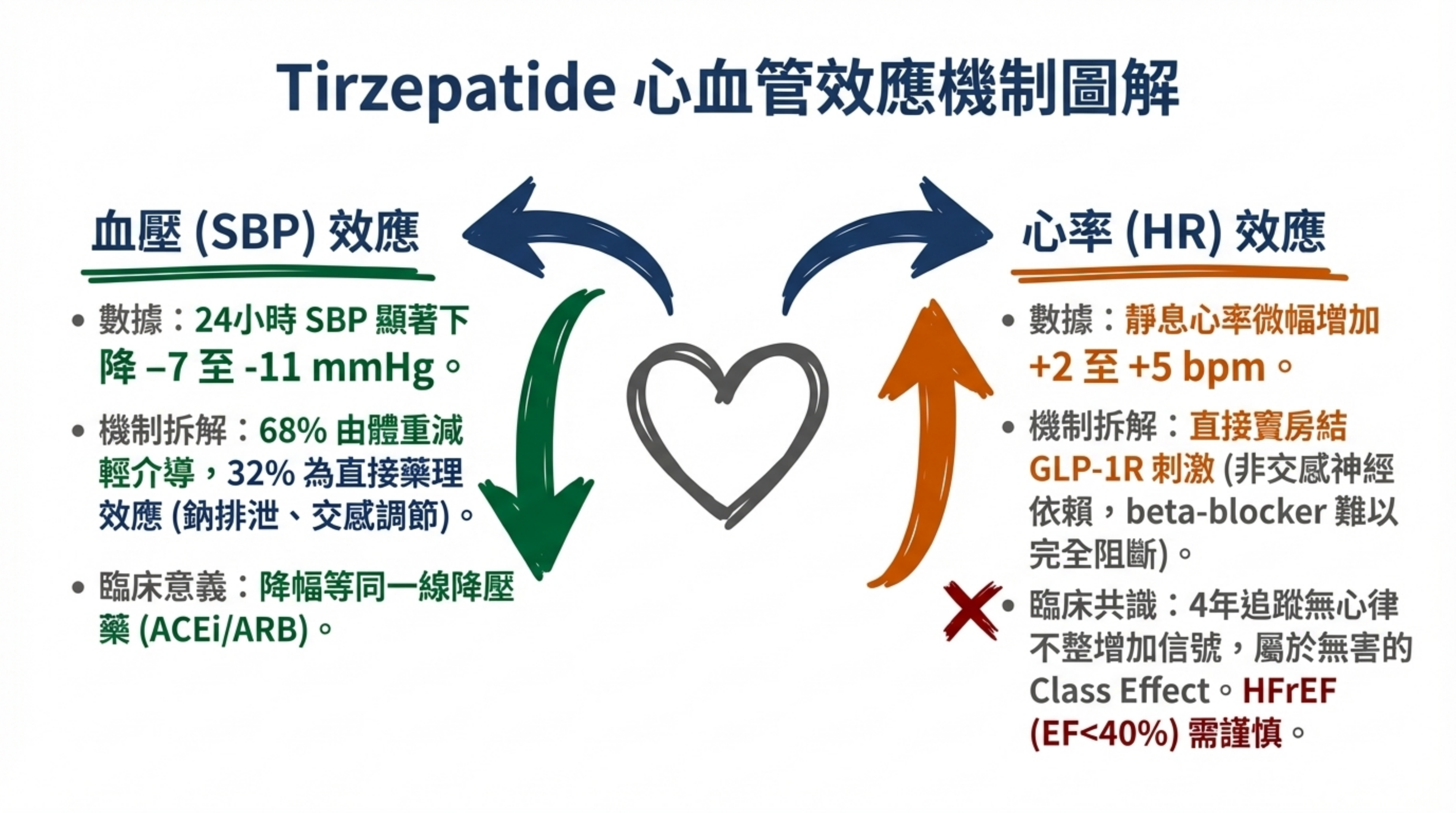
- 24 小時 SBP 下降(安慰劑調整):5mg −7.4 mmHg;10mg −10.6 mmHg;15mg −8.0 mmHg
- 72 週時 58% tirzepatide 組達到正常血壓(vs. 35% placebo)
中介分析: 體重減輕貢獻約 68% 的 SBP 下降、71% 的 DBP 下降。其餘 ~30% 為體重非依賴性機制(可能涉及腎臟鈉排泄增加、交感神經活性改變)15。
臨床意義: SBP 下降 7–11 mmHg 與大多數一線降壓藥(ACE 抑制劑、ARB 的 SBP −6–10 mmHg)效果相當,可望帶來獨立的 CV 事件減少。
2.4 心率變化
Tirzepatide 造成輕度心率增加:5mg +2.1 bpm;10mg +2.3 bpm;15mg +5.4 bpm(⬛ Strong)14。此為 GLP-1 RA 的類別效應(semaglutide +1–3 bpm;liraglutide +2–4 bpm)。機制主要為直接竇房結 GLP-1R 刺激,而非交感神經激活。
SURPASS-CVOT(4 年追蹤)無心率相關安全訊號;tirzepatide 組中未見心律不整增加。+2–5 bpm 的增幅在臨床上不影響心臟做功或耗氧量。
2.5 脂質與發炎標記
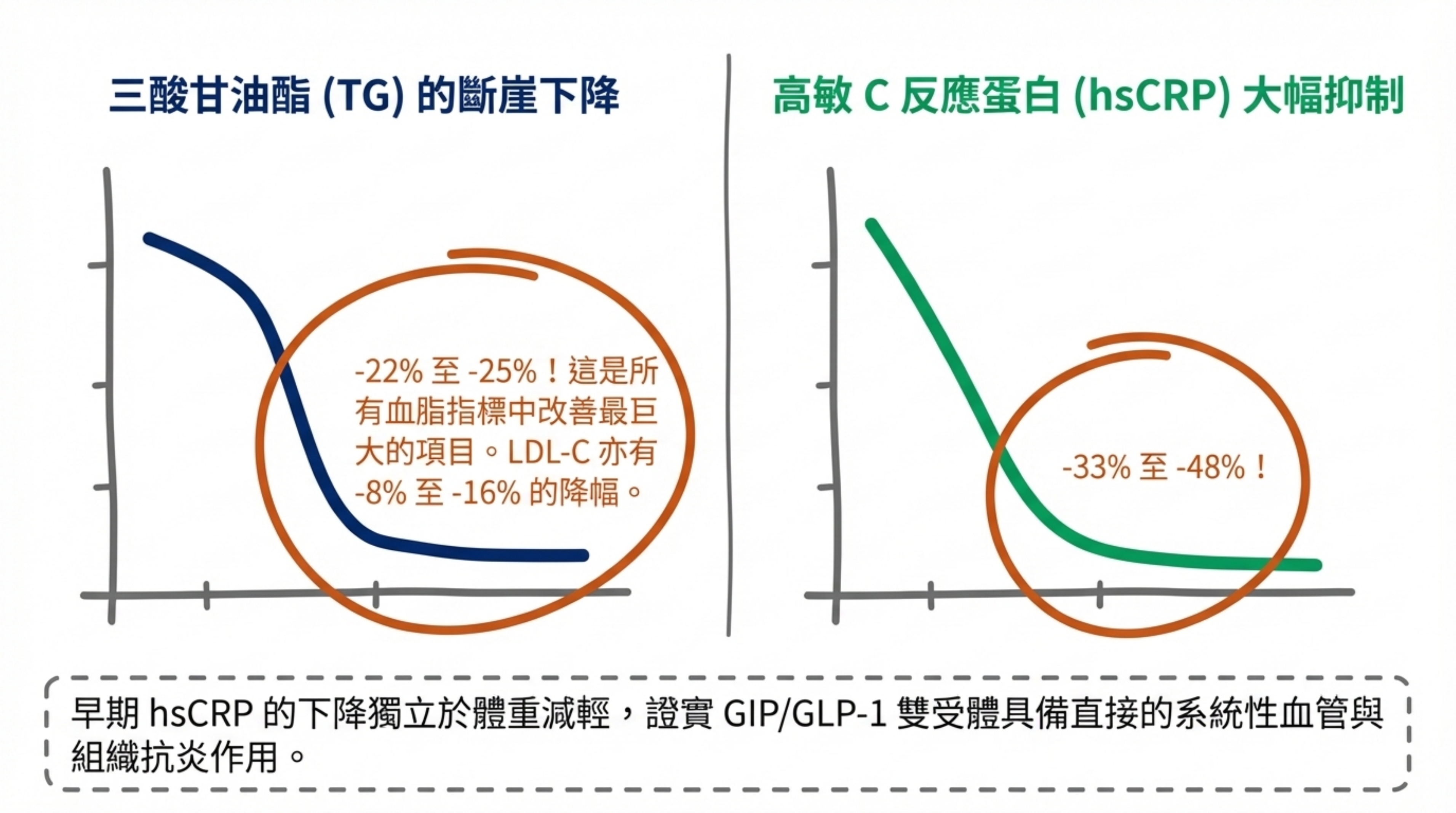
| 指標 | Tirzepatide 效應 | 臨床意義 |
|---|---|---|
| TG(三酸甘油酯) | −22–25% | 最顯著的脂質效應 |
| LDL-C | −8–16% | 中等效果 |
| hsCRP | −33–48% | 強烈抗炎效應 |
| Lp(a) | 略降或不變 | 需更多數據 |
| TC | −5.6% | 輕度 |
hsCRP 的大幅下降(−33–48%)特別值得關注,反映 tirzepatide 的系統性抗炎效應,可能獨立於代謝改善對 CV 風險產生保護。
2.6 待定:SURMOUNT-MMO
SURMOUNT-MMO(NCT05556512) 是正在進行的大型 CVOT,在非糖尿病心血管高風險肥胖患者中評估 tirzepatide 的 MACE 效益(~15,000 人),預計 2027–2028 年完成 16。這將填補 SELECT 試驗(semaglutide 在非糖尿病肥胖患者中 MACE −20%)的 tirzepatide 對應數據空白。
第三章:癌症風險
3.1 整體癌症安全性
最大規模 RCT meta-analysis(⬛ Strong): Ko et al.(2026)涵蓋 48 個 RCT(N=94,245),為迄今最大規模的 GLP-1 RA 癌症安全性分析。結論:GLP-1 RA(含 tirzepatide)對 13 種肥胖相關癌症幾乎無影響(中等確定性)17。
Tirzepatide 特異性 RCT: Kim MK et al.(2025)的 13 RCT meta-analysis(N=13,761)顯示整體癌症 RR=0.78(0.53–1.16),無顯著差異。各劑量(5/10/15mg)均無劑量相關癌症風險增加 4。
關鍵限制: RCT 追蹤期(最長 72 週)遠短於多數癌症潛伏期(>10 年)。「RCT 未見信號」≠「長期無風險」。此限制必須明確告知。
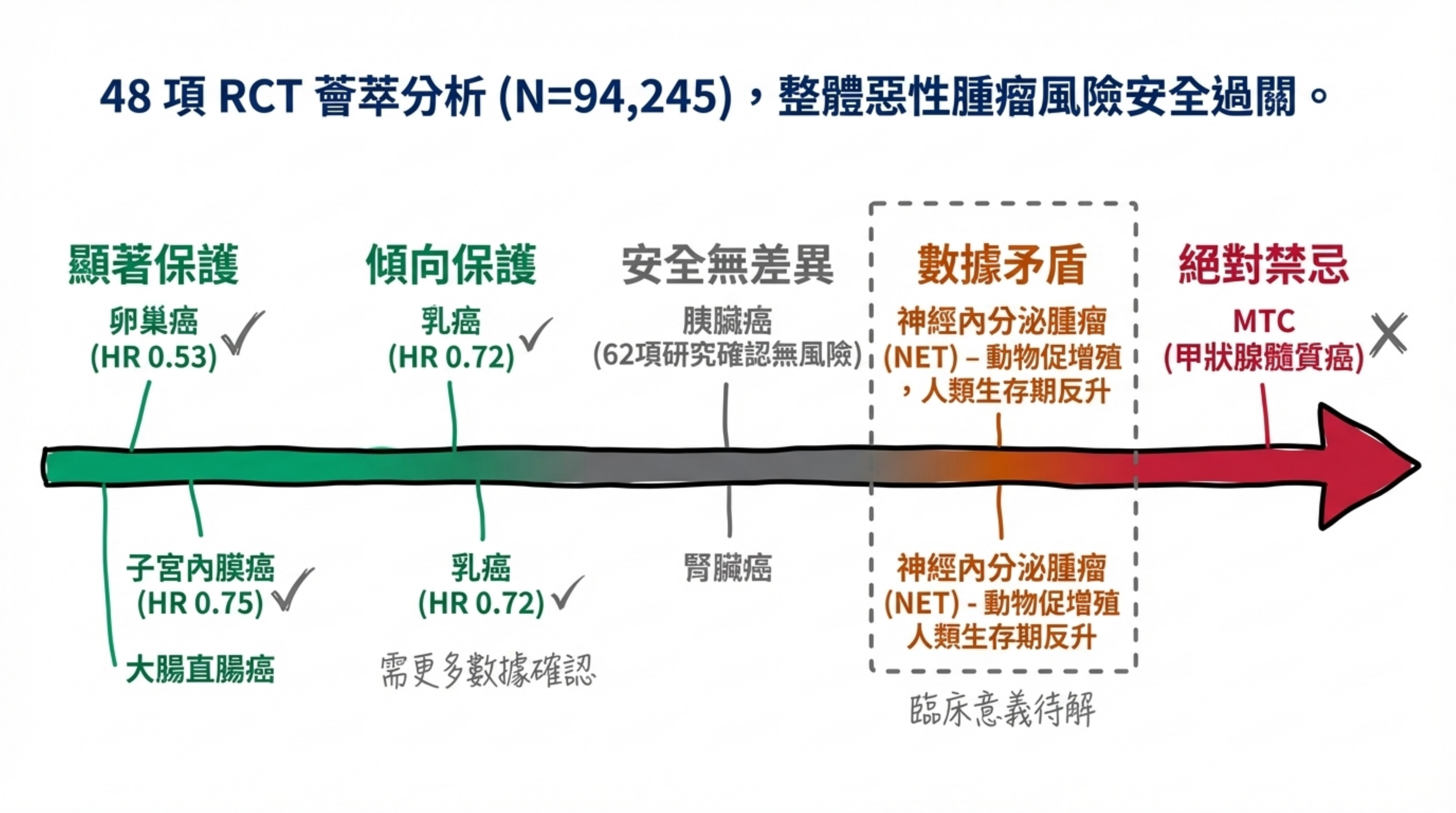
3.2 器官特異性癌症——保護效應的新興證據
子宮內膜癌——最有說服力的保護證據(🟧 Moderate):
- 兩項獨立大型世代研究均顯示 HR ~0.75(25% 相對風險降低)1819。
- 前臨床金標準研究(Bhatt et al., 2024):tirzepatide 在小鼠模型中直接縮小子宮內膜癌腫瘤,通過體重依賴(雌激素降低)和體重非依賴(ErbB 信號抑制、糖酵解干預)雙重機制 20。
- 機制清晰:減重 → 脂肪組織 aromatase 活性↓ → 雌激素暴露↓ → 風險↓。
乳癌(🟧 Moderate):
- 1.1 百萬肥胖患者世代顯示 HR=0.72(保護傾向)19。
- 前臨床:肥胖小鼠 tirzepatide 治療使腫瘤體積縮小 ~20%。
- FITWISE 試驗:HR+/HER2- 乳癌患者使用 tirzepatide 可耐受,無安全疑慮。
- RCT meta-analysis:RR=0.59(0.21–1.65),傾向保護但未達顯著 4。
大腸直腸癌(🟧 Moderate):
- 大型 T2DM 世代(N=1.65 百萬):顯著風險降低 18。
- ACG 摘要:早發性 CRC OR=0.61(39% 保護)。
- 前臨床亮點(Zhang et al., 2025):tirzepatide 通過 GIPR/GLP-1R 雙重激動靶向 HIF-1α 介導的糖酵解(Warburg effect),抑制結腸癌增殖——在高血糖和正常血糖條件下均有效 21。
- 注意:部分回顧性研究因嚴重混雜因子顯示矛盾的 RR 2.31,解釋為 detection bias 和未校正的適應症差異。
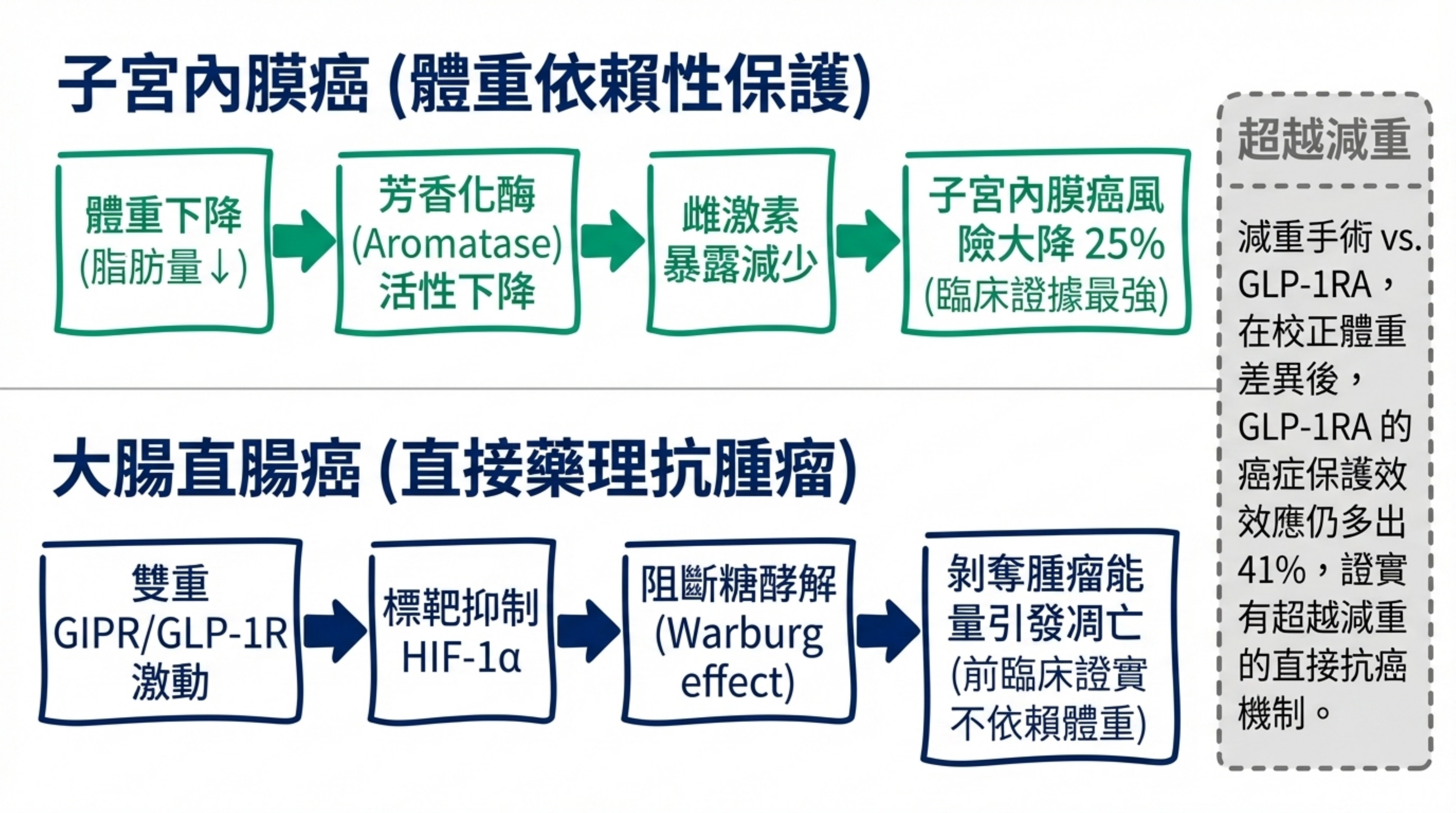
肥胖相關癌症整體(⬛ Strong): Nørgaard et al.(2024)在 >165 萬 T2DM 患者中顯示,GLP-1 RA 使用者在 10/13 肥胖相關癌症中風險降低(vs. insulin),整體癌症死亡率降 8% 18。減重本身是已確立的癌症保護因子。
3.3 GLP-1R 陽性神經內分泌腫瘤的矛盾數據

一個需要關注的例外是 GLP-1R 陽性神經內分泌腫瘤(NET)。體外研究顯示 GLP-1 RA 促進 GLP-1R+ NET 細胞增殖 19–22%,semaglutide 在異種移植瘤模型中促進腫瘤生長 72%(PMID 39665969)。然而,大型配對世代研究反而顯示 GLP-1 RA 使用與 NET 患者生存期改善相關(反映整體代謝益處)。此矛盾提示 NET 可能需要個別化評估 22。
3.4 癌症小結
現有證據不支持 tirzepatide 增加任何類型癌症風險,多個器官(子宮內膜、乳房、大腸直腸)甚至傾向保護效應。 保護機制涉及減重介導的荷爾蒙環境改善(雌激素↓)、直接抗腫瘤代謝效應(HIF-1α 抑制)和系統性抗炎作用。然而,RCT 追蹤期的根本限制使長期(>10 年)風險無法排除,需要持續的登錄研究和主動監測。
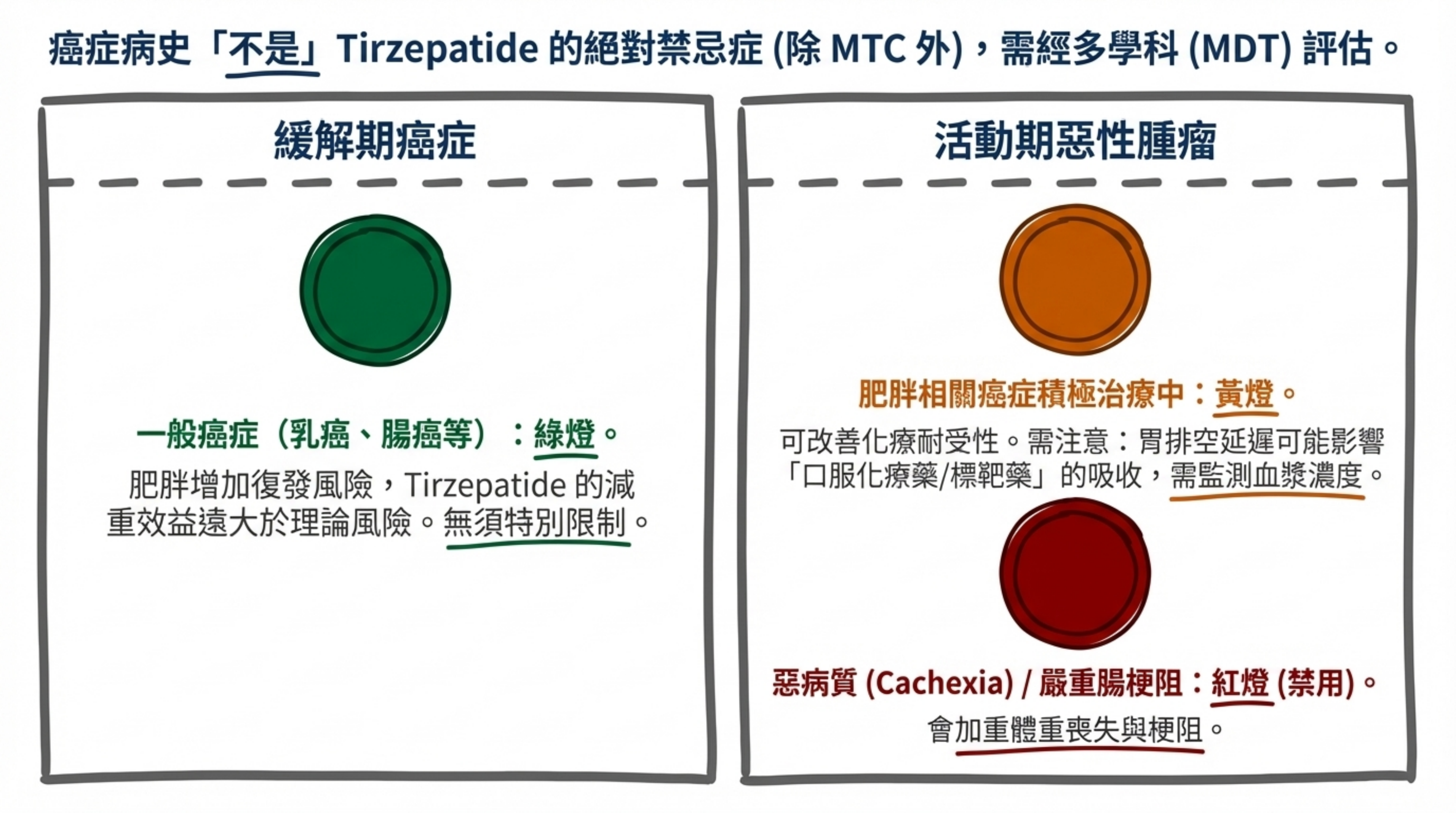
第四章:特殊族群安全性
4.1 腎功能不全(⬛/🟧)
藥物動力學: 專屬 PK 研究(N=45)確認腎功能損害(含透析)對 tirzepatide 暴露無臨床顯著影響。Tirzepatide 主要通過蛋白水解代謝(不依賴腎臟清除),t₁/₂ ≈ 5 天。各 CKD 分期無需調整劑量 23。
腎臟保護效應: SURPASS-4 事後分析顯示,tirzepatide vs. insulin glargine 的 eGFR 年下降速率差異為 +2.2 mL/min/1.73m²(p<0.001);在 eGFR <60 亞組差異更大(+3.7)。複合腎臟終點 HR=0.58(0.43–0.80),tirzepatide 顯著降低腎臟風險 42% 24。
警示: GI 副作用導致的脫水仍可引發急性腎損傷(AKI),尤其在加速劑量遞增時。CKD 患者的 GI 症狀期間需監測腎功能並考慮暫停腎毒性合併用藥。
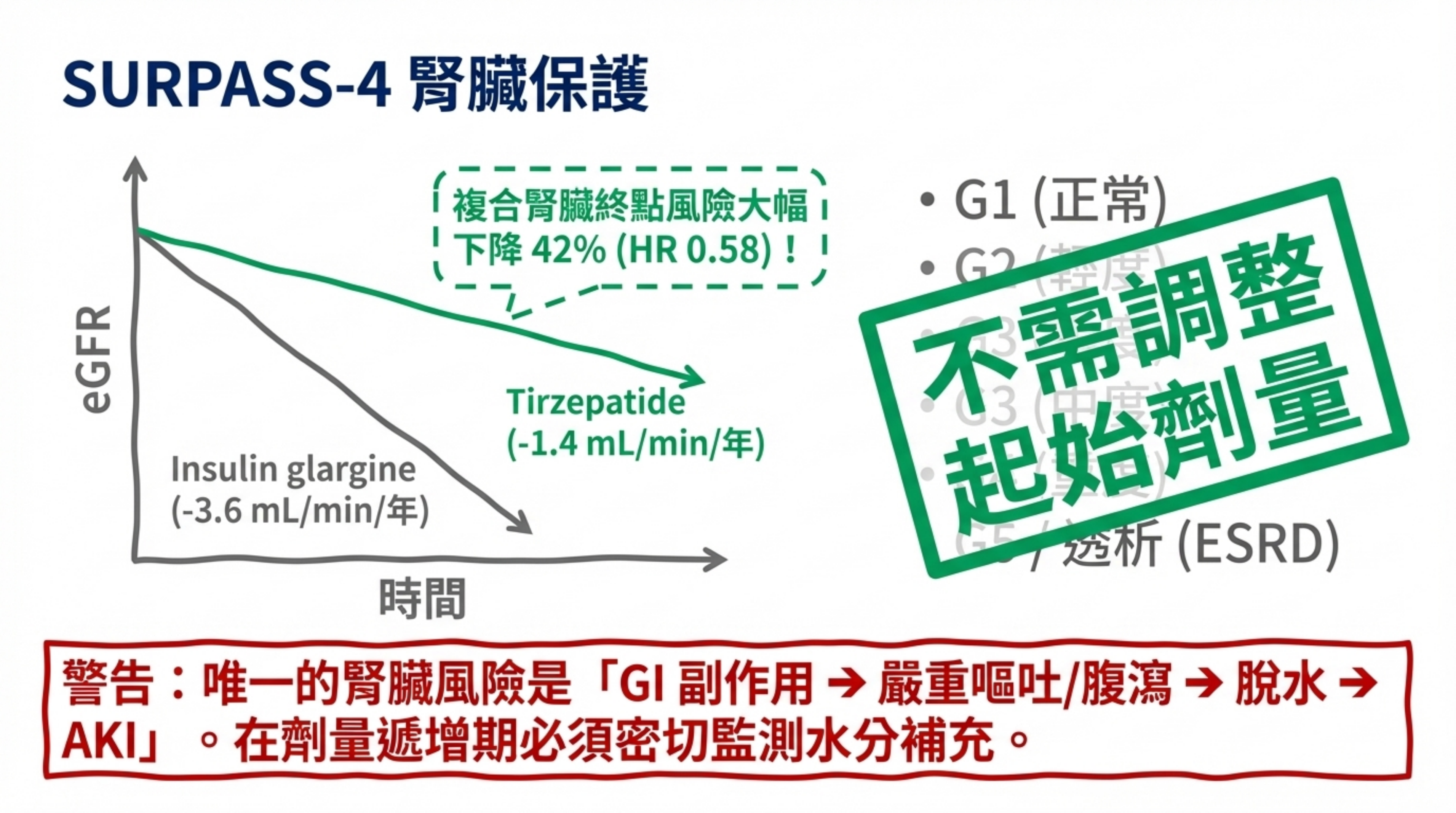
4.2 孕期與哺乳(⬜ 人類數據嚴重缺失)
孕期:禁用。 動物數據顯示在接近臨床暴露量時出現外部、內臟和骨骼畸形(可能部分源於藥理性母體體重減少)。人類孕期安全數據完全缺失 25。
停藥時機: t₁/₂ ≈ 5 天,完全洗滌需 4–5 週。FDA 建議計畫懷孕前至少停藥 1 個月(部分指南建議 2 個月更保守)25。
哺乳: 乳汁中 tirzepatide 濃度極低(<0.02% 母體劑量),且作為大分子蛋白質可能在嬰兒 GI 中被水解。LactMed 建議:若母親需要 tirzepatide,不是停止哺乳的理由 26。
重要警示——口服避孕藥交互作用: Tirzepatide 延遲胃排空可降低口服避孕藥吸收(ethinyl estradiol Cmax ↓59%,AUC ↓20%)。FDA 建議開始 tirzepatide 或每次增量後 4 週內使用非口服避孕法或加用屏障法 27。此外,體重下降可恢復 PCOS 患者的排卵功能,意外懷孕風險可能增加。

4.3 青少年(🟧 Moderate)
SURPASS-PEDS(Lancet 2025): 10–18 歲 T2DM 患者的 Phase 3 RCT 顯示 HbA1c −2.23%(vs. placebo +0.05%),BMI −7.4% 至 −11.2%,安全性與成人一致。已支持 10 歲以上 T2DM 的 Mounjaro 批准 28。
SURMOUNT-ADOLESCENTS-2(NCT06439277): 12–17 歲肥胖適應症 Phase 3 試驗進行中,尚無公開結果。
生長發育疑慮(⬜ Knowledge gap): 骨密度影響(青春期骨骼峰值累積的關鍵時期)、能量攝入減少對身高增長的影響、GLP-1R 在下丘腦-垂體軸的潛在效應等,均需長期前瞻性監測。

4.4 精神疾病族群(⬜ 數據極度缺乏)
無 RCT 直接評估 tirzepatide 在精神疾病族群的安全性。一項案例報告顯示 tirzepatide 可成功治療 clozapine 誘發的體重增加 29。回顧性數據顯示精神分裂症族群使用 tirzepatide 的自殺行為 HR=0.43(0.27–0.70),提示可能有益。但需注意 GLP-1 RA 可能影響精神科藥物的吸收(胃排空延遲效應)。
4.5 老年人 ≥65 歲(🟧 Moderate)
SURPASS 老年亞組分析: 療效維持,但 AE 相關停藥率較高(反映老年人對 GI 症狀的耐受性較差)30。SURMOUNT-1 DXA 數據顯示 ≥65 歲亞組脂肪佔體重減少的 76%(vs. 全體 74%),比例維持穩定。
特殊考量:
- 肌少症風險(Part 2.2 已詳述):基線肌肉量可能已處於功能障礙閾值附近
- 骨折風險:HR 1.44 vs. 其他 GLP-1 RA
- 建議緩慢劑量滴定 + 前置運動介入 + 骨密度評估 + 定期功能評估(SPPB、握力)

4.6 肝功能損害 / MASH(⬛/🟧)
藥物動力學: 專屬 PK 研究確認輕度至重度肝功能損害(Child-Pugh A–C)對 tirzepatide 暴露無臨床顯著影響,無需調整劑量 31。
SYNERGY-NASH(NEJM 2024): Phase 2b RCT 顯示 tirzepatide 在 MASH 患者中達到卓越的組織學改善——MASH 緩解率 44–62%(vs. placebo 10%),纖維化改善率 51–59%(vs. 30%)32。這是 tirzepatide 最有前景的肝臟適應症數據。
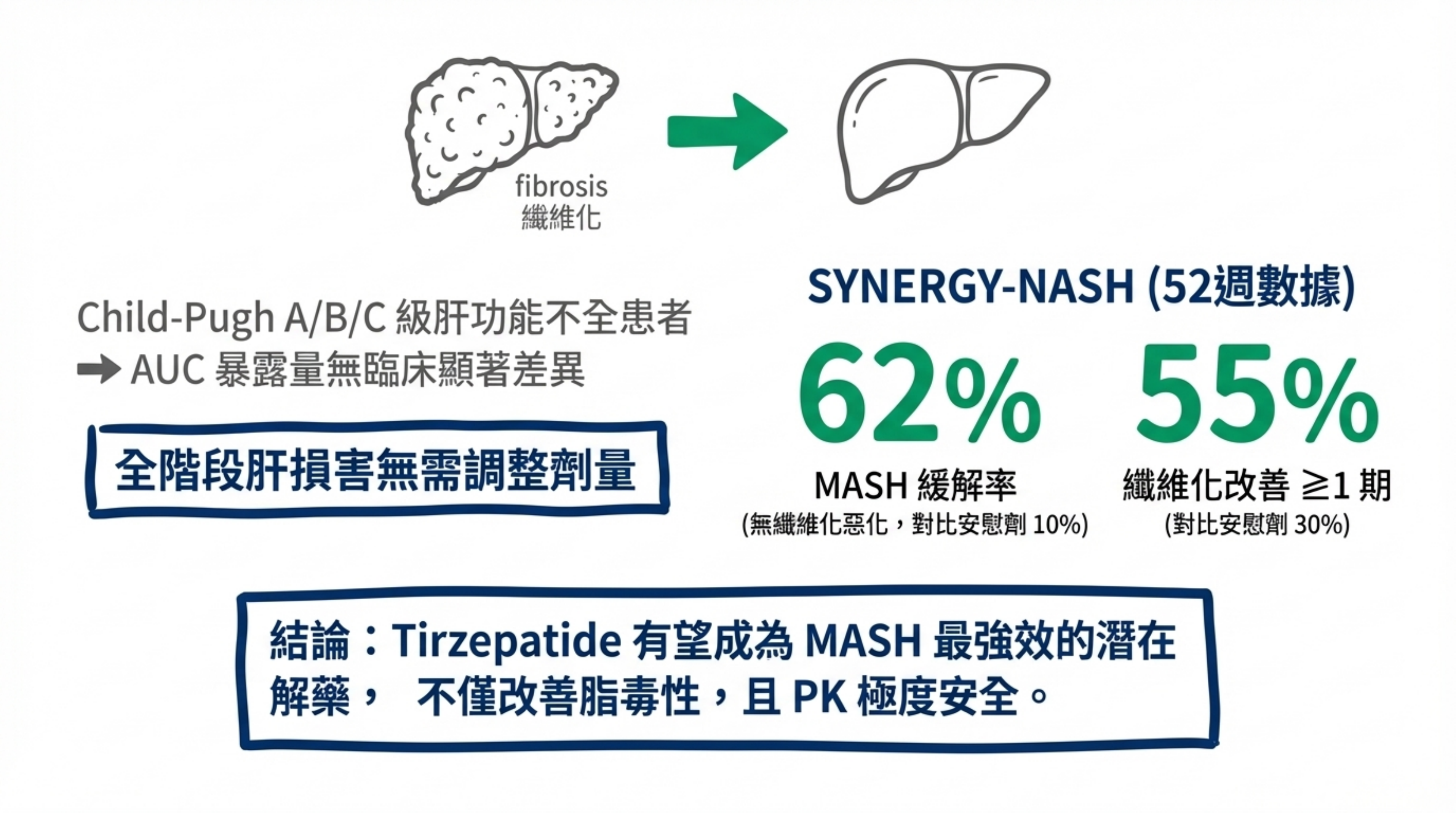
結語
歷經 Part 1–3 共 10 個研究主題、涵蓋超過 150 篇文獻的系統性分析,tirzepatide 的臨床安全性全貌可總結如下:
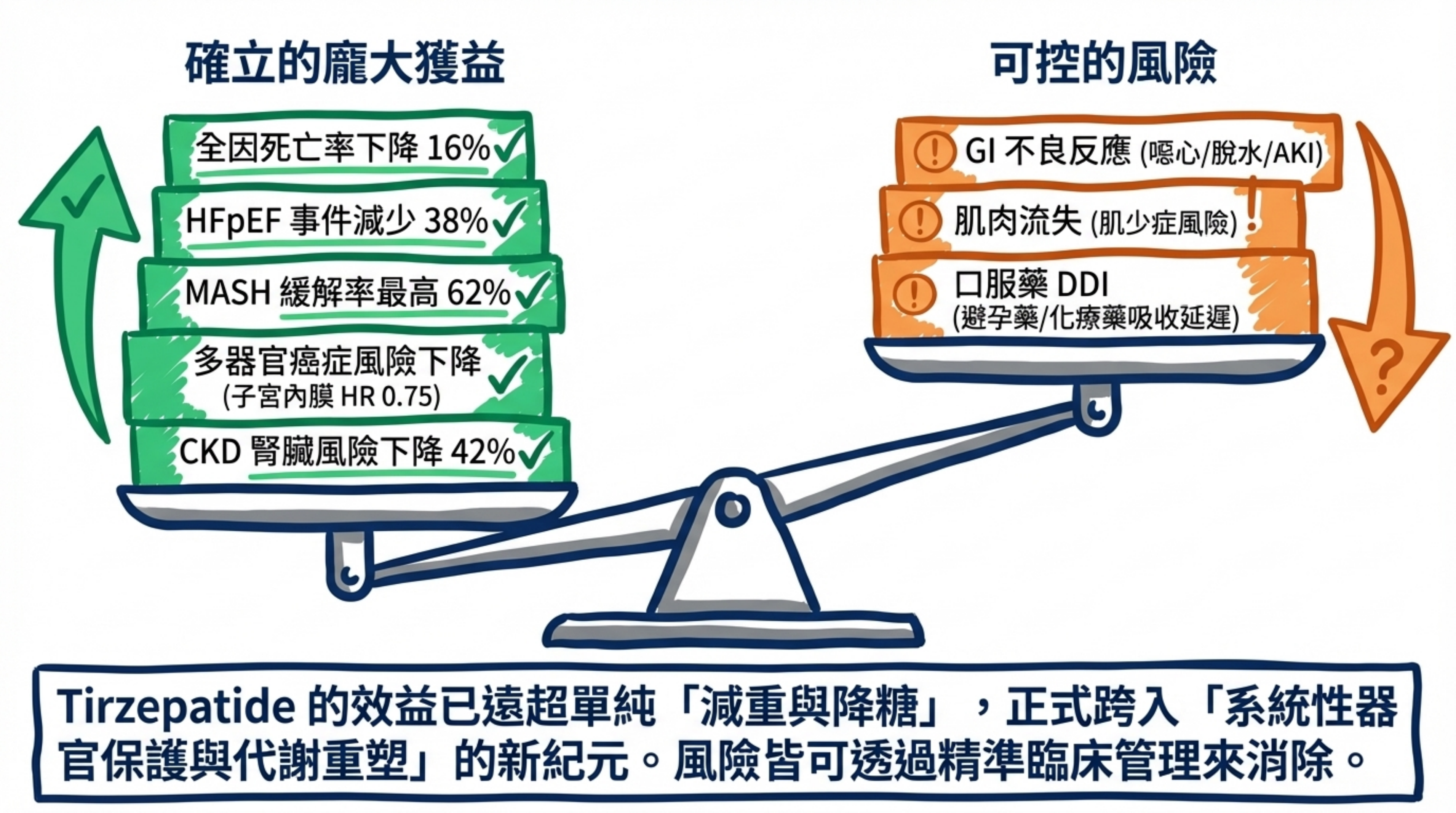
已確立的風險(可管理):
- GI 副作用:常見但多為一過性,透過劑量爬升策略可有效管理
- 膽道疾病:RR ~= 1.67,NNH ~= 149,透過篩查和 ursodiol 可部分預防
- 肌肉流失:符合生理預期,阻力訓練+蛋白質可有效保存
已排除或極低的風險:
- 精神科安全性:最高級別證據確認無因果關聯
- 甲狀腺 MTC:人類 C-cell 不表達 GLP-1R,臨床 0 例 MTC
- 急性胰臟炎:RCT 無顯著增加
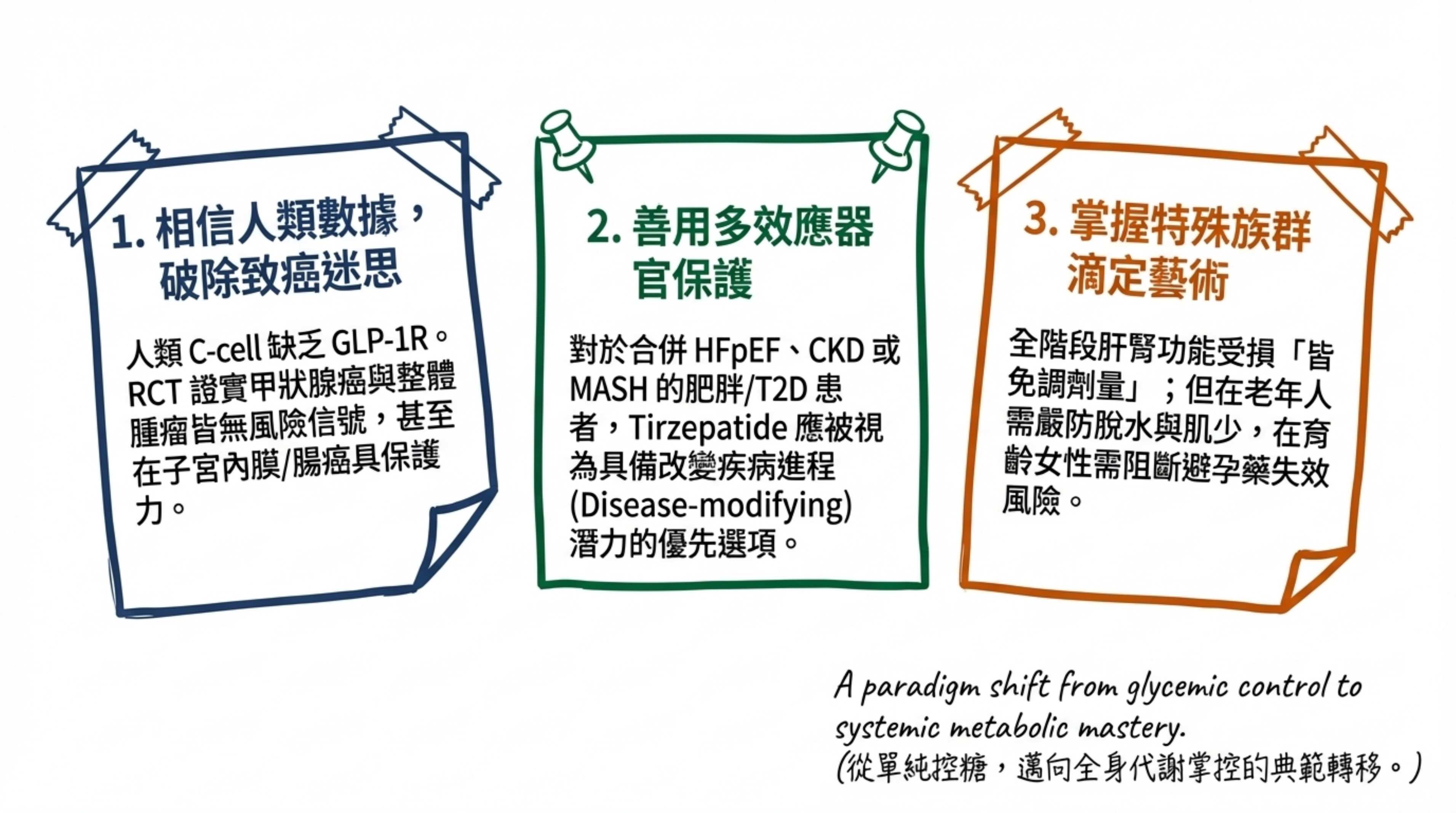
明確的獲益:
- 心血管:HFpEF 事件減少 38%,全因死亡減少 16%,SBP −7–11 mmHg
- 癌症:多器官保護傾向(子宮內膜、乳房、大腸直腸)
- 腎臟:腎臟風險降低 42%
- 肝臟:MASH 緩解 44–62%
尚待釐清的議題:
- GIP 受體的多器官獨立效應——全研究最核心的未解之謎
- 停藥後身體組成惡化
- 長期(>10 年)癌症和胰臟安全性
- 中度至重度 NPDR 患者的 DR 惡化風險管理
- 特殊族群(孕期、精神疾病、兒科長期生長發育)的充分數據
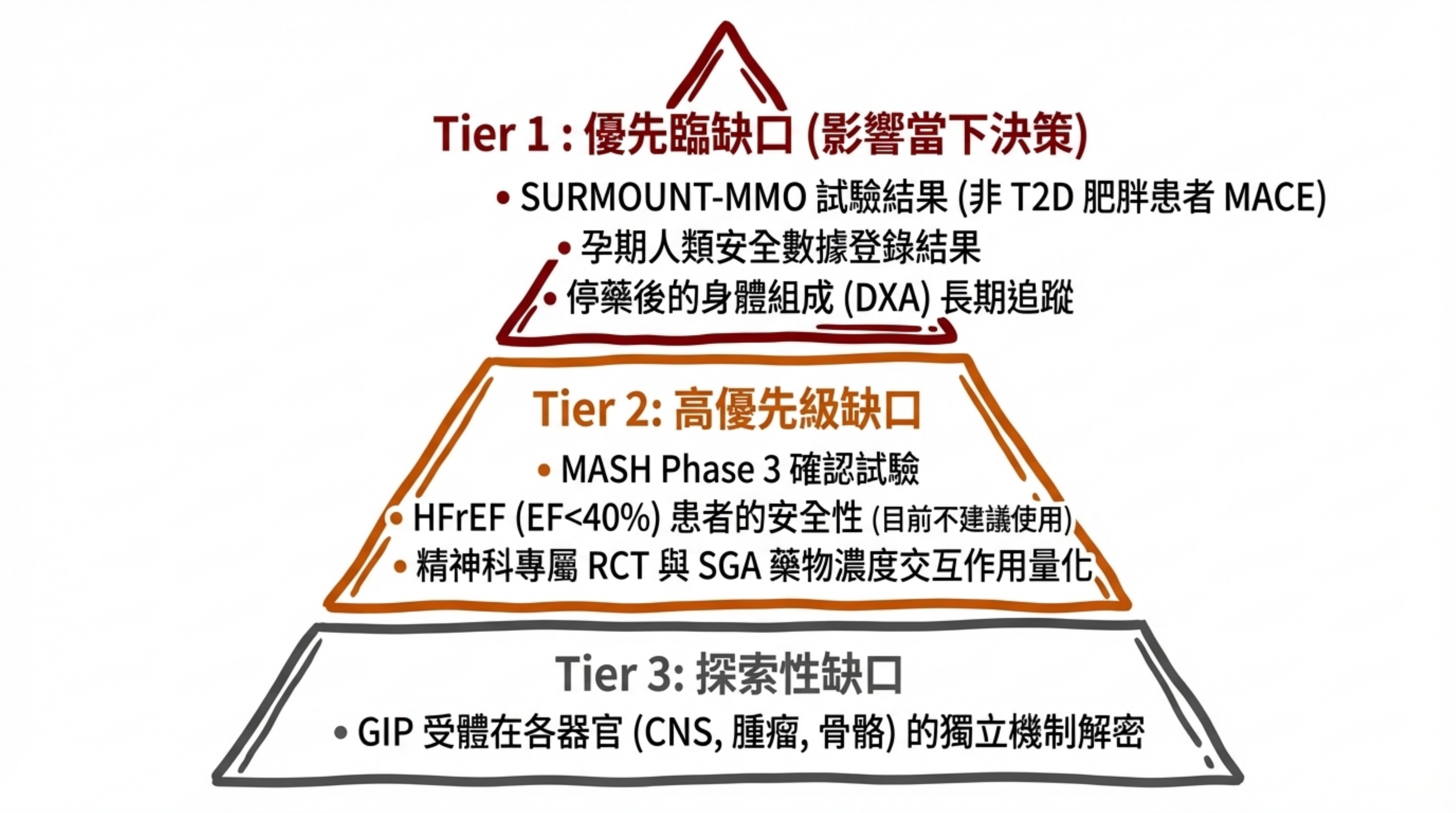
Tirzepatide 代表了代謝藥物治療的範式轉移——其卓越的療效伴隨著需要審慎管理的安全性特徵。個人化的風險評估、多學科協作照護和持續的上市後監測,是確保這一突破性治療安全造福患者的關鍵。
參考文獻
Footnotes
-
Mounjaro (tirzepatide) Prescribing Information. Eli Lilly, 2022–2025. ↩
-
Knudsen LB et al. (2010). GLP-1R agonists activate rodent thyroid C-cells. Endocrinology. PMID: 20203154. ↩
-
Boess F et al. (2013). GLP-1R effect on primary C-cells from rodent and man. J Mol Endocrinol. PMID: 23463748. ↩
-
Kim MK / Kamrul-Hasan et al. (2025). Tirzepatide cancer risk meta-analysis. Endocrinol Metab. PMID: 39814031. ↩ ↩2 ↩3
-
Silverii GA et al. (2024). GLP-1RA thyroid cancer risk RCT meta-analysis. Diabetes Obes Metab. PMID: 38018310. ↩
-
Bezin J et al. (2023). GLP-1 RA thyroid cancer French cohort. Diabetes Care. PMID: 36356111. ↩
-
Daou AZE et al. (2025). Weight-loss medications and thyroid cancer FAERS. Endocrinol Diabetes Metab. PMID: 40055991. ↩
-
Occhi et al. (2022). GIPR expression in MTC. Endocrine Abstracts 81:RC6.6. ↩
-
Changes in thyroid function with tirzepatide (2023). J Endocr Soc. PMC: 10555370. ↩
-
Packer M et al. (2025). SUMMIT trial: tirzepatide for HFpEF. N Engl J Med. PMID: 39555826. ↩
-
SUMMIT CMR substudy (2025). JACC. PMID: 39566869. ↩
-
ACC 2025 Scientific Statement: Obesity in HF. JACC. PMID: 40512113. ↩
-
SURPASS-CVOT (2025). N Engl J Med. PMID: 41406444. ↩
-
SURMOUNT-1 ABPM substudy (2024). Hypertension. PMID: 38314555. ↩ ↩2
-
SURMOUNT-1 BP stratified analyses (2024). Heart. PMID: 39084707. ↩
-
SURMOUNT-MMO design (2025). Obesity. PMID: 40545827. ↩
-
Ko A et al. (2026). GLP-1RA cancer risk 48 RCTs meta-analysis. Ann Intern Med. PMID: 41359966. ↩
-
Nørgaard CH et al. (2024). GLP-1RA and obesity-related cancer risk. JAMA Intern Med. PMID: 38967919. ↩ ↩2 ↩3
-
Bhatt AS et al. (2024). Tirzepatide shrinks endometrial cancer. Gynecol Oncol. PMID: 39388742. ↩
-
Zhang Y et al. (2025). Tirzepatide inhibits CRC via HIF-1α. Advanced Science. PMID: 40125821. ↩
-
GLP-1R agonist and NET proliferation (2025). Surgery. PMID: 39665969. ↩
-
Urva S et al. (2021). Tirzepatide renal impairment PK. PMID: 33778934. ↩
-
Heerspink HJL et al. (2022). SURPASS-4 renal post hoc. PMID: 36152639. ↩
-
LactMed Tirzepatide entry. NBK581488. ↩
-
Oral contraceptive DDI study. PMID: 37940101. ↩
-
SURPASS-PEDS (2025). Lancet. PMID: 40975112. ↩
-
Tirzepatide for clozapine-induced weight gain (2025). PMID: 40650875. ↩
-
SURPASS elderly post hoc (2025). Diabetes Therapy. PMC: 11925828. ↩
-
Tirzepatide hepatic impairment PK (2022). PMID: 35674880. ↩
-
SYNERGY-NASH (2024). N Engl J Med. PMID: 38856224. ↩