 Aldosterone 分泌的「最後一哩路」——也就是 細胞內鈣離子(Ca++)濃度的上升。無論上游是 Ang II 還是血鉀濃度,最終都是殊途同歸,透過鈣離子來啟動 的轉錄。
Aldosterone 分泌的「最後一哩路」——也就是 細胞內鈣離子(Ca++)濃度的上升。無論上游是 Ang II 還是血鉀濃度,最終都是殊途同歸,透過鈣離子來啟動 的轉錄。
這也是為什麼學界常說:「Aldosterone 的分泌機制,本質上是一個鈣離子訊號的遊戲。」
拆解 突變 這個在亞洲人(特別是台灣)最常見的致病機轉。這能完美解釋為什麼這些腺瘤可以「不甩」正常的生理回饋機制。
核心問題
「當原本負責維持『冷靜』(過極化)的鉀通道叛變,開始放任鈉離子闖入時,如何引發一連串不可逆的鈣離子訊號與 Aldosterone 狂瀉?」
邏輯拆解:從離子通道到基因轉錄
突變的機制,就是一個「細胞膜電位失控」的故事。請依序跟隨這個因果鏈:
- 正常狀態 (The Guard):
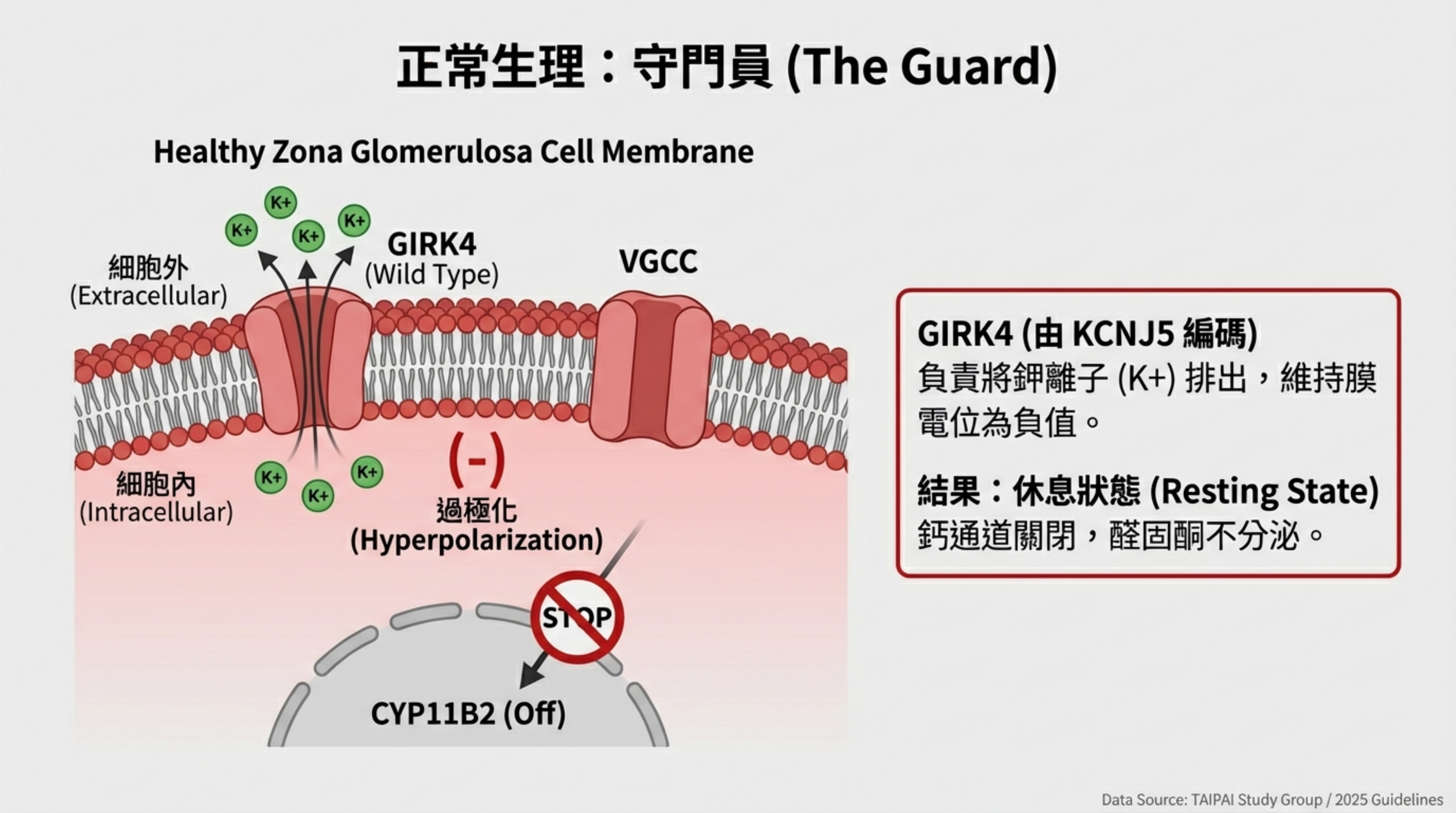
- 編碼的是 GIRK4 (G-protein-activated Inward Rectifier Potassium channel 4)。
- 它的正常職責是讓鉀離子 (K+) 流出細胞(或維持通透性),使細胞膜內電位保持在 負值 (Hyperpolarization),也就是讓細胞處於「休息、冷靜」的狀態,關閉電壓依賴性鈣通道 (VGCC)。
- 突變發生 (The Betrayal):
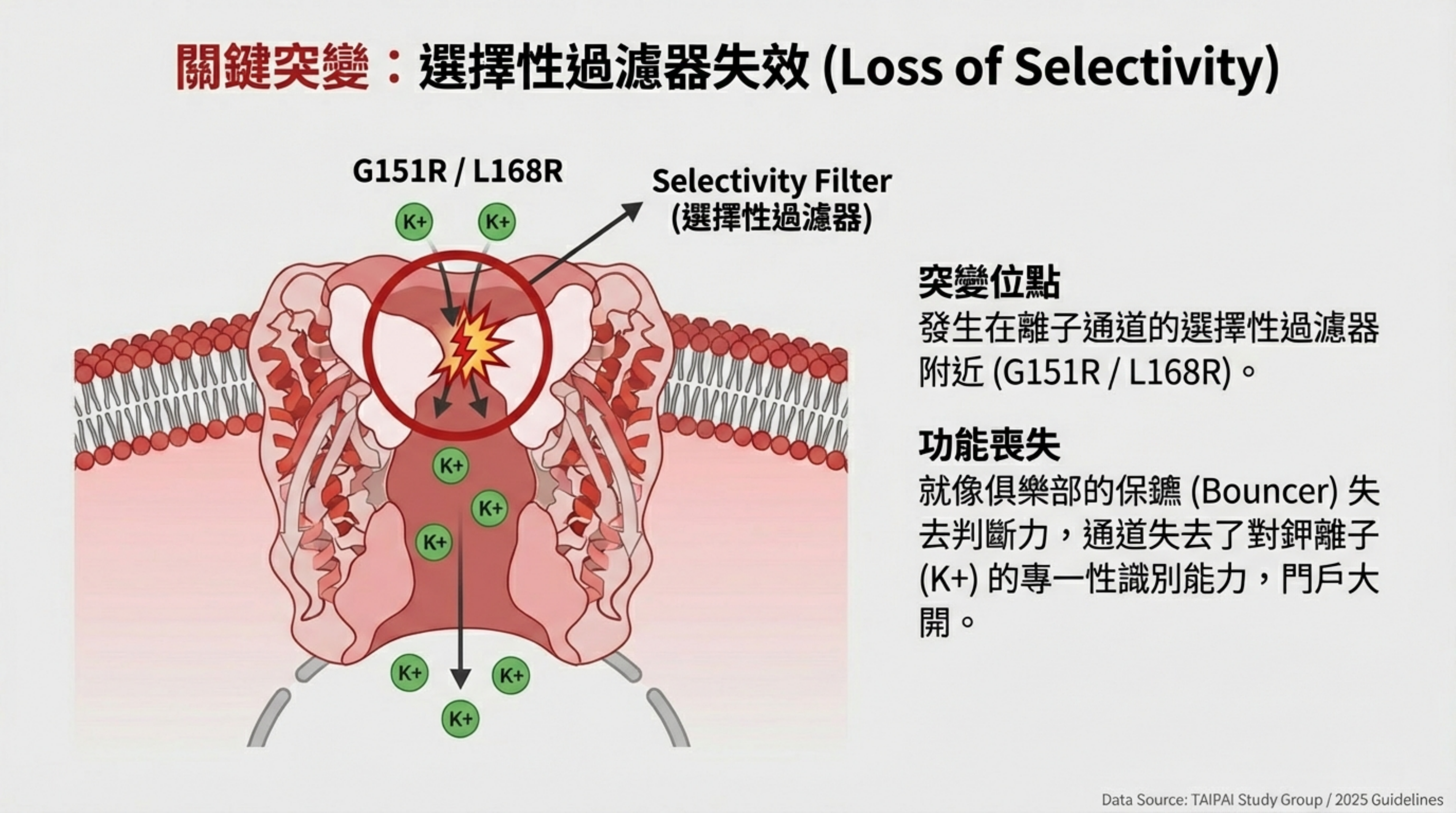
- 突變通常發生在離子通道的 選擇性過濾器 (Selectivity Filter) 附近(如 G151R 或 L168R 位點)。
- 這導致通道「變笨了」,失去了對鉀離子的專一性。
- 鈉離子入侵 (The Invasion):
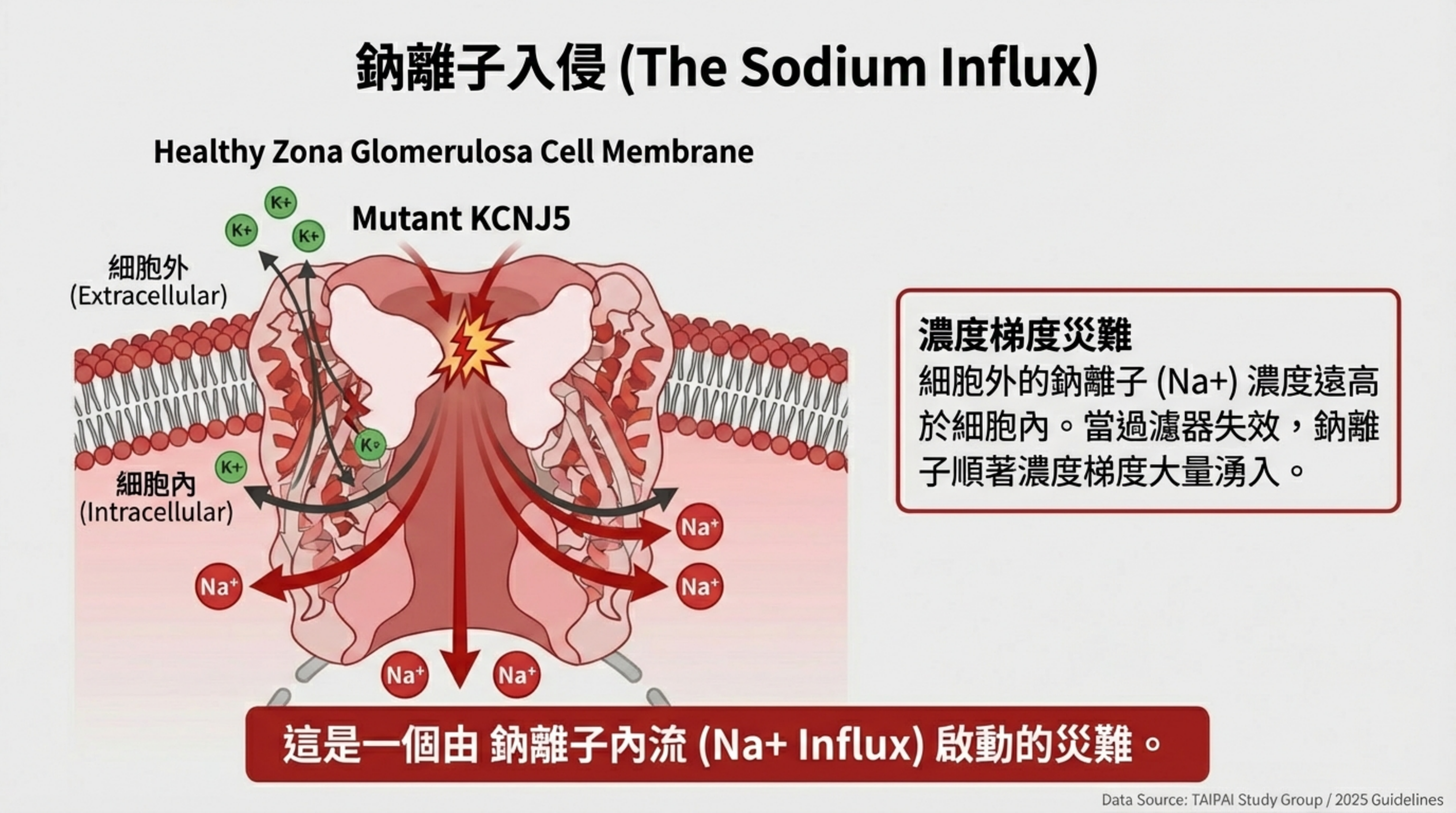
- 因為細胞外的鈉離子濃度 (Na+) 遠高於細胞內,一旦通道失去選擇性, 就會順著濃度梯度 大量湧入 細胞內。
- 去極化與鈣湧入 (The Explosion):
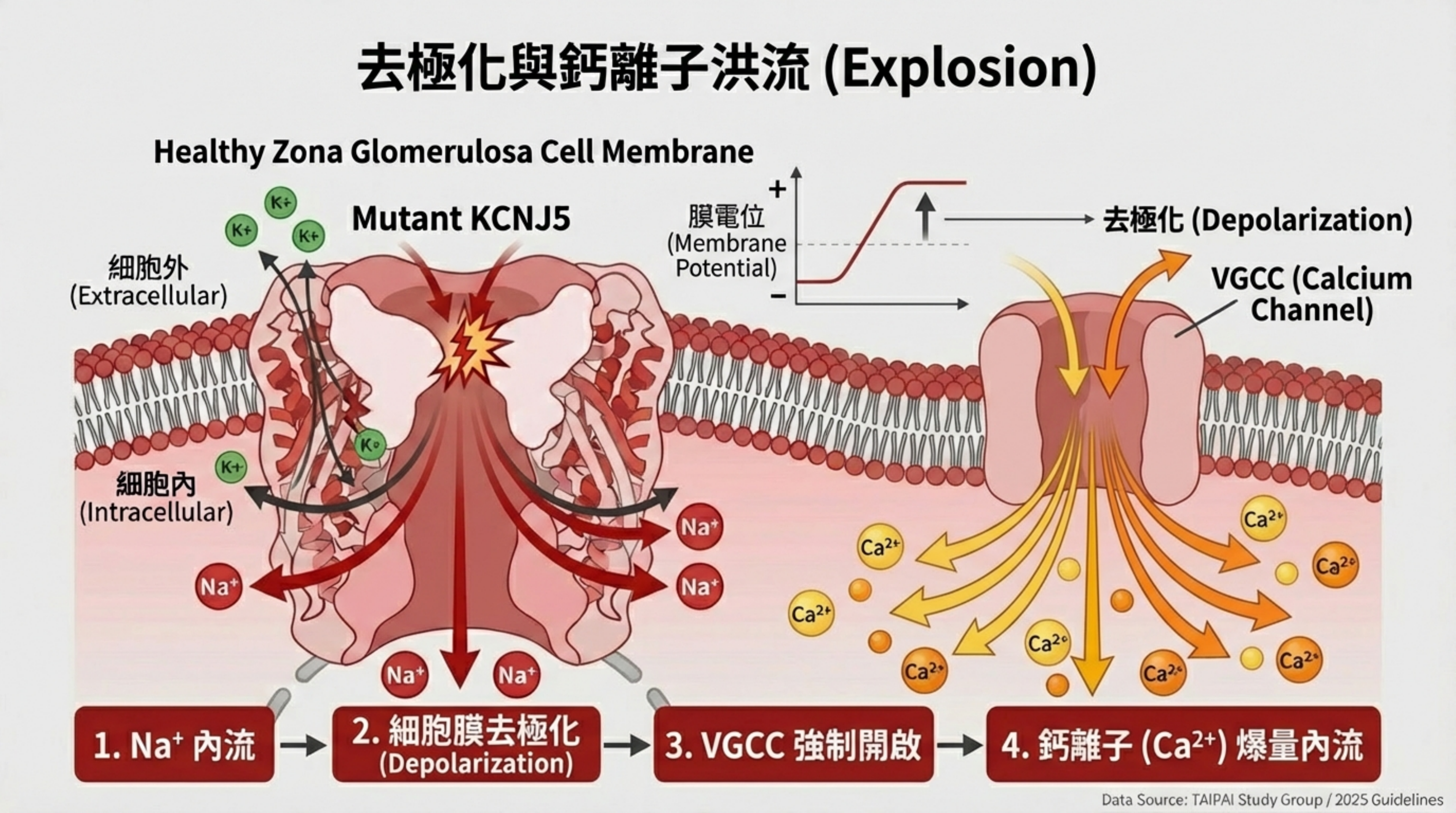
- 帶正電,大量湧入導致膜電位上升(去極化, Depolarization)。
- 這直接 強制開啟 你剛才提到的 電壓依賴性鈣離子通道 (VGCC)。
- 結果: 即使沒有 Ang II 或高血鉀的刺激,鈣離子也持續不斷地湧入細胞。
- Aldosterone 合成 (The Product):
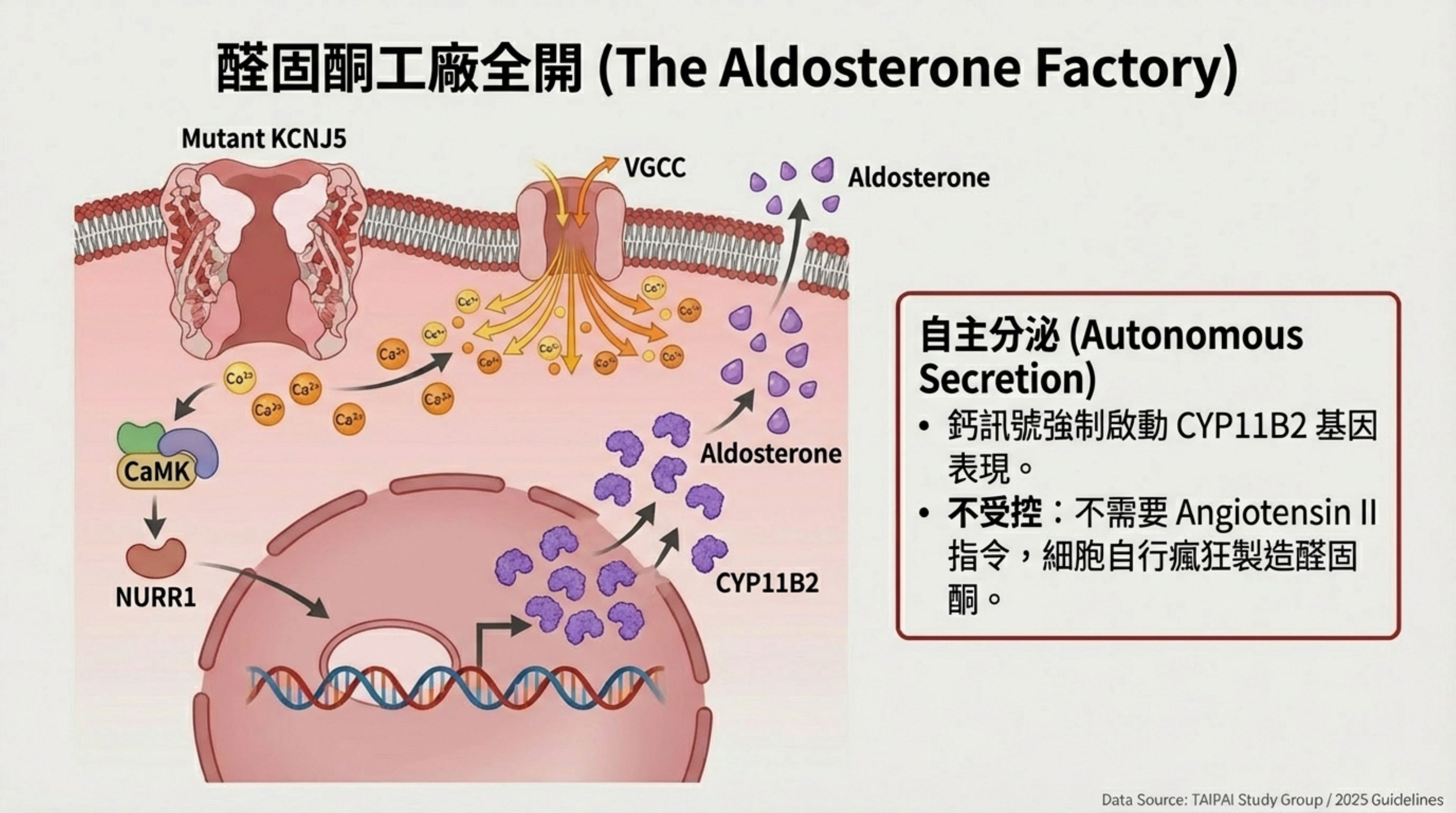
- 持續的高鈣訊號 → 活化 CaMK → 啟動 NURR1 持續轉錄 → Aldosterone 大量製造。
為什麼這樣想是合理的(學術佐證)
這個機制在 2011 年由 Choi et al. (Science) 首次發表,是 PA 研究的里程碑 。
-
生理證據: 在細胞實驗中,如果我們將突變的 基因轉染進去,會觀察到細胞膜電位顯著上升(去極化),且醛固酮分泌量大增。
-
藥理證據: 如果使用鈣離子通道阻斷劑 (CCB) 處理這些細胞,醛固酮的分泌就會被抑制。這證明了 突變確實是透過「鈣離子通道」這條路徑來發揮作用的 。
-
病理特徵: 這也解釋了為什麼 突變的腺瘤通常 染色極強,且血中 Aldosterone 濃度通常較高,因為它的鈣離子訊號是持續且強烈的 。
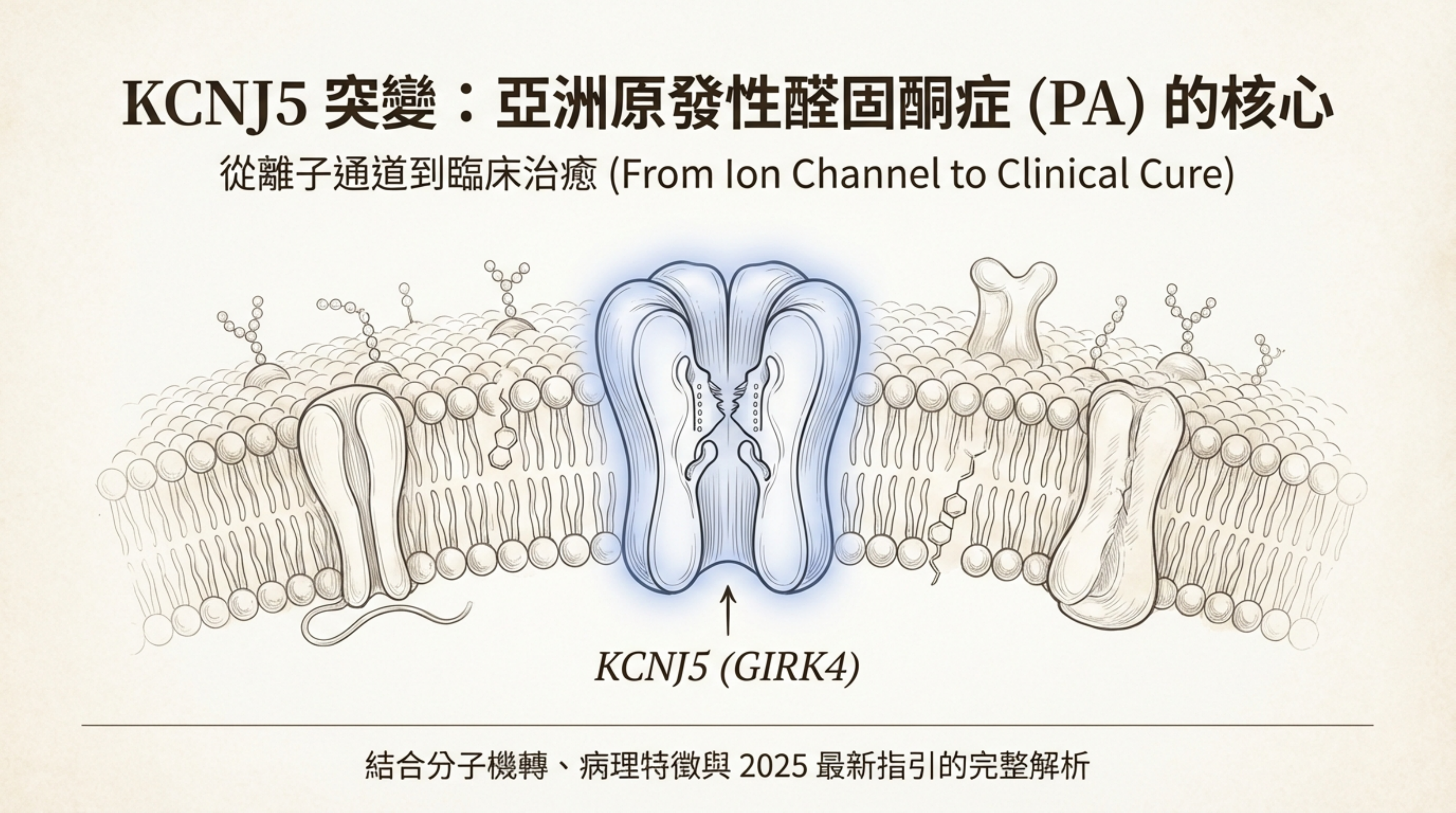
KCNJ5 突變:亞洲原發性醛固酮症 (PA) 的核心
針對 KCNJ5 突變 (GIRK4 通道病變) ,整合了分子生物機轉、臨床表型、病理特徵以及診斷意涵。
1. 基本定義與流行病學
- 基因與蛋白:KCNJ5 基因編碼 GIRK4 (G-protein-activated Inward Rectifier Potassium channel 4) 蛋白,這是腎上腺皮質細胞膜上負責維持靜止膜電位的關鍵鉀離子通道 。
盛行率:
-
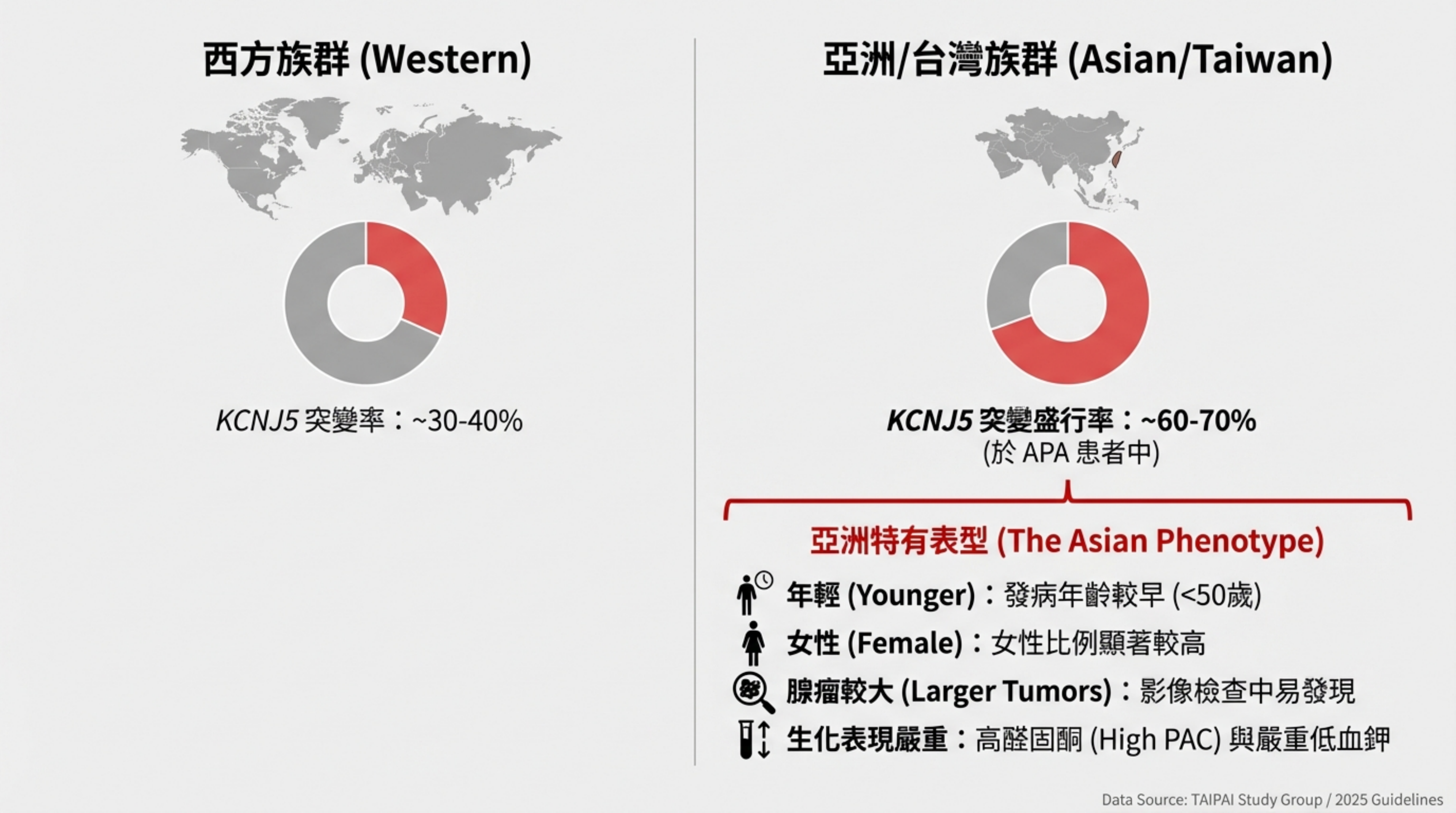
亞洲 (含台灣):這是最常見的體細胞突變 (Somatic Mutation),盛行率極高,約佔所有醛固酮腺瘤 (APA) 的 60% - 70% 。
-
西方國家:盛行率較低,約佔 30% - 40%
-
好發族群:典型表現為 年輕女性,且腺瘤體積通常較大 。
2. 分子致病機轉 (Molecular Pathogenesis)
這是理解該疾病的核心邏輯。
正常生理 (Normal Physiology):
- GIRK4 通道負責讓鉀離子 (K+) 流出或維持通透性,使細胞保持 過極化 (Hyperpolarization) 的狀態。
- 這種負電位狀態會關閉電壓依賴性鈣離子通道 (VGCC),阻止鈣離子內流,使細胞處於「休息」狀態 。
突變效應 (Loss of Selectivity):
- 突變點位通常發生在離子通道的 選擇性過濾器 (Selectivity Filter) 附近(最常見為 G151R 或 L168R)。
後果:通道失去對 的專一性,變成非特異性的陽離子通道,允許細胞外高濃度的 鈉離子 (Na+) 大量湧入 。
連鎖反應 (The Cascade):
-
去極化 (Depolarization): 內流導致膜電位上升 。
-
鈣離子通道開啟:去極化直接打開電壓依賴性鈣離子通道 (VGCC) 。
-
鈣訊號活化:細胞內鈣離子濃度 (Ca++) 持續升高,活化 CaMK 路徑 。
-
基因轉錄:啟動 NURR1 等轉錄因子,強制驅動 (Aldosterone Synthase) 的大量表現與醛固酮合成 。
3. 病理組織學特徵 (Histopathology)
KCNJ5 突變的腺瘤在顯微鏡下有非常獨特的外觀,這與其細胞來源和代謝特性有關。
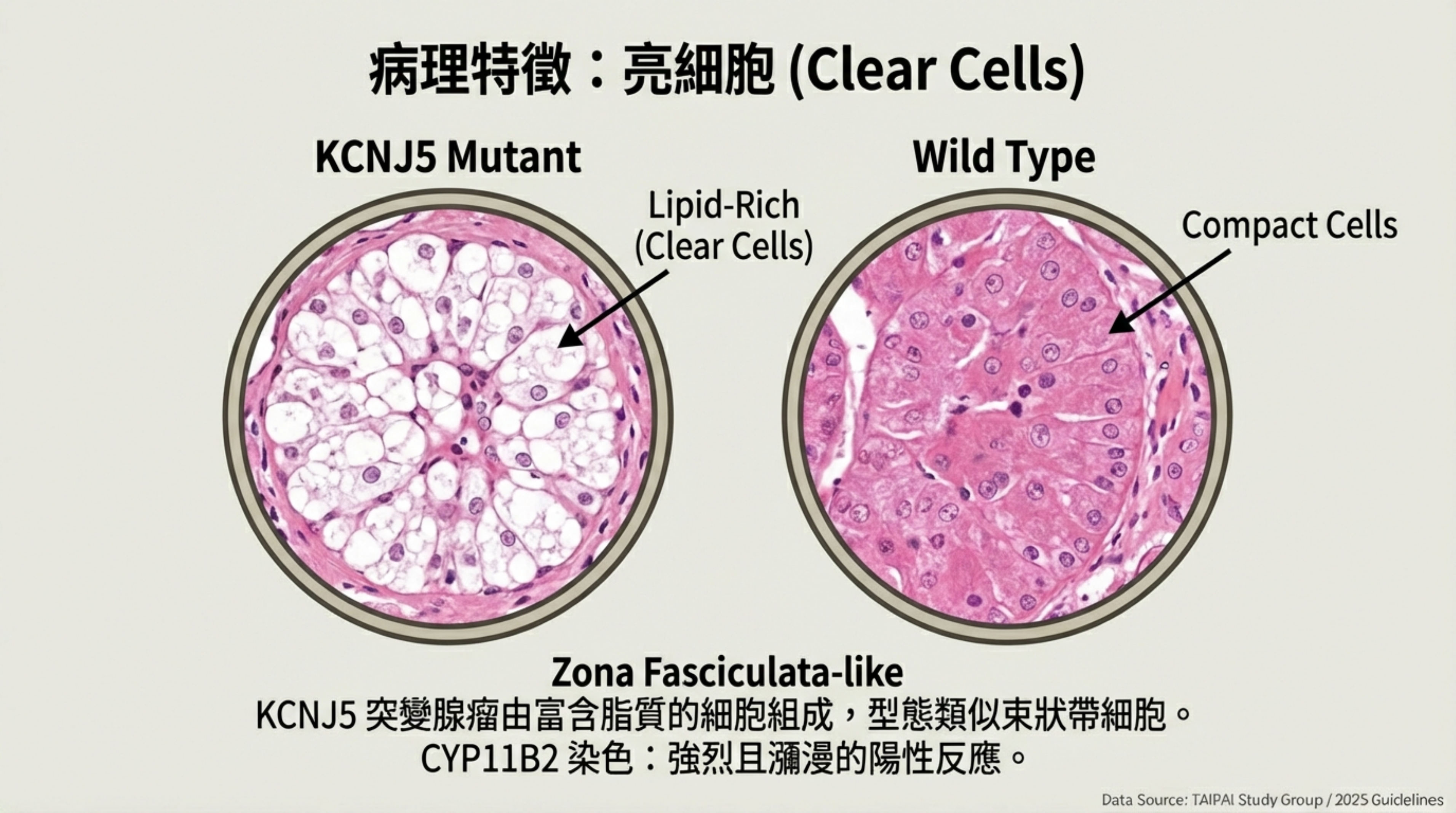
- 細胞型態:主要由 Clear cells (亮細胞/富含脂質) 組成,型態類似腎上腺皮質的束狀帶 (Zona Fasciculata-like cells) 。這與 ATP1A1 或 CACNA1D 突變常見的 Compact cells (緻密細胞) 不同 。
-
免疫染色:
-
CYP11B2 (Aldosterone Synthase):染色強烈,證實其為醛固酮的主要來源 。
-
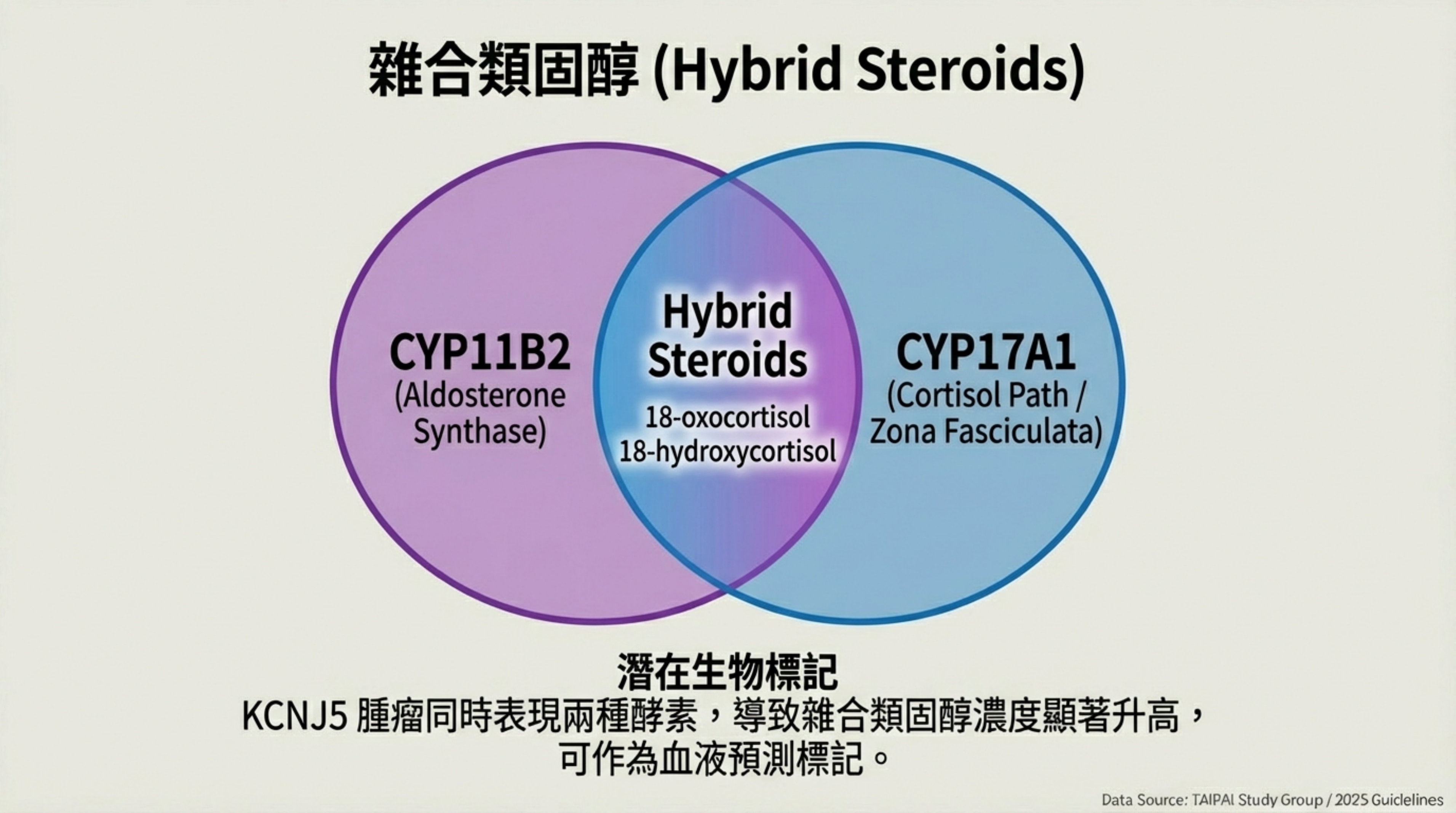
CYP17A1 & CYP11B1:這些通常只在束狀帶 (ZF) 表現的酵素,在 KCNJ5 突變腺瘤中也常呈現陽性 。這解釋了為何這類腺瘤能合成「雜合類固醇」(Hybrid Steroids)。
4. 臨床診斷特徵與生化表現
KCNJ5 突變賦予了腫瘤「自主性」,這直接影響了臨床檢驗的結果。
-
疾病嚴重度:通常表現為較嚴重的 PA,包括較高的血漿醛固酮濃度 (PAC) 和較嚴重的低血鉀 (Hypokalemia) 。
-
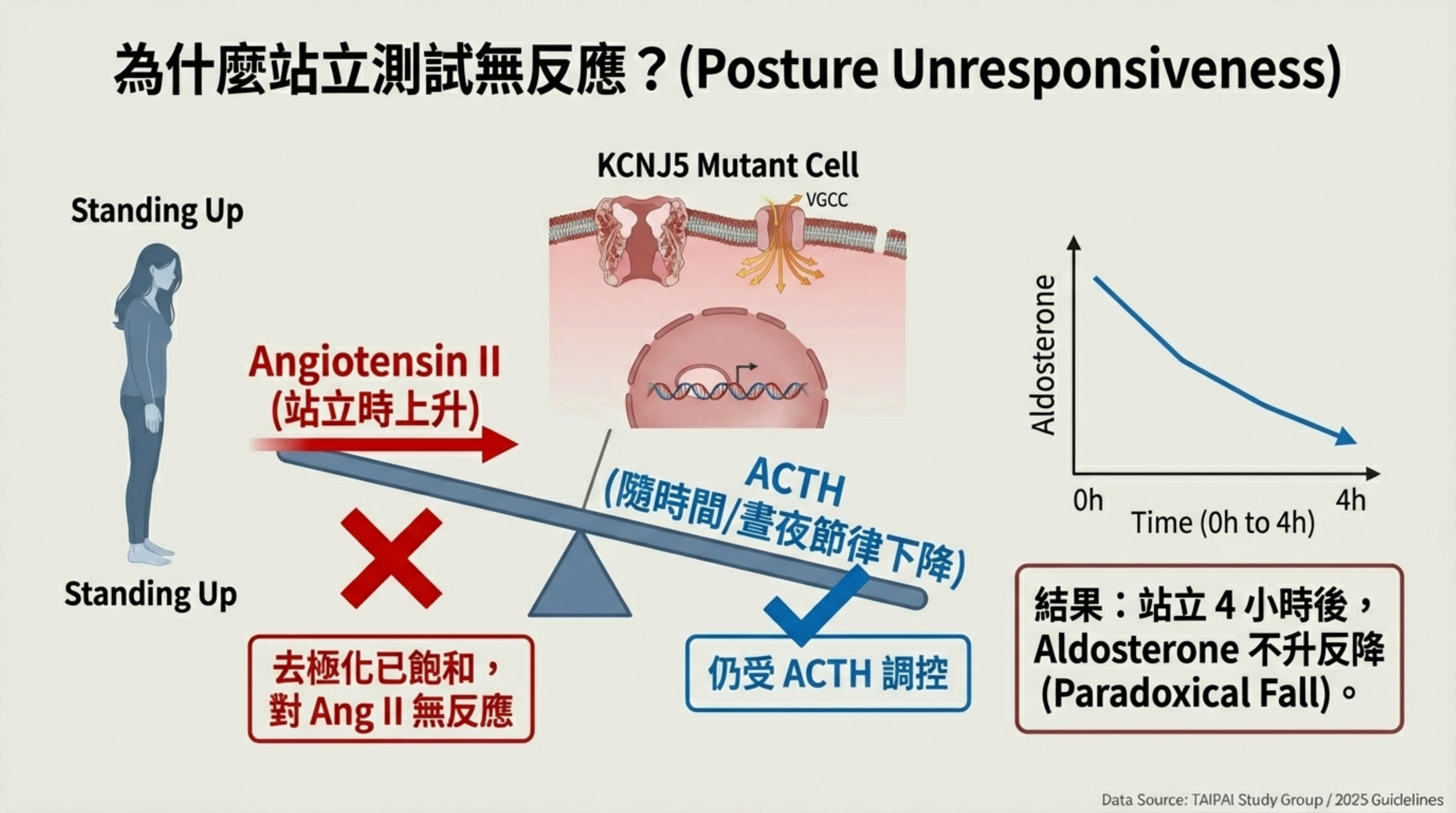
姿勢測試 (Posture Stimulation Test):
-
反應:無反應 (Unresponsive) 或 矛盾下降。
-
原因:因為細胞已經處於持續去極化的強直狀態,對外源性的 Angiotensin II (站立時產生) 已不再敏感。此時醛固酮的分泌反而受 ACTH 的晝夜節律影響(早上高、下午低),因此站立 4 小時後數值反而下降
- 特殊生化標記 (Hybrid Steroids):
- 由於同時表現 CYP11B2 和 CYP17A1,這類腺瘤會分泌大量的 18-oxocortisol 和 18-hydroxycortisol 。這在未來可能成為不需侵入性檢查就能預測突變型態的血液標記。
5. 治療與預後 (Prognosis)
-
手術預後佳:雖然 KCNJ5 突變導致較嚴重的生化異常,但也因為它多半形成 單側、明顯的大腺瘤 (Adenoma),手術切除後,高血壓與生化異常的 緩解率 (Clinical & Biochemical Success) 通常較好 。
-
藥物反應:對於不開刀的病人,MRA (如 Spironolactone) 仍是標準治療。亦有研究指出 Macrolide 類抗生素可能對突變通道有抑制作用,但尚未進入臨床應用 。
總結:KCNJ5 突變的「速記口訣」
為了方便記憶,您可以將 KCNJ5 突變聯想為一個 「年輕、激動、卻又固執的亞洲女性」:
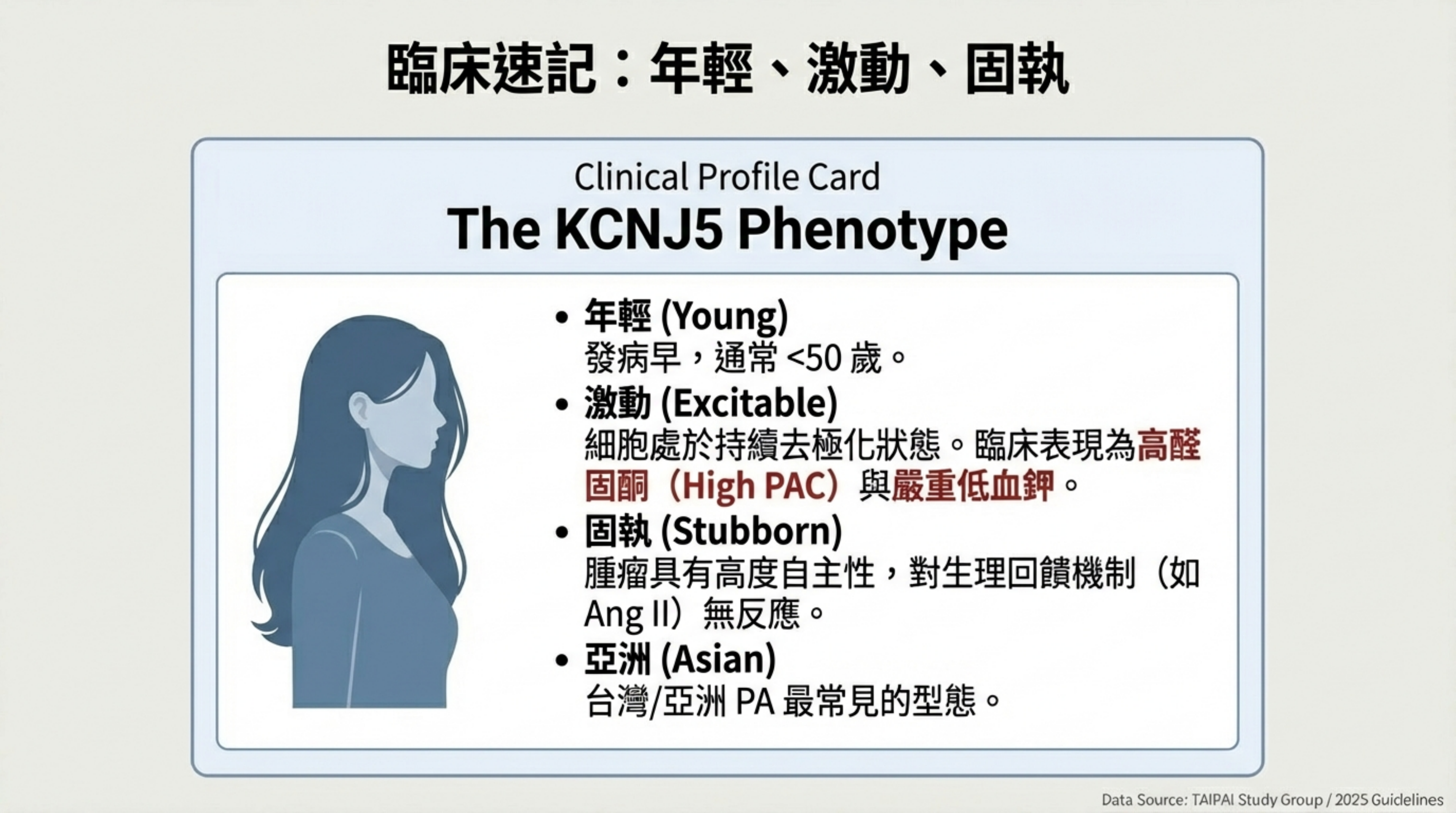
- 年輕女性 (Young female) 多見。
- 激動 (Excitable):離子通道漏電,鈉鈣內流,細胞持續去極化興奮。
- 固執 (Autonomous):不甩 Angiotensin II 的指揮(姿勢測試無反應)。
- 亞洲 (Asia):亞洲人最常見。
- 亮細胞 (Clear cell):病理下細胞質亮亮的(富含脂質)。
PA 診斷與病理生理學中最細膩的觀念之一。
KCNJ5 突變 導致的細胞生理特性有直接且深刻的關係,導致躺和坐在測量上的巨大差異。
將這個問題拆解成兩個層次:
- 為什麼做確診試驗(如 Saline Infusion Test, SIT)時,現在建議「坐著」做而非「躺著」做?
- 為什麼做分型診斷(Posture Stimulation Test)時,KCNJ5 突變會導致數值「不升反降」?
1. 姿勢對「確診」的影響:坐著做 SIT (Seated SIT) 的革命
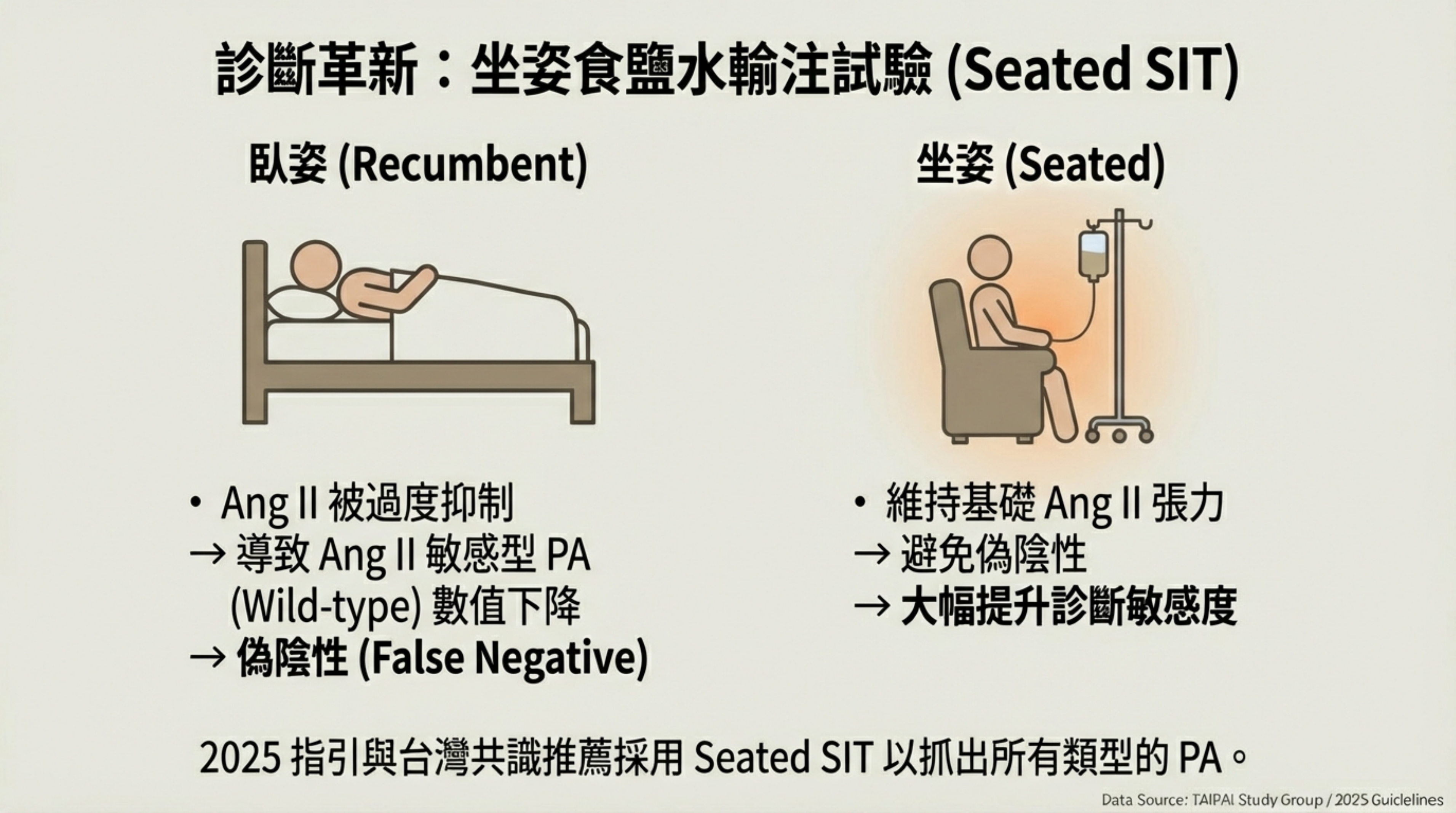
在 2025 年的新指引以及台灣的共識中,非常強調生理食鹽水輸注試驗(SIT)建議改為 坐姿 (Seated) 進行,而非傳統的 臥姿 (Recumbent)。
邏輯拆解
- 躺著 (Recumbent):回心血量增加 → 腎臟血流充沛 → Renin 與 Angiotensin II (Ang II) 被生理性抑制到最低。
- 風險:對於那些 Ang II-Responsive(對血管張力素敏感) 的 PA 病人(通常是 Wild-type 或 Hyperplasia),因為 Ang II 降得太低,導致 Aldosterone 也跟著下降。
結果:Aldosterone 被「假性抑制」了,你看起來以為他是正常的(偽陰性,False Negative) 。
- 坐著 (Seated):地心引力讓血液積在下肢 → 腎臟感受到一點壓力 → 維持一定的 Renin 與 Angiotensin II 基礎濃度。
- 優勢:這個基礎的 Ang II 濃度,足以讓那些 Ang II-Responsive 的 PA 病人持續分泌 Aldosterone,不會被食鹽水壓下去。但對於正常人來說,食鹽水的體液擴充效果仍足以抑制 Aldosterone。
- 結果:大幅提高了診斷的 敏感度 (Sensitivity),抓出更多輕微或 Ang II 敏感型的 PA 。
2. KCNJ5 突變與姿勢測試 (Posture Stimulation Test)
問題的核心:「KCNJ5 突變是否造成了差異?」 是的。這也是為什麼早期的文獻會用「姿勢測試」來區分是 腺瘤 (Adenoma) 還是 增生 (Hyperplasia),但後來發現這其實是在區分 Ang II 不敏感 (Unresponsive) 與 Ang II 敏感 (Responsive) 的亞型。
機制對決:Ang II vs. ACTH
當一個病人早上 8 點起床站立到中午 12 點(站立 4 小時),體內會有兩股力量在拉扯:
- 站立壓力:Renin↑ → Ang II ↑ (這股力量叫 Aldosterone 上升)。
- 生理時鐘:早上 8 點是 Cortisol 高峰,中午 12 點 ACTH↓ (這股力量叫 Aldosterone 下降)。
KCNJ5 突變的反應 (The Unresponsive Type)
-
病理狀態:如我們上一輪所說,KCNJ5 突變導致鈉離子持續內流,細胞膜已經處於「強直去極化」狀態,鈣通道全開。
-
對 Ang II 的反應:細胞已經「極度興奮」了,外來的 Ang II 訊號對它來說微不足道(或是受體表現量低),它對 Ang II 「無感」 。
-
對 ACTH 的反應:它仍然保留對 ACTH 的敏感性。
-
臨床結果:站立 4 小時後,Ang II 雖然上升但叫不動它;反而是隨著時間接近中午,ACTH 濃度自然下降,導致 Aldosterone 跟著 下降(Paradoxical drop)。
-
這就是典型 KCNJ5 突變大腺瘤的表現。
Wild Type 或 增生 (The Responsive Type)
- 病理狀態:沒有離子通道漏電,細胞膜電位相對正常。
- 對 Ang II 的反應:非常敏感。
- 臨床結果:站立後,Ang II 的上升訊號 強過 ACTH 下降的訊號,導致 Aldosterone 上升 。
為什麼這樣想是合理的(文獻證據)
-
細胞學證據:研究證實,KCNJ5 突變的細胞,其 CYP11B2 的表現與 Ang II 的連結脫鉤,轉而更依賴細胞內的鈣離子濃度與 ACTH 訊號。同時這類腫瘤常表現 CYP17A1,這通常是束狀帶(受 ACTH 控制)的特徵 。
-
臨床研究:在 Tunny 等人的經典研究中,將 PA 分為「姿勢反應型」與「姿勢無反應型」。後來的基因定序研究證實,「姿勢無反應型」高度對應到 KCNJ5 突變 。
如果今天有一個 PA 病人,他的 CT 影像看起來雙側腎上腺都正常(沒有明顯腫瘤),但他在做「站立姿勢測試」時,Aldosterone 數值從早上的 25 ng/dL 劇烈上升 到 45 ng/dL。
- 根據剛剛的邏輯,這比較像是哪一種基因型態(KCNJ5 mutant 還是 Wild type/Hyperplasia)?
- 既然影像看起來正常,但生化反應這麼強烈,這是否暗示他可能是適合開刀的對象,還是更偏向藥物治療?(提示:思考 "Ang II Responsive" 通常對應到的病理型態是單顆大瘤還是瀰漫性小結節?)
核心結論:
「Aldosterone 隨站立劇烈上升 → 代表 Ang II Responsive → 暗示 Wild-type 或 Hyperplasia 偏向藥物治療。」
這條邏輯鏈是 PA 分型診斷的黃金法則之一(雖然現代多用 AVS 取代,但觀念依然適用)。
邏輯拆解與學術驗證
1. 基因與生理 (The Driver)
-
KCNJ5 Mutant:
-
狀態:細胞膜因為鈉離子持續內流,處於 「強直去極化 (Constitutive Depolarization)」。
-
反應:電壓開關「卡在開的位置」,鈣離子持續湧入。外來的 Ang II 訊號對它來說是「多餘的」。
-
表現:Unresponsive(隨 ACTH 下降而下降)。
-
Wild-type / Hyperplasia:
-
狀態:離子通道功能正常,細胞膜電位處於 「可調控」 狀態。
-
反應:站立時 Renin 上升產生 Ang II,Ang II 成功透過抑制鉀通道讓細胞去極化,打開鈣通道。
-
表現:Responsive(隨 Ang II 上升而劇烈上升)。
2. 病理型態 (The Pathology)
- Ang II Unresponsive (KCNJ5):通常對應到 「單顆、較大、富含脂質 (Clear cell)」 的典型腺瘤。這類腫瘤邊界清楚,切除效果極好。
- Ang II Responsive (Wild-type):通常對應到 「多發性小結節 (Micronodules)、緻密細胞 (Compact cell)、或瀰漫性增生 (Diffuse Hyperplasia)」。
- 這類病變往往太小,CT 掃不到(正如你設定的「影像正常」)。
- 這類病變常是 雙側性 或 多發性 的。
3. 治療決策 (The Strategy)
-
手術效果 (Surgical Outcome):
-
手術最怕「切了一邊,結果另一邊也有病」。
-
Responsive / Wild-type 的病人,因為傾向是 瀰漫性/雙側性 病變,單側腎上腺切除往往無法達到「完全治癒 (Complete Clinical Success)」,術後高血壓持續的風險較高。
-
結論:這類病人若無法透過 AVS 強力證明是單側,藥物治療 (MRA) 確實是更穩健的首選。
如果今天有一個病人,他的姿勢測試是「Responsive」(Aldo 上升),CT 上卻看到一顆 1.5 公分的腺瘤。
- 這時候你會聽「生理反應」(Responsive -> 像是雙側/增生 -> 吃藥)?
- 還是聽「影像結果」(有瘤 → 像是單側 → 開刀)?
- 這個矛盾的狀況下,哪一個檢查會成為最終的裁判官(Tie-breaker)?為什麼?
(提示:回想一下,有沒有可能是一顆「剛好長大」的 Wild-type 腺瘤?或者是功能不強的腺瘤配上旁邊的增生?)
「影像 (Anatomy) 與功能 (Physiology) 不一致」 時的決策核心:功能(AVS)大於影像(CT)。這正是內分泌高血壓診斷中最容易犯錯、也最重要的觀念。
這也是為什麼 2025 Guideline 強烈建議除了年輕 (<35歲)、表現極典型且影像吻合的病人外,其餘想開刀者都必須做 AVS 。
核心總結:影像與功能的法庭辯論
面對這個矛盾的病例:
- 生理證人 (Posture Test - Responsive):
- 證詞:「這個病人的 Aldosterone 會隨 Ang II 上升,代表細胞膜電位沒有『卡死』,像是 雙側增生 (IHA) 或 Wild-type。」
- 傾向判決:藥物治療 (MRA)。
- 影像證人 (CT - 1.5 cm Adenoma):
- 證詞:「左邊有一顆明顯的瘤,右邊正常,這看起來像是 單側腺瘤 (APA)。」
- 傾向判決:手術切除。
陷阱 (The Trap):這可能是一顆 無功能的偶發瘤 (Non-functioning Incidentaloma)。因為 35 歲以上的人,腎上腺偶發瘤非常常見 。如果是「右邊增生分泌 Aldosterone,左邊剛好長一顆無功能瘤」,只看 CT 去切左邊,病人就白挨一刀了。
- 最終法官 (AVS - The Gold Standard):
- 只有 AVS 能告訴我們,那顆 1.5 cm 的瘤 「到底有沒有在做事」。
- 判決 A (Lateralization):如果 AVS 顯示左邊優勢,代表這是一顆 少見的、對 Ang II 有反應的 Wild-type 單側腺瘤。 → 開刀 (Cure)。
- 判決 B (No Lateralization):如果 AVS 顯示兩邊都有分泌,代表那是無功能瘤合併雙側增生。→ 吃藥 (MRA)。
為什麼這樣想是合理的(文獻支持)
-
CT 的不可靠性:統合分析顯示,單靠 CT/MRI 判斷 PA 的側性,與 AVS 的結果相比,約有 38% (接近 4 成) 的機會是錯的 。這就是為什麼你堅持要做 AVS 是絕對正確的。
-
病理驗證:若最後證實是「對 Ang II 有反應的單側腺瘤」,切下來的病理通常會是 Compact cells (緻密細胞) 為主,且 CYP11B2 染色可能呈現 Heterogeneous (不均勻) 的型態,這符合 Wild-type 的特徵 。
