1: 標題頁 - 糖尿病的精準革命
詳細說明: 這張投影片宣告了糖尿病醫學的典範轉移:從過去依賴「群體治療(一體適用)」的模式,轉向基於「基因組學」與「病理生理學」的個人化精準醫療 。
核心驅動力: 這一波革命由三大支柱驅動:
-
基因組學突破: 如 GWAS 研究與多基因風險評分 (PRS) 。
-
免疫學分期: 實現 T1D 的症狀前篩檢 。
-
精準藥物選擇: 依據併發症風險與基因型用藥(如 2025 ADA 指南強調的重點)。
2: 糖尿病的異質性:為何一種治療策略無法適用於所有人?
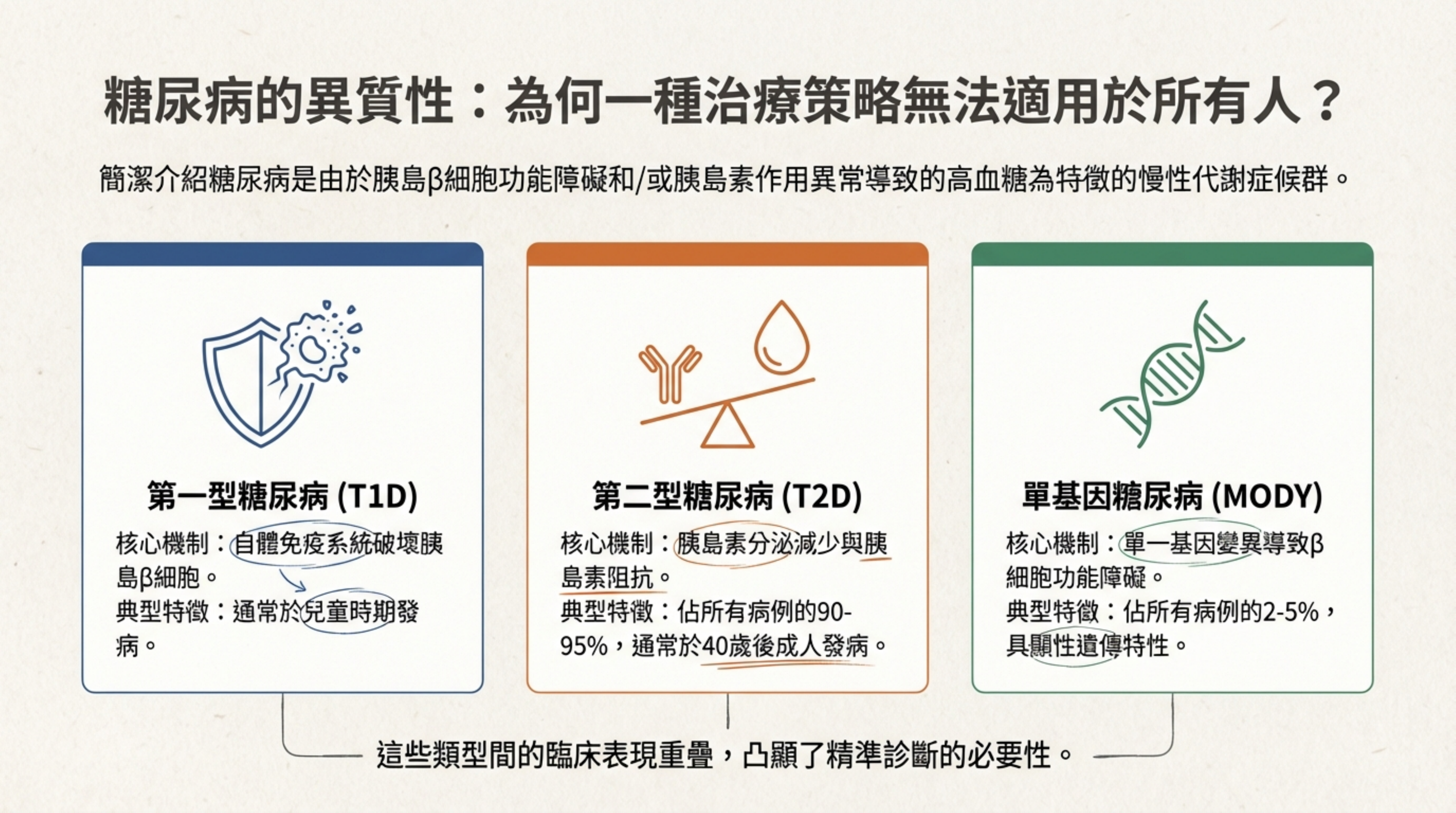
詳細說明: 本頁強調糖尿病並非單一疾病,而是高度異質的症候群 。
-
第 1 型糖尿病 (T1D): 自體免疫破壞 細胞,好發於兒童 。
-
第 2 型糖尿病 (T2D): 佔 90-95%,機制為胰島素阻抗與分泌不足 。
-
單基因糖尿病 (MODY): 佔約 2-5%,常被誤診。其為單基因顯性遺傳,具有明確的「全或無」效應 。
臨床意義: 區分這些類型至關重要,因為 MODY 患者若被誤診為 T1D,可能會接受不必要的胰島素治療,而實際上他們可能對口服磺醯脲類藥物反應更好 。
3: 管理策略的雙軌制:上游預防 vs. 下游減災
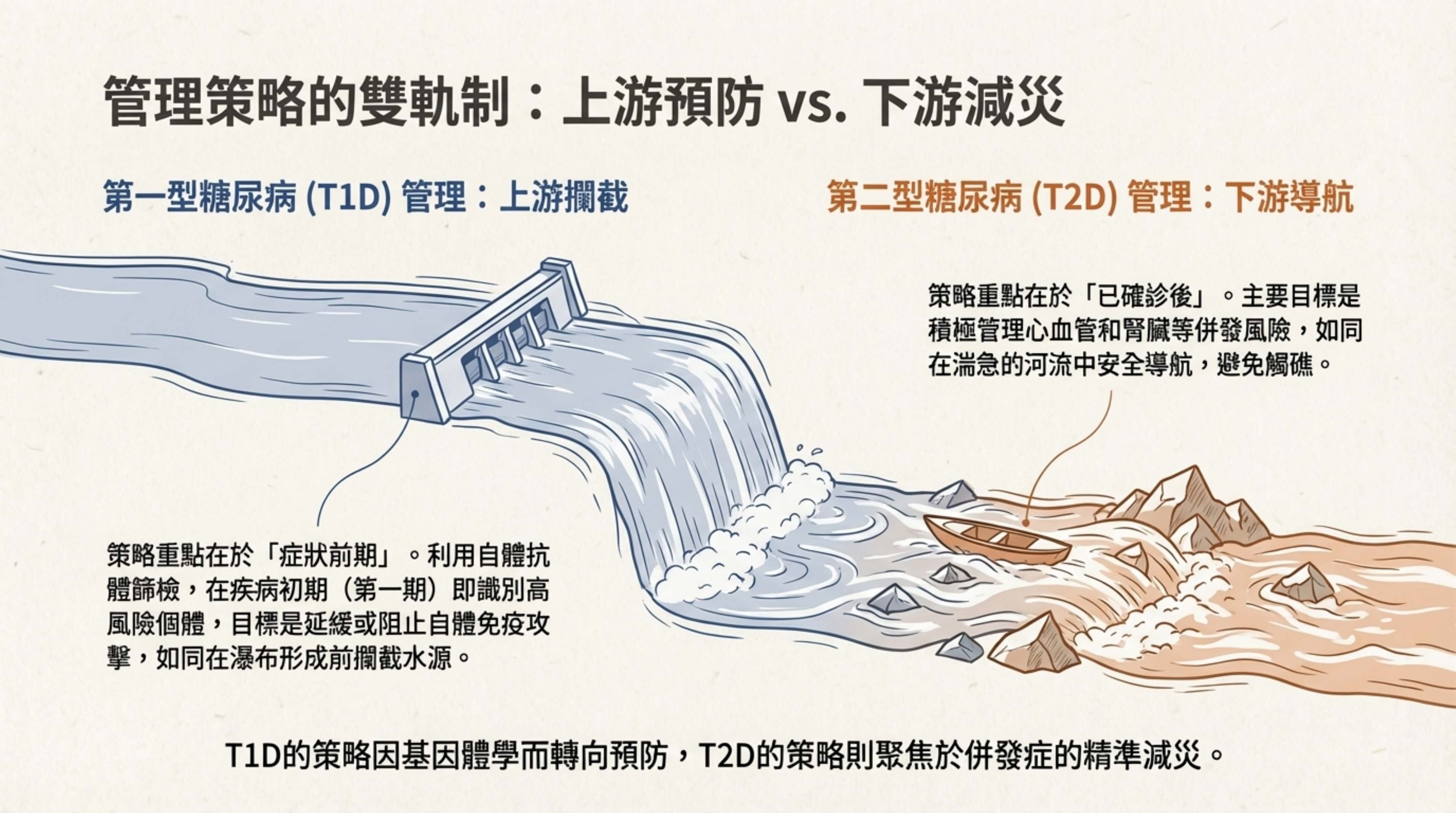
詳細說明: 根據 2025 ADA 指南與最新趨勢,T1D 與 T2D 的管理策略呈現「雙軌化」 :
T1D (上游攔截): 重點在於「症狀前期」的篩檢。透過檢測自體抗體,在第 1 期 (Stage 1) 就識別出高風險個體,目標是延緩發病或進行預防性治療 。
T2D (下游導航): 重點在於「確診後」的併發症管理。由於 T2D 發現時常已伴隨代謝異常,策略聚焦於使用 SGLT2i 或 GLP-1 RA 等藥物來預防心血管與腎臟併發症 。

4: 評估 T2D 風險:我們如何量化未來十年的可能性?
詳細說明: 介紹臨床常用的風險評估工具 芬蘭糖尿病風險評分 (FINDRISC) 。
評估項目: 包含年齡、BMI、腰圍、活動量、蔬果攝取、高血壓病史等 8 項指標 。
分數解讀:
21 分 (極高風險): 10 年內發病機率達 50%,建議每年檢測 HbA1c 。
15-20 分 (高風險): 10 年發病率 33%,建議每 3-5 年檢測 。
價值: 作為一種低成本、非侵入性的篩檢工具,能有效將醫療資源集中於高風險族群 。

5: 預見 T1D:在症狀出現前,血液中的免疫信號
詳細說明: T1D 的風險評估依賴於檢測血液中的糖尿病相關自體抗體 (AABs) 。
篩檢對象: T1D 患者的親屬(患病風險比一般人高 15 倍)。建議篩檢對象包括 2-45 歲的一等親或 2-20 歲的二等親 。
目標抗體: 胰島素 (IAA)、谷氨酸脫羧酶 (GADA)、胰島細胞抗原-2 (IA-2A)、鋅轉運蛋白 8 (ZnT8A) 。
判定標準: 檢測到兩種或以上的持續性自體抗體,即被定義為早期 T1D,終生發病風險接近 100% 。
6: T1D 的演進三部曲:從免疫觸發到臨床診斷的旅程
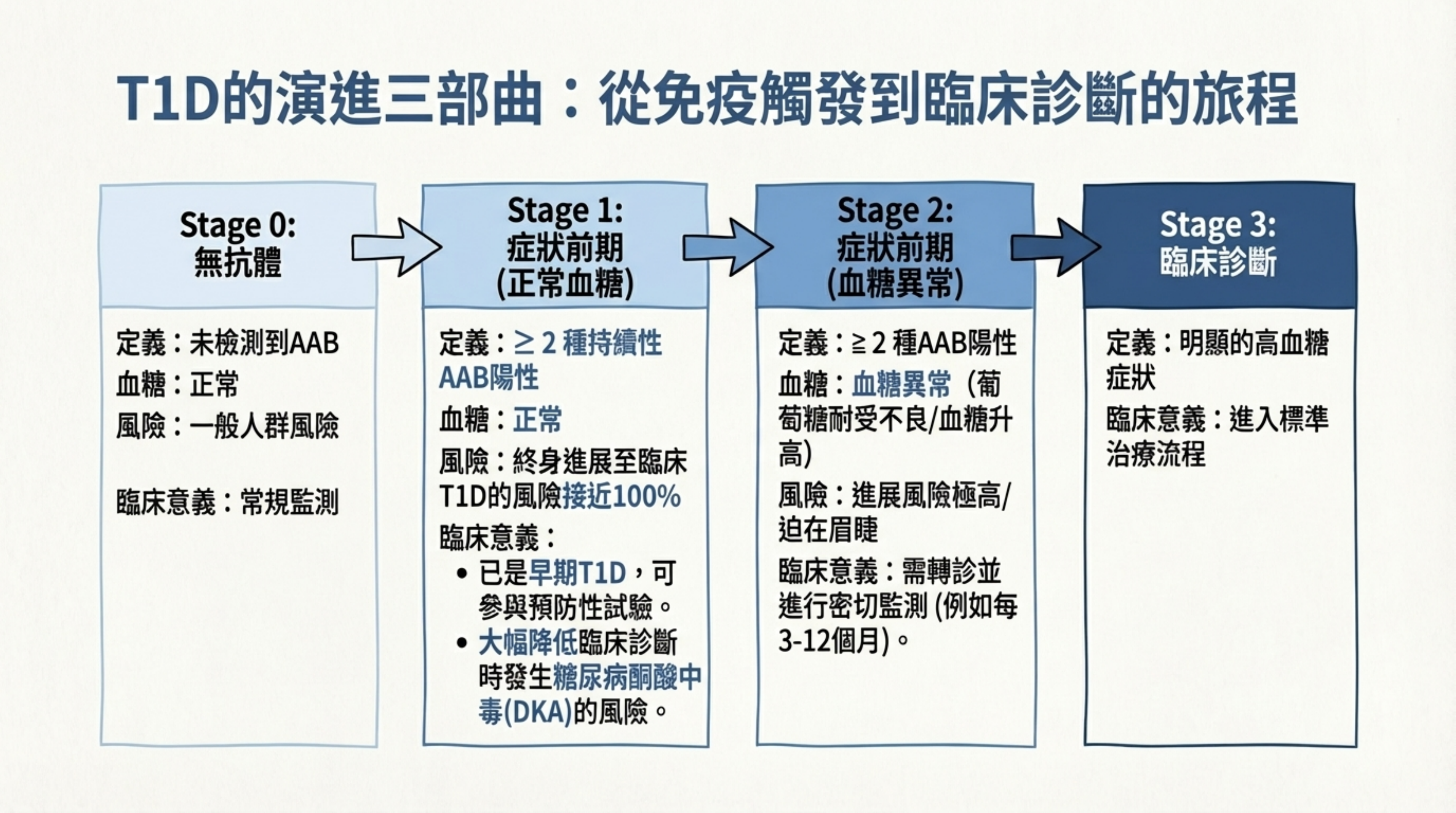
詳細說明: T1D 的發病是一個漸進過程,臨床上分為三期 :
Stage 1 (症狀前期-正常血糖): 2 種 AAB 陽性 + 血糖正常。此階段已是早期 T1D,關鍵價值在於可參與預防性試驗,並大幅降低診斷時發生酮酸中毒 (DKA) 的風險 。
Stage 2 (症狀前期-血糖異常): 2 種 AAB 陽性 + 血糖異常 (Dysglycemia),但無明顯症狀。進展風險極高,需密切監測(每 3-6 個月)。
Stage 3 (臨床診斷): 出現典型高血糖症狀,需標準胰島素治療 。
7: 糖尿病的基因藍圖:三種截然不同的遺傳故事
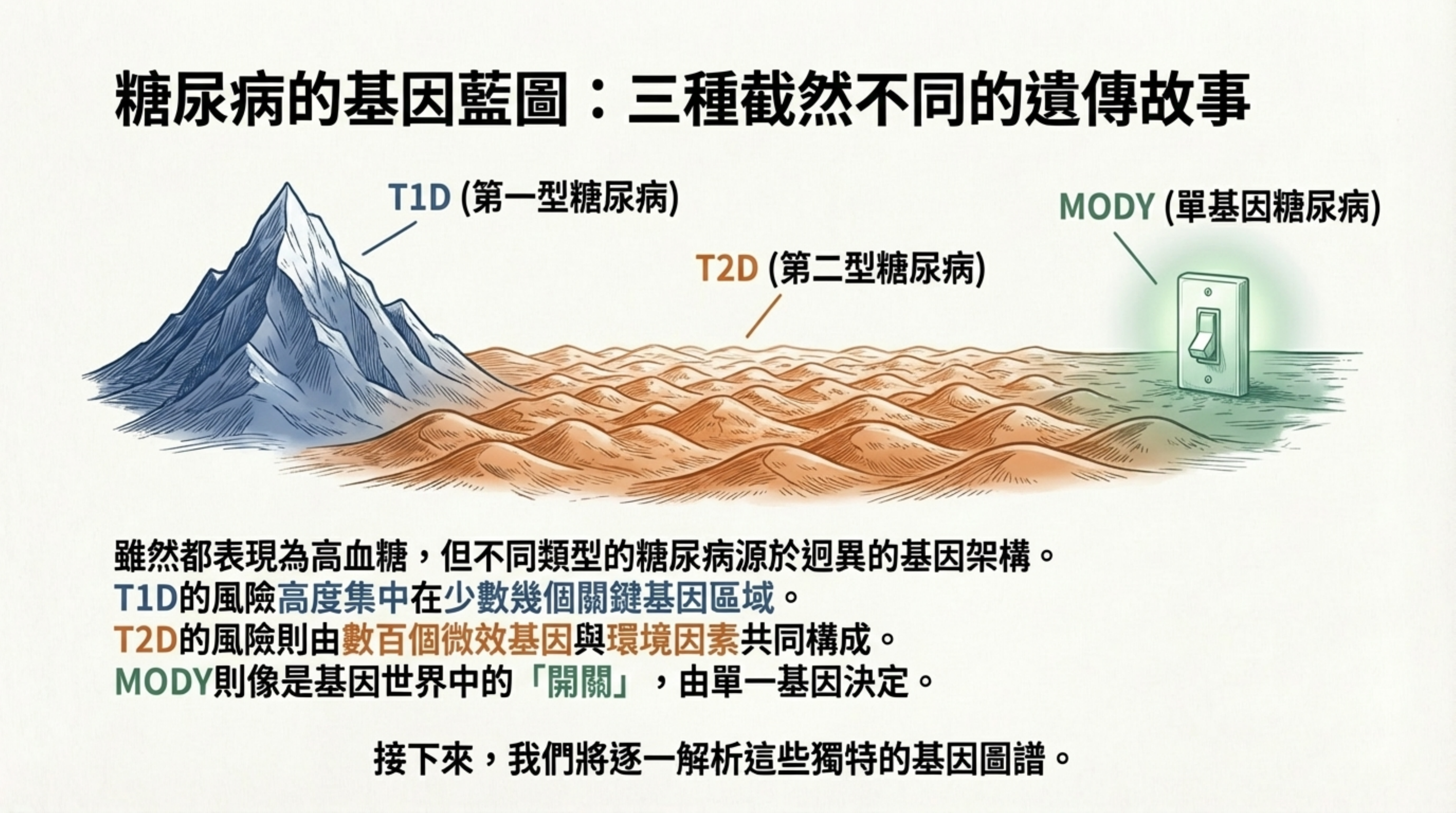
詳細說明: 使用地貌比喻來解釋不同亞型的基因架構 :
T1D (高山): 遺傳風險高度集中在少數幾個關鍵區域(主要是 HLA 區域),影響力巨大 。
T2D (丘陵): 高度多基因特性。風險由數百個微效基因(如 TCF7L2, FTO)與環境因素共同堆疊而成 。
MODY (開關): 單基因特性。由單一基因變異(如 HNF1A)決定,像開關一樣直接導致疾病 。
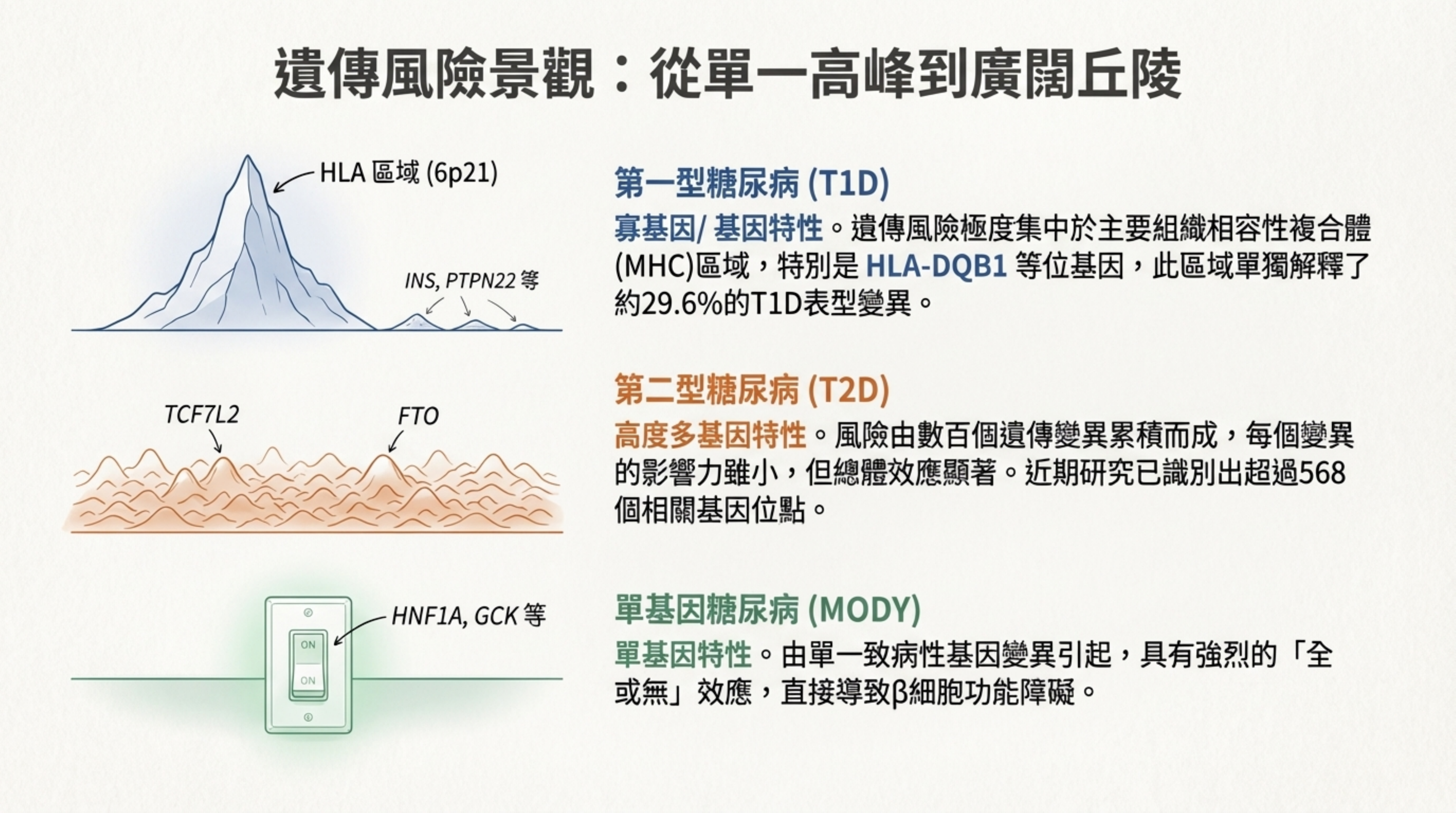
8: 遺傳風險景觀:從單一高峰到廣闊丘陵
詳細說明: 深入解析各亞型的關鍵基因 :
T1D: 主要由 HLA Class II 區域 (6p21) 驅動,特別是 HLA-DQB1,單獨解釋了約 30% 的表型變異 。
T2D: 已識別出超過 568 個相關位點。雖然單個變異影響小,但累積效應顯著 。關鍵基因包括影響胰島素分泌的 TCF7L2 和與肥胖相關的 FTO 。
MODY: 由 HNF1A, GCK, HNF4A 等基因的單一突變引起,具有強烈的家族遺傳性 。
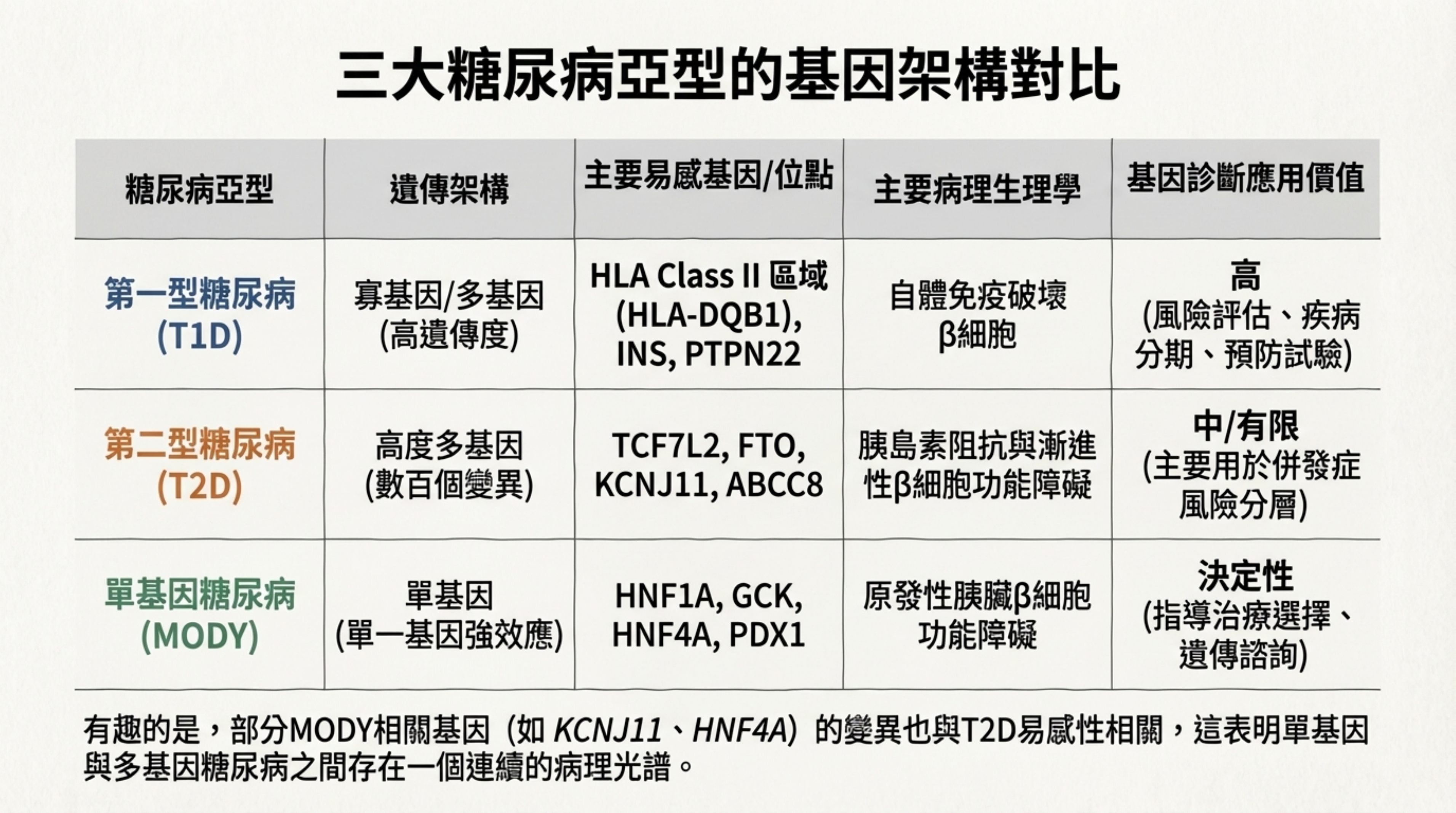
9: 三大糖尿病亞型的基因架構對比
詳細說明: 這是一個總結比較表 :
T1D: 寡基因/多基因,主要病理為自體免疫。基因診斷價值在於風險評估與分期 。
T2D: 高度多基因,病理為胰島素阻抗與 細胞衰竭。基因診斷價值中等,主要用於併發症風險分層 。
MODY: 單基因,病理為原發性 細胞功能障礙。基因診斷具有決定性價值,可直接指導治療選擇(如停用胰島素) 。

10: 多基因風險評分 (PRS):是預測未來的占卜,還是指導行動的羅盤?
詳細說明: 介紹 PRS (Polygenic Risk Score) 的概念與局限。
定義: PRS 將數百萬個基因變異的微小風險加總,計算個體的累積遺傳易感性 。
挑戰:
-
預測能力有限: 在預測 T2D 發病方面,PRS 目前並未顯著優於 FINDRISC 等臨床評分 。
-
族群偏差: 現有模型多基於歐洲人數據 (PRS_EU),應用於亞洲或非裔族群時準確度大幅下降 。
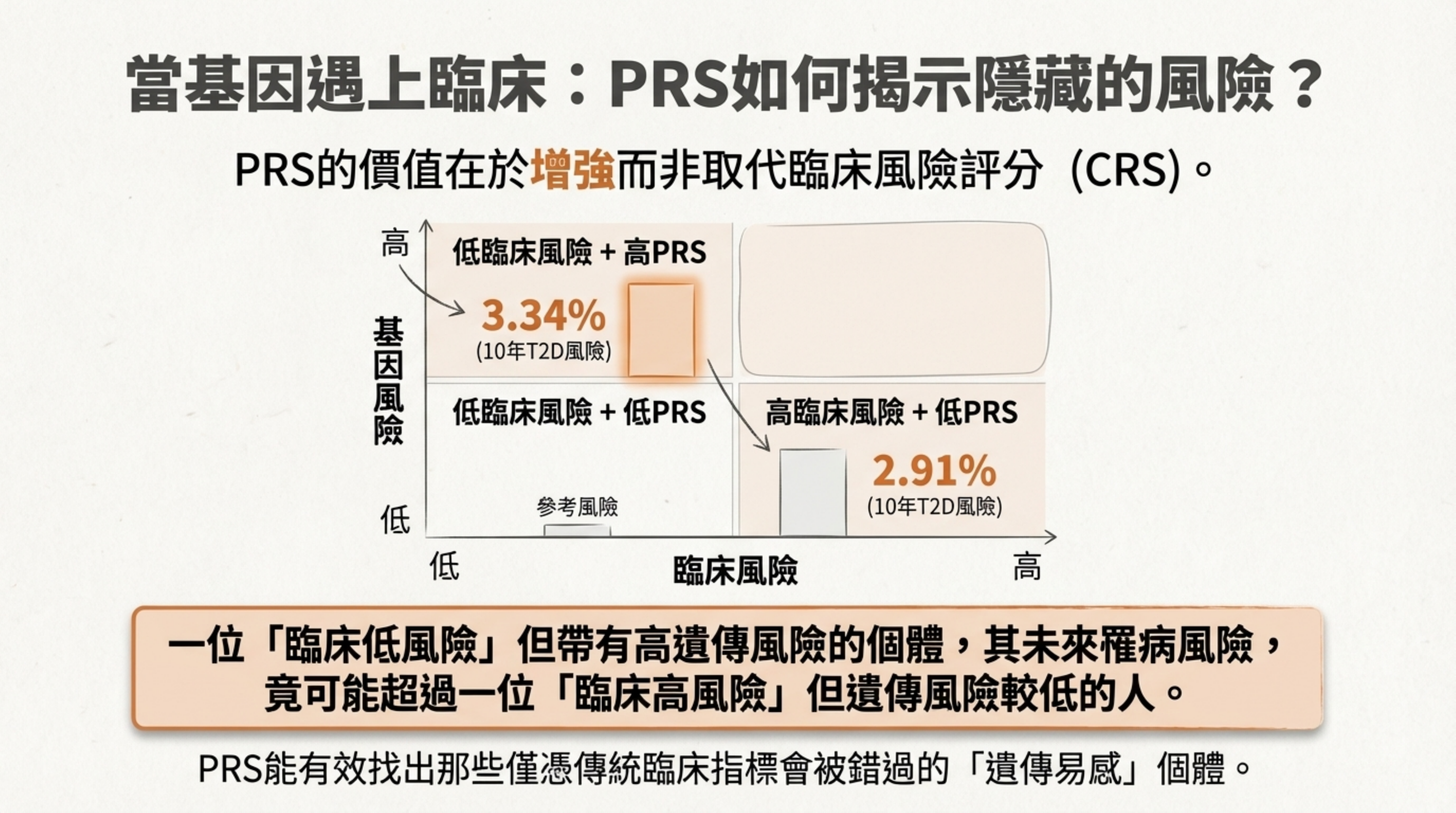
11: 當基因遇上臨床:PRS 如何揭示隱藏的風險?
詳細說明: PRS 的真正價值在於增強而非取代臨床評分 。
數據洞察: 研究發現,一位「臨床低風險」但帶有高遺傳風險 (High PRS) 的個體,其未來 10 年的發病風險 (3.34%),竟然超過一位「臨床高風險」但遺傳風險較低的人 (2.91%) 。
意義: 這表明 PRS 能找出那些僅憑 BMI 或年齡會被漏掉的「遺傳易感」隱形患者 。
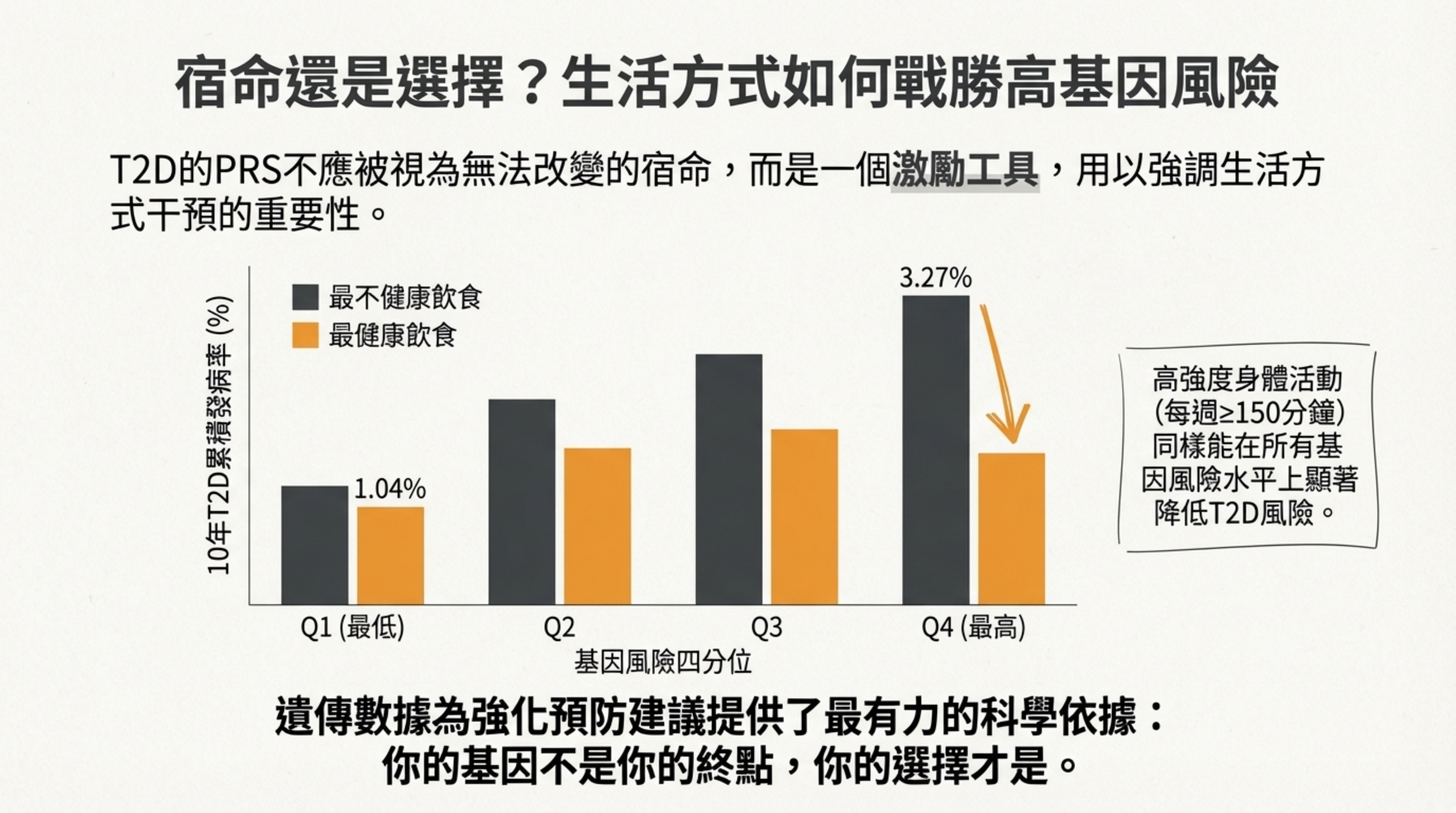
12: 宿命還是選擇?生活方式如何戰勝高基因風險
詳細說明: 探討 基因-環境 (G x E) 交互作用 。
核心訊息: 基因不是宿命。EPIC-InterAct 研究顯示,即便在基因風險最高的那群人中,若能維持健康飲食與運動,其 10 年累積發病率可從 3.27% 降至 1.04% 。
應用: PRS 應作為一個激勵工具,用科學數據告訴患者:「你的基因不是你的終點,你的選擇才是」 。
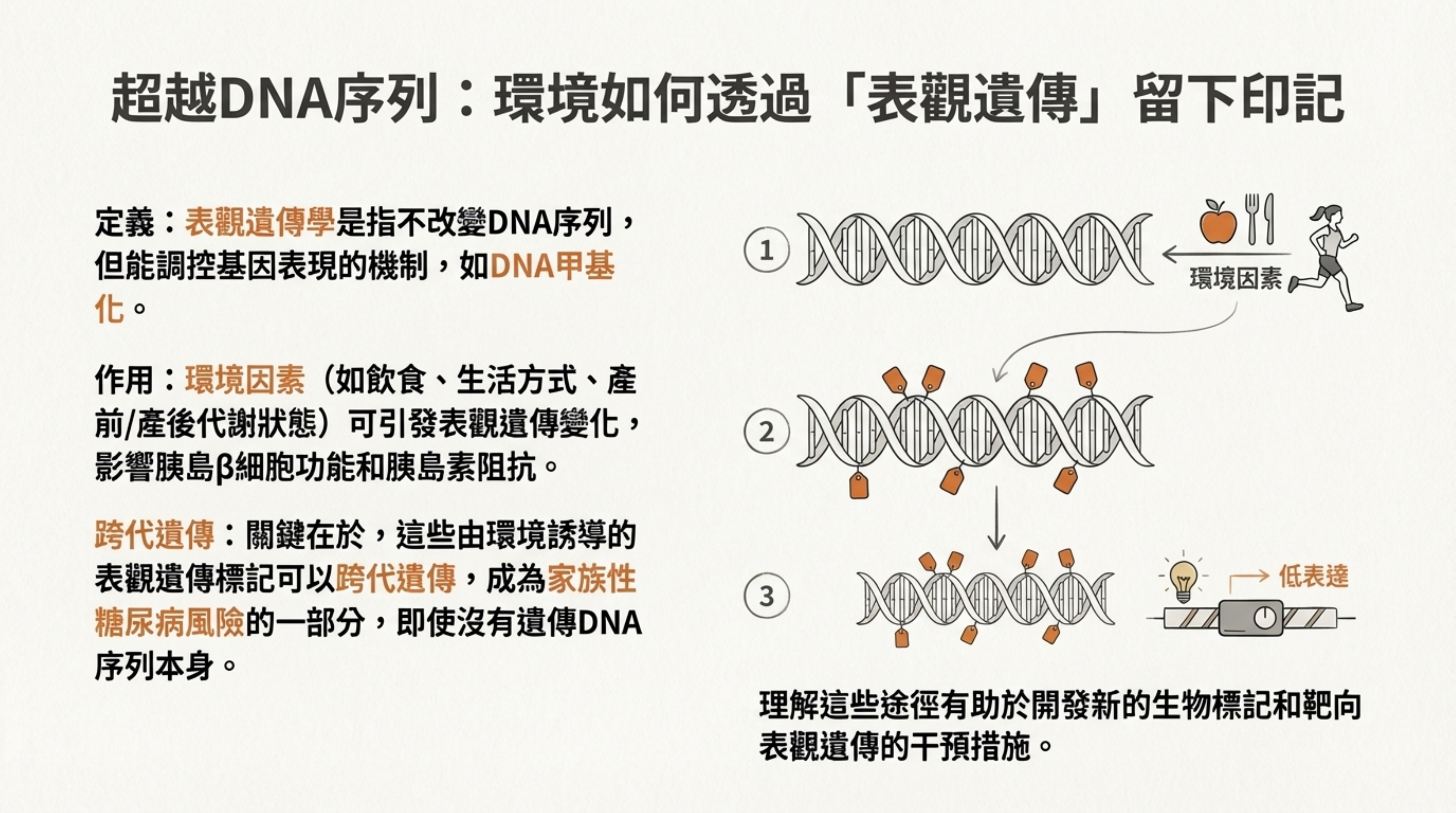
13: 超越 DNA 序列:環境如何透過「表觀遺傳」留下印記
詳細說明: 介紹表觀遺傳學 (Epigenetics) 作為連接環境與基因的橋樑 。
機制: 環境因素(如飲食、壓力)不改變 DNA 序列,但透過 DNA 甲基化等機制調控基因表現 。
影響: 這些變化可影響胰島素分泌與阻抗,甚至可能跨代遺傳,解釋了為何不良生活環境會增加後代的糖尿病風險 。
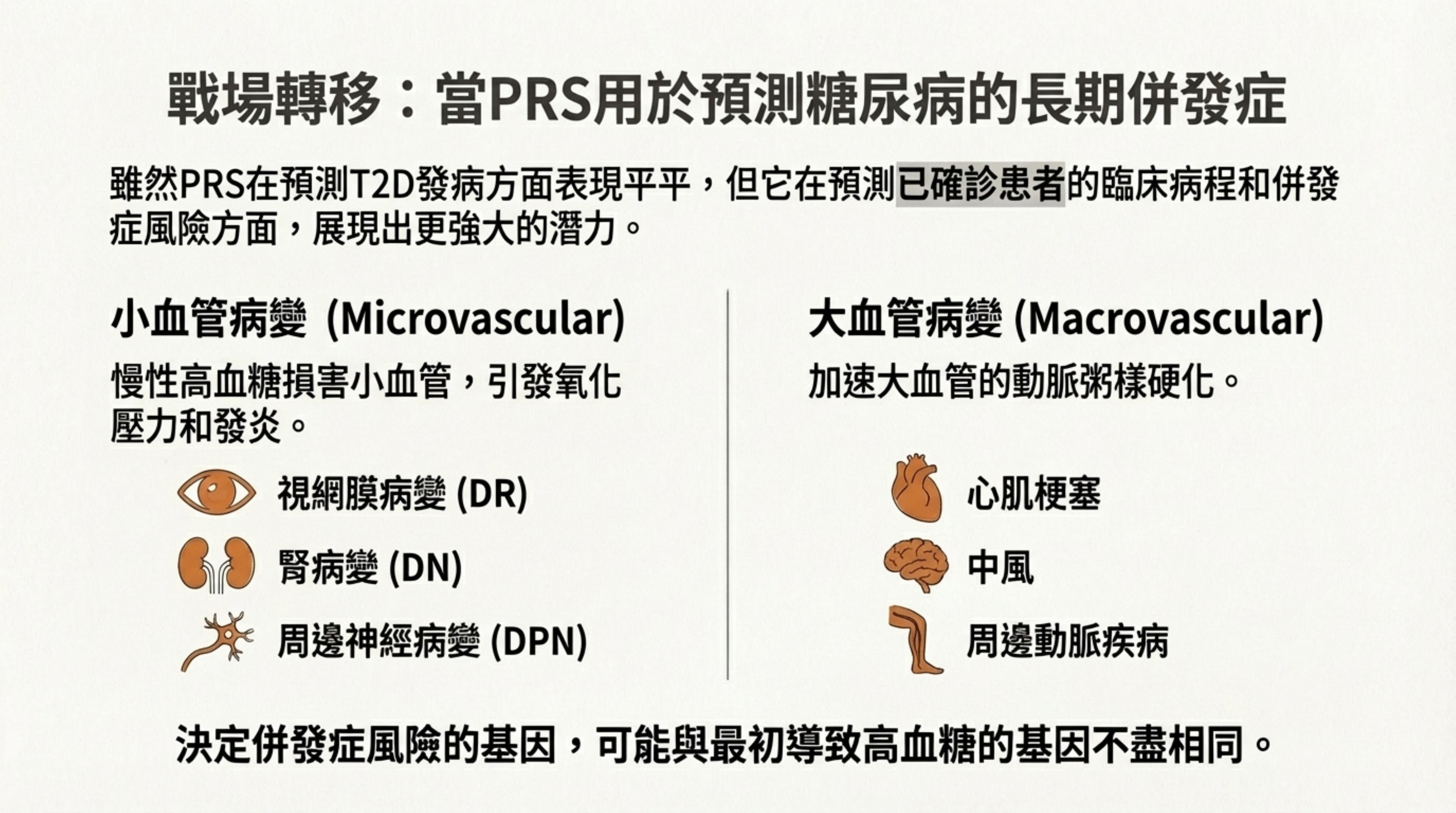
14: 戰場轉移:當 PRS 用於預測糖尿病的長期併發症
詳細說明: PRS 的應用重心正從預測「發病」轉向預測「併發症」 。
潛力: 研究顯示,針對糖尿病視網膜病變 (DR) 開發的 PRS,能有效預測患者未來 20 年發展成嚴重 DR 的風險 。
價值: 這使得臨床醫師能針對高 PRS 患者進行更頻繁的眼底檢查或早期介入,實現分層管理 。
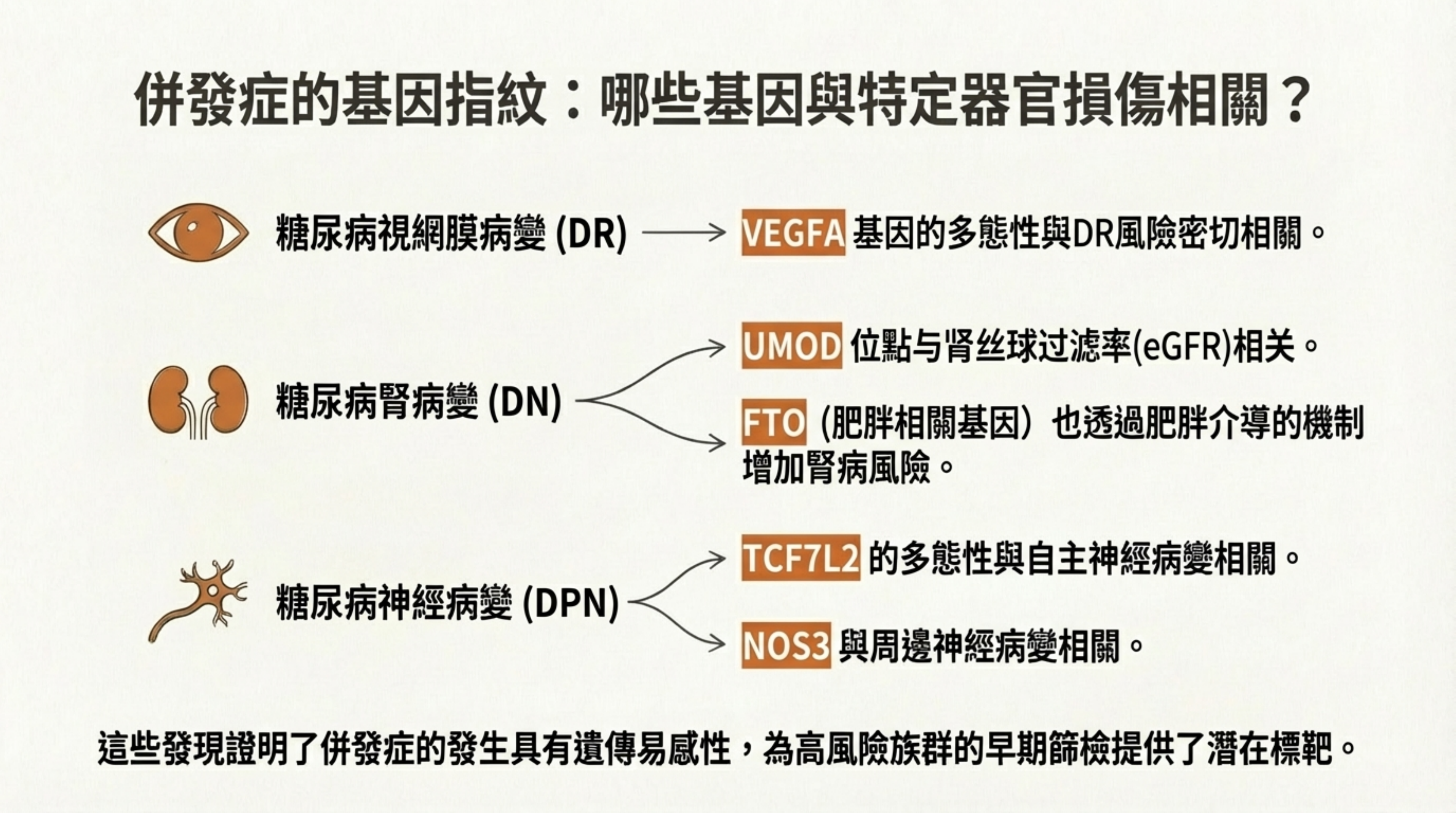
15: 併發症的基因指紋:哪些基因與特定器官損傷相關?
詳細說明: 列舉與特定併發症高度相關的基因位點 :
視網膜病變 (DR): VEGFA 基因多態性與視網膜血管增生風險密切相關 。
腎病變 (DN): UMOD 位點與腎絲球過濾率 (eGFR) 相關;FTO 透過肥胖機制增加腎病風險 。
神經病變 (DPN): TCF7L2 與 NOS3 基因變異分別與自主神經及周邊神經病變相關 。
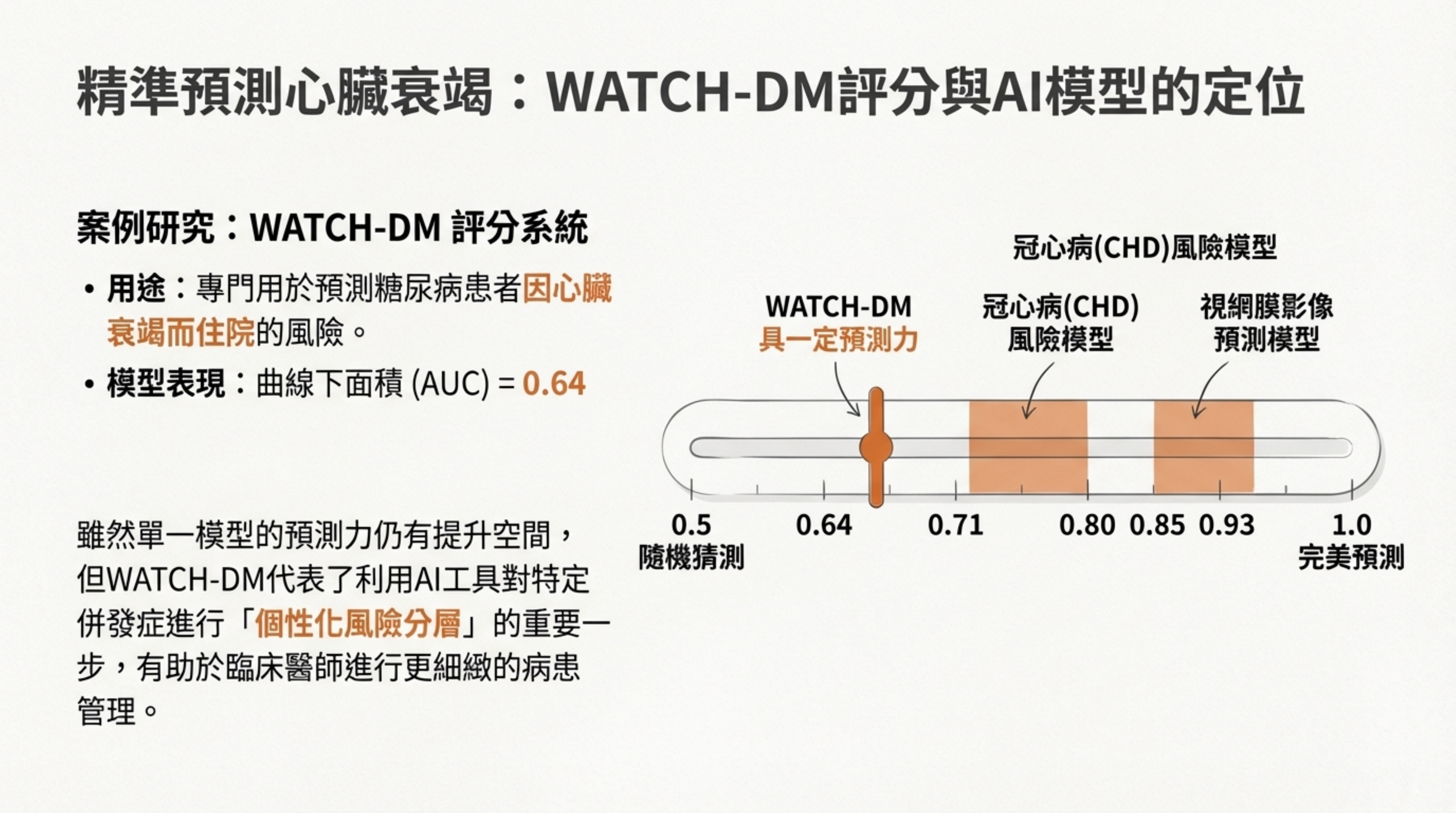
16: 精準預測心臟衰竭:WATCH-DM 評分與 AI 模型的定位
詳細說明:
WATCH-DM 評分: 這是一個專門用於預測 T2D 患者心臟衰竭住院風險的臨床工具,其 AUC 約為 0.64。(註:此內容來自投影片本身,RTF 文件中主要討論 SCORE2-Diabetes ,但概念一致,皆為針對糖尿病患的心血管風險分層工具)。
定位: 雖然單一模型預測力有限,但結合 AI 與基因數據(如 SGLT2i 反應相關基因),能進一步提升對心腎併發症的預測精準度 。
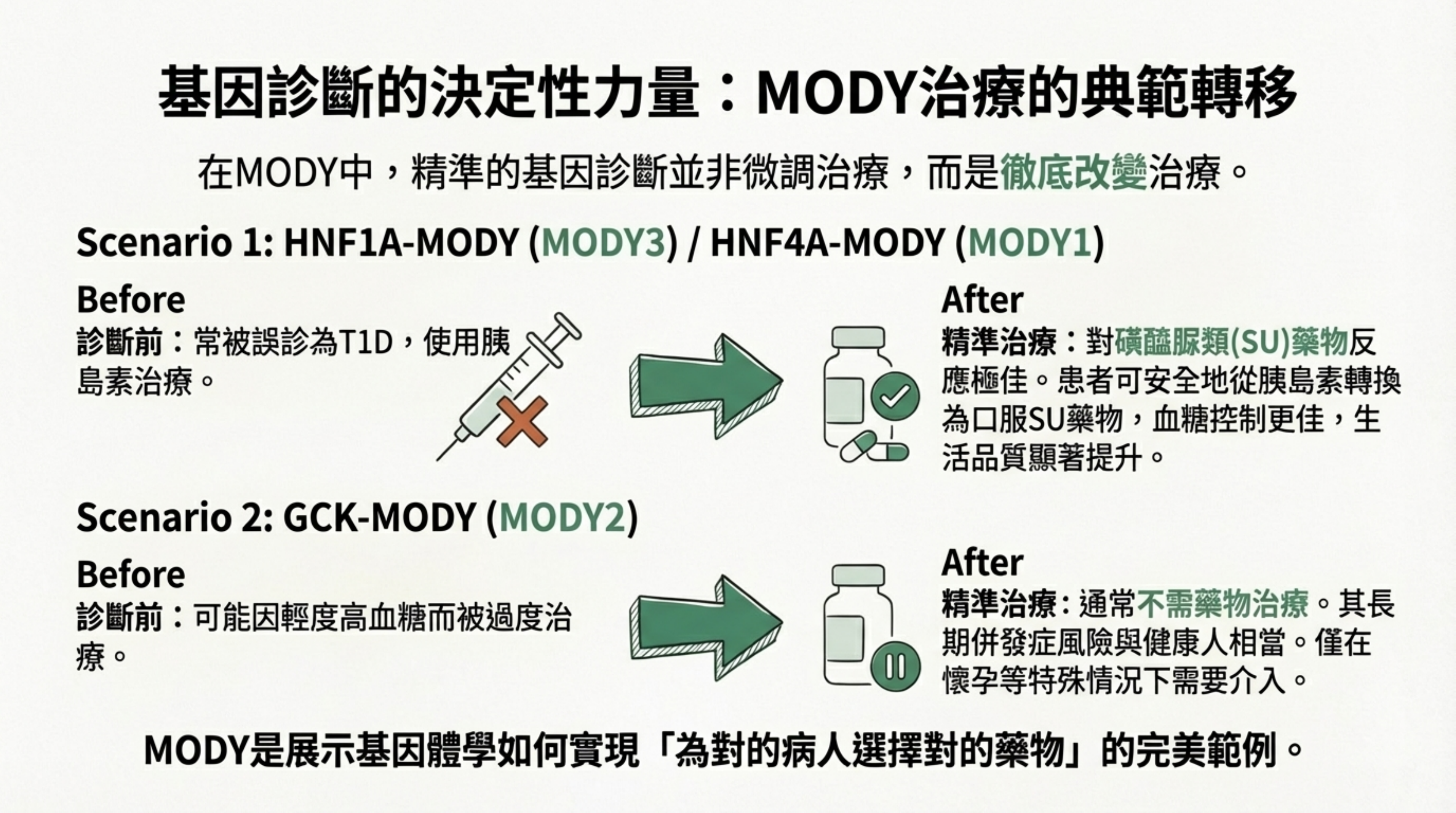
17: 基因診斷的決定性力量:MODY 治療的典範轉移
詳細說明: 展示基因檢測如何徹底改變治療方案 (Pharmacogenomics) :
HNF1A/HNF4A-MODY: 這些患者常被誤診為 T1D 而打胰島素。基因確診後,可轉用磺醯脲類 (SU) 口服藥,效果更好且生活品質提升 。
GCK-MODY: 表現為輕度高血糖,通常不需治療,長期預後良好。避免了過度醫療 。

18: T2D 的藥物基因體學:解碼藥物反應的個體差異
詳細說明: 探討 T2D 常見藥物的基因反應差異 :
Metformin: 療效受藥物動力學 (PK) 基因影響,個體差異大 。
SGLT2 抑制劑: 其降低心臟衰竭風險的效益與 CXCL10 等發炎基因有關,提示可用於篩選最能從心臟保護中獲益的族群 。
磺醯脲類 (SU): 代謝組學研究發現,特定代謝物濃度可預測 T2D 患者對 SU 的反應 。
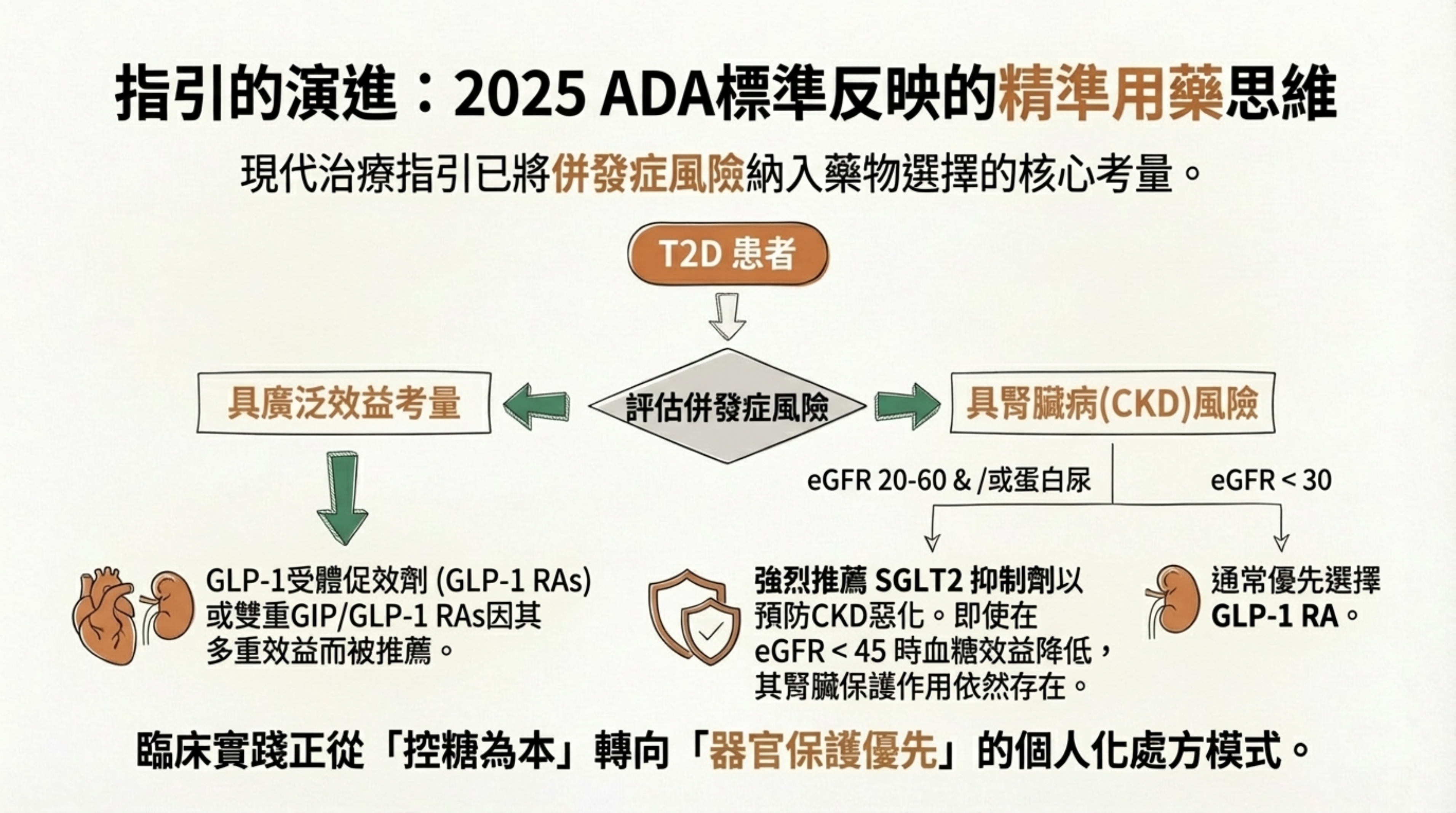
19: 指引的演進:2025 ADA 標準反映的精準用藥思維
詳細說明: 2025 ADA 指南將「併發症風險」納入核心考量 :
器官保護優先: 具腎臟病風險 (eGFR 20-60) 者,強烈推薦 SGLT2i 以預防 CKD 惡化 。
心血管效益: 具廣泛效益考量時,優先選擇 GLP-1 RA 。
*這標誌著治療思維從單純「控糖」轉向基於個人共病風險的「精準保護」 。
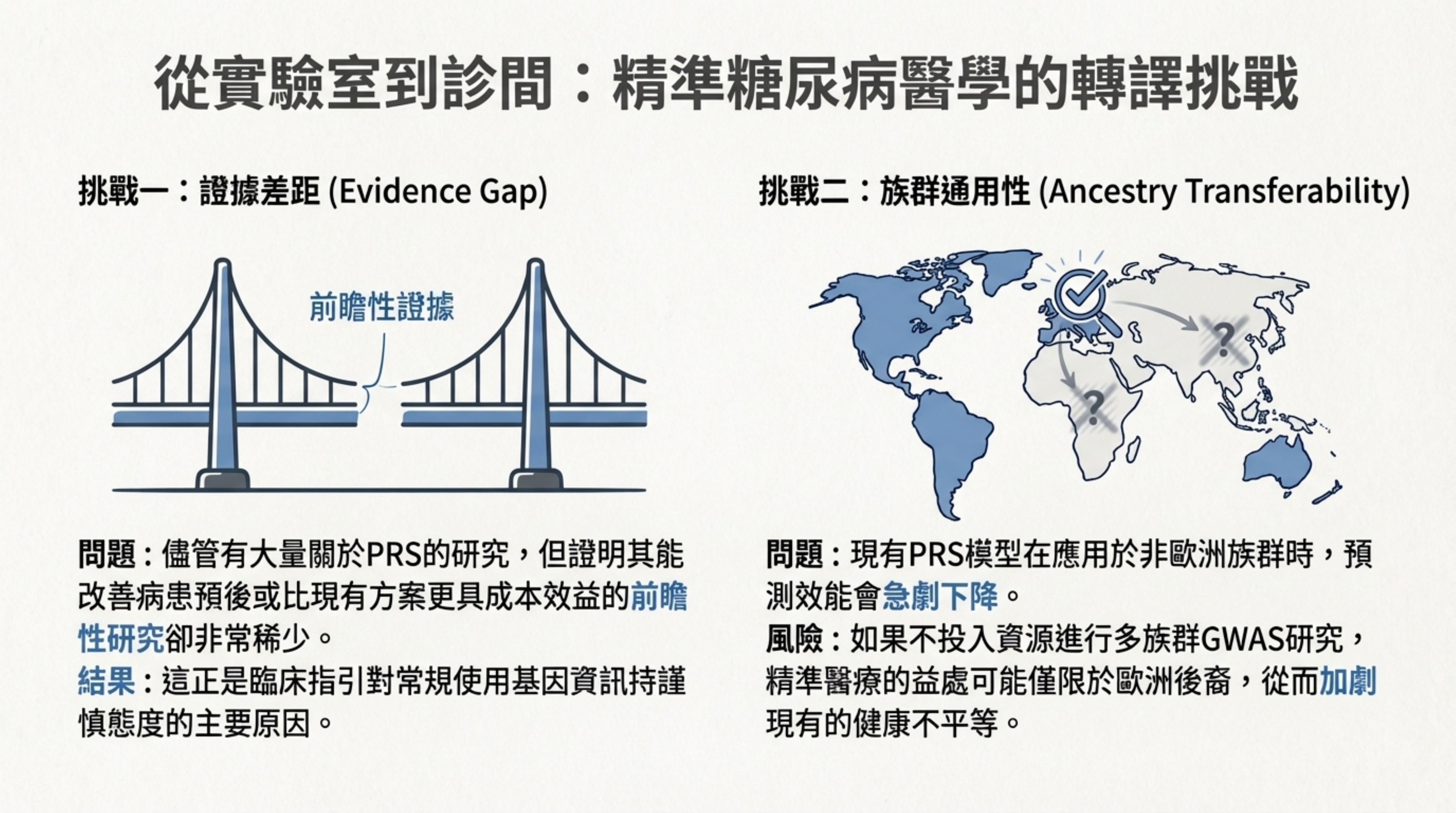
20: 從實驗室到診間:精準糖尿病醫學的轉譯挑戰
詳細說明: 分析推動精準醫療面臨的兩大障礙 :
-
證據差距 (Evidence Gap): 雖然有大量 PRS 研究,但缺乏前瞻性研究證明其能改善臨床預後或具成本效益 。
-
族群通用性 (Ancestry Transferability): 現有模型多基於歐洲人,對非歐洲族群預測力差。若不解決,可能加劇健康不平等 。
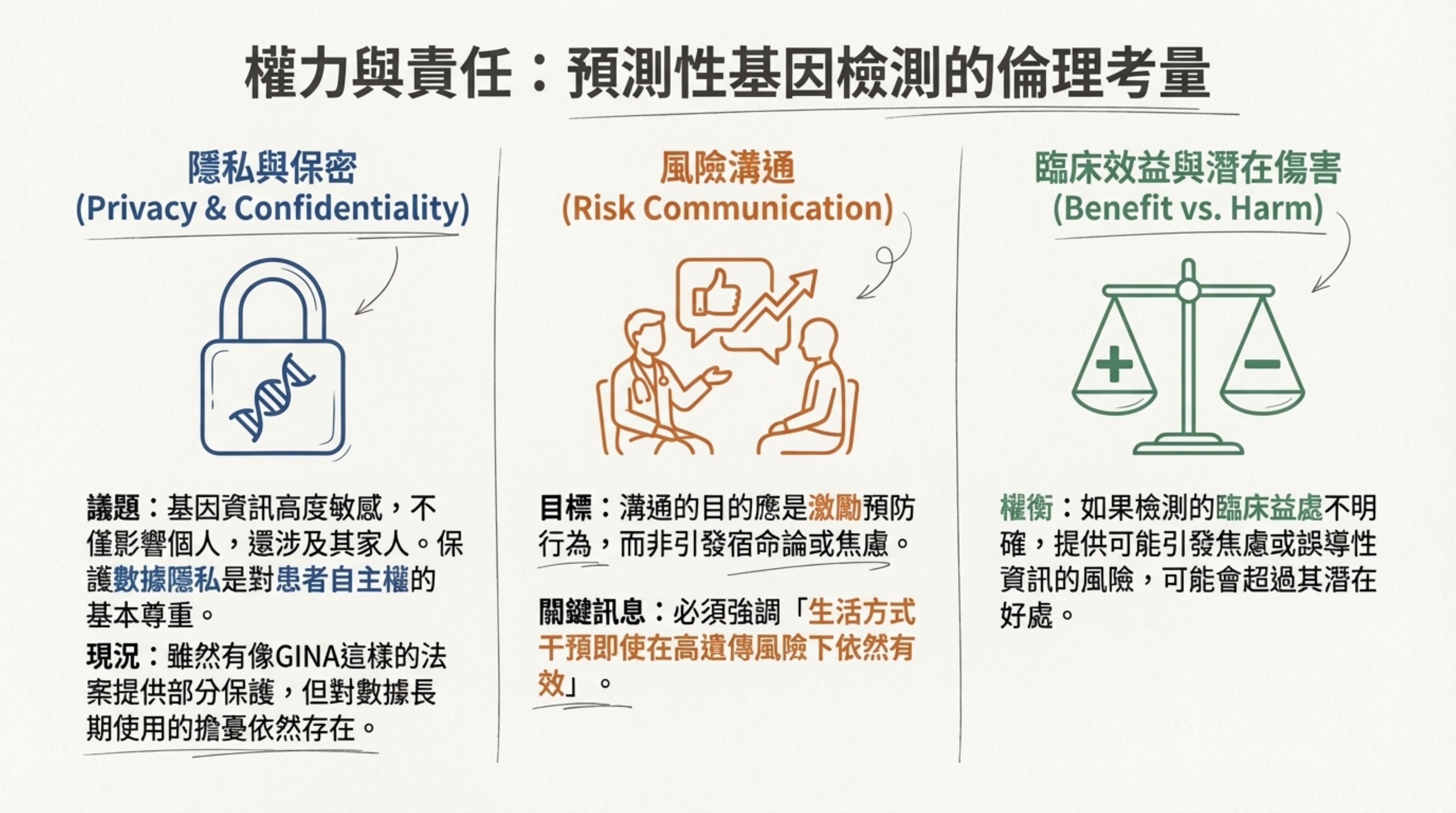
21: 權力與責任:預測性基因檢測的倫理考量
詳細說明: 探討基因檢測帶來的倫理議題 :
隱私與保密: 基因資訊高度敏感,需嚴格保護(如 GINA 法案) 。
風險溝通: 溝通目的應是「激勵預防」而非引發焦慮或宿命論。必須強調生活方式干預的有效性 。
臨床效益平衡: 若無明確臨床效益,提供風險資訊可能弊大於利 。
22: 精準糖尿病醫學的現況:時機與機制的掌握
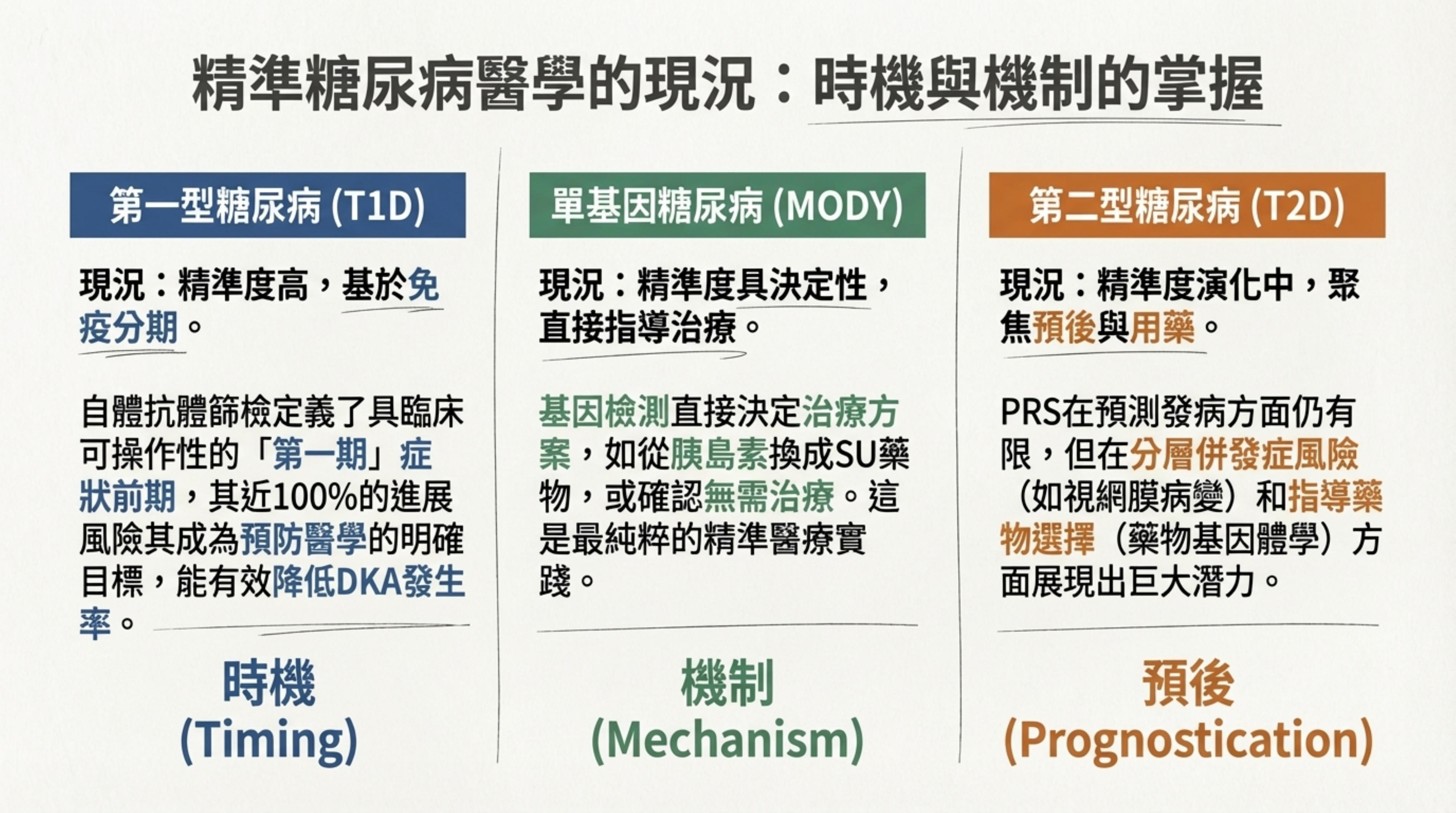
詳細說明: 總結目前的臨床應用現況 :
T1D (時機): 精準度高,基於免疫分期,重點在早期攔截 (Stage 1/2) 。
MODY (機制): 精準度具決定性,基因檢測直接指導治療 。
T2D (預後): 精準度演化中,重點在於併發症分層與藥物選擇 (PGx) 。
23: 推進精準糖尿病照護的策略藍圖
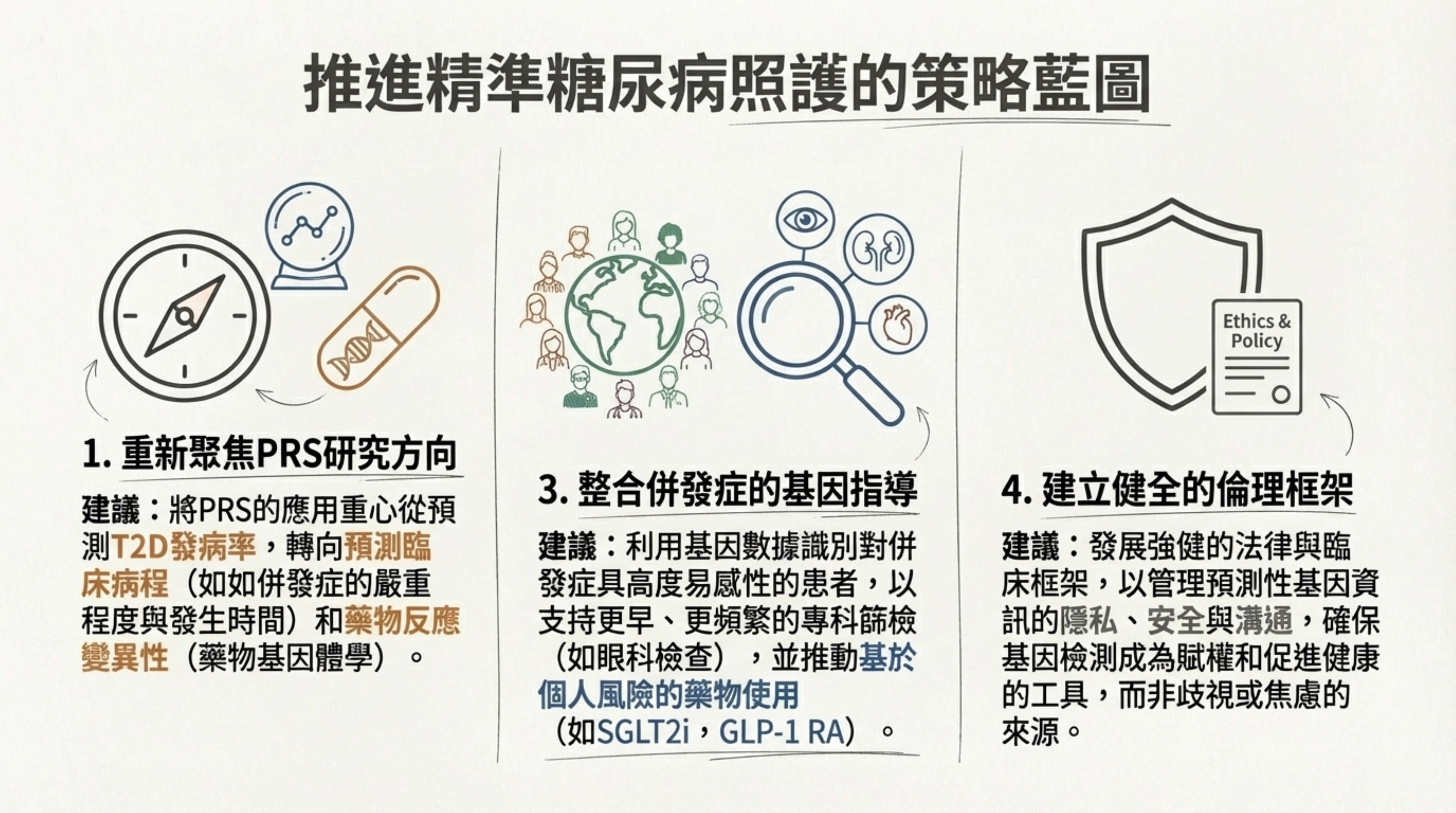
詳細說明: 提出未來的四大行動建議 :
-
重新聚焦 PRS 研究: 從預測發病轉向預測「臨床病程」與「藥物反應」 。
-
整合併發症的基因指導: 利用基因數據識別高風險併發症患者,支持更積極的篩檢與用藥 。
-
建立健全的倫理框架: 確保基因資訊的安全與隱私,讓其成為賦權工具 。
Reference:
- [1] Approach to Monogenic Diabetes. Endotext.
- [4] Diagnosis and Clinical Management of Monogenic Diabetes. Endotext.
- [5] Updates from the 2025 American Diabetes Association guidelines.
- [6] Pathway to Prevention. Type 1 Diabetes TrialNet.
- [7] 2025 ADA Standards of Medical Care in Diabetes: Updates!
- [9] Genetic risk profiling for prediction of type 2 diabetes. PLOS Currents.
- [11] FINDRISC (Finnish Diabetes Risk Score). MDCalc.
- [12] Framingham Risk Score... (Contextual reference for risk scores)
- [13] Pathway to Prevention. Type 1 Diabetes TrialNet.
- [15] Type 1 Diabetes Screening & Early Detection. Breakthrough T1D.
- [16] What you need to know if your child has type 1 diabetes autoantibodies. Breakthrough T1D.
- [18] Genetics of Type 1 Diabetes. NCBI.
- [21] Polygenic score from MODY genes is associated with type 1 diabetes... NIH.
- [20] Progress in genetics of type 2 diabetes and diabetic complications. PMC.
- [18] Genetics of Type 1 Diabetes. NCBI.
- [24] Clinical use of polygenic scores in type 2 diabetes. PubMed.
- [24] Clinical use of polygenic scores in type 2 diabetes. PubMed.
- [25] Assessing the prediction of type 2 diabetes risk using polygenic and clinical risk scores in South Asian study populations. PMC.
- [26] Polygenic Risk Score, Lifestyles, and Type 2 Diabetes Risk: A Prospective Chinese Cohort Study. PMC.
- [28] Gene-Lifestyle Interaction and Type 2 Diabetes: The EPIC InterAct Case-Cohort Study.
- [31] Epigenetics and Type 2 Diabetes Risk. PMC.
- [40] Polygenic risk score for predicting diabetic retinopathy in patients with type 2 diabetes: A twenty-year follow-up study.
- [24] Clinical use of polygenic scores in type 2 diabetes. PubMed.
- [34] Identifying Common Genetic Risk Factors of Diabetic Neuropathies. PMC.
- [20] Progress in genetics of type 2 diabetes and diabetic complications. PMC.
- [49] Genomic insights about the effect of SGLT2 inhibitors. PMC. (For genetic linkage to HF risk).
- [45] Treatment Options for MODY Patients: A Systematic Review. PMC.
- [46] Diagnosis and Treatment of MODY: An Updated Mini Review. MDPI.
- [47] Genetics and response to treatment with metformin. PMC.
- [49] Genomic insights about the effect of SGLT2 inhibitors. PMC.
- [52] Clinical utility of polygenic risk scores: a critical 2023 appraisal. PMC.
- [53] Ethical issues of predictive genetic testing for diabetes. Scholars@Duke.
- [54] Ethical Considerations in Precision Medicine... ACP Journals.
