從受體調控到基因轉錄,再到腸胃道吸收的臨床機轉全解析
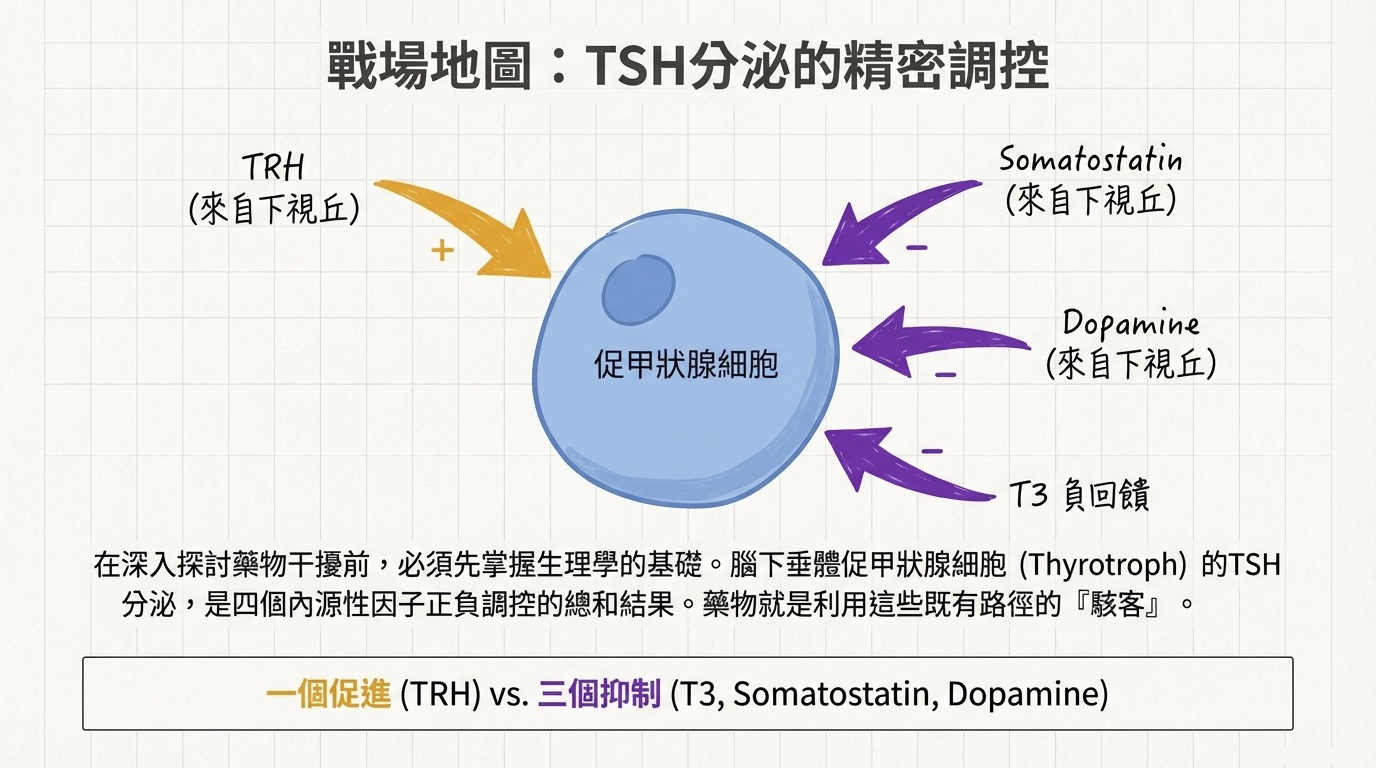
腦下垂體前葉的促甲狀腺細胞(Thyrotroph)處於多種內源性因子的精密調控之下,其最終輸出的 TSH(促甲狀腺素)是正向與負向訊號的總和。 在生理狀態下,四大內源性因子控制著 TSH 的分泌:
- 正向調節 (+): TRH (促甲狀腺素釋放激素)
- 負向調節 (-): T3 (三碘甲狀腺素)、Somatostatin (生長抑素)、Dopamine (多巴胺)
臨床藥物往往扮演著這些自然路徑的「駭客」,透過劫持這些機制產生預期之外的內分泌效應。本文將深入探討三種中樞調控機制與腸胃道吸收障礙的臨床病理生理學。
第一類機制:Dopamine D2 受體路徑與 ICU 的診斷陷阱
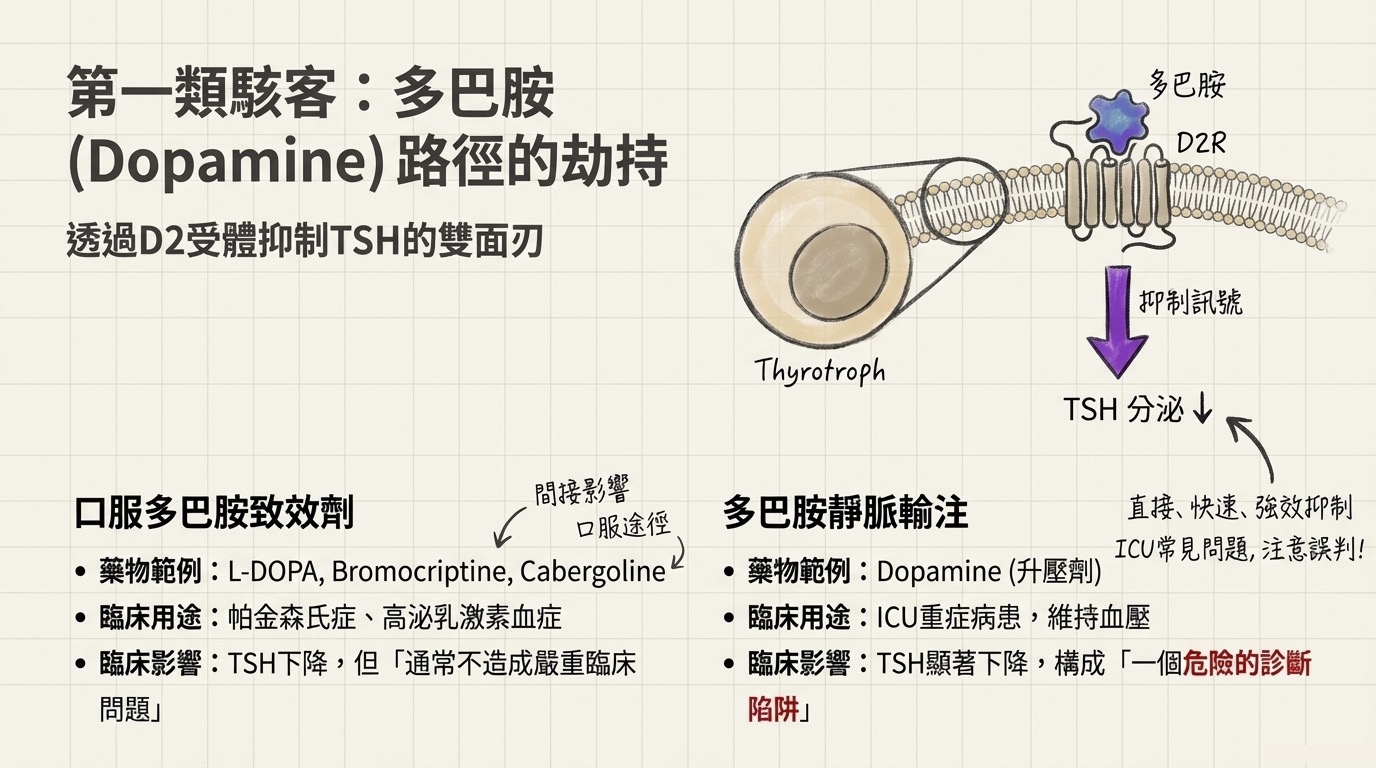
內源性的 Dopamine 透過腦下垂體細胞膜上的 Dopamine D2 受體 (D2R) 發揮抑制 TSH 的生理作用。當藥物介入此路徑時,會因給藥途徑不同而產生截然不同的臨床後果。
1. 藥物分類與差異
- Dopamine Agonists (口服致效劑): 如 Bromocriptine、Cabergoline。常用於治療帕金森氏症或高泌乳激素血症。雖然會降低 TSH,但通常不至於造成嚴重臨床問題。
- Dopamine Infusions (靜脈輸注): 在加護病房 (ICU) 用於維持重症病患血壓的強心升壓藥。這是一個具備高度臨床風險的診斷陷阱。
2. ICU 中的「掩蓋效應 (Masking Effect)」
在重症監護環境下,Dopamine infusion 會導致醫源性的中樞性甲狀腺功能低下 (Central Hypothyroidism)。這不僅僅是數值的改變,更會干擾我們對病患原始甲狀腺狀態的判斷。
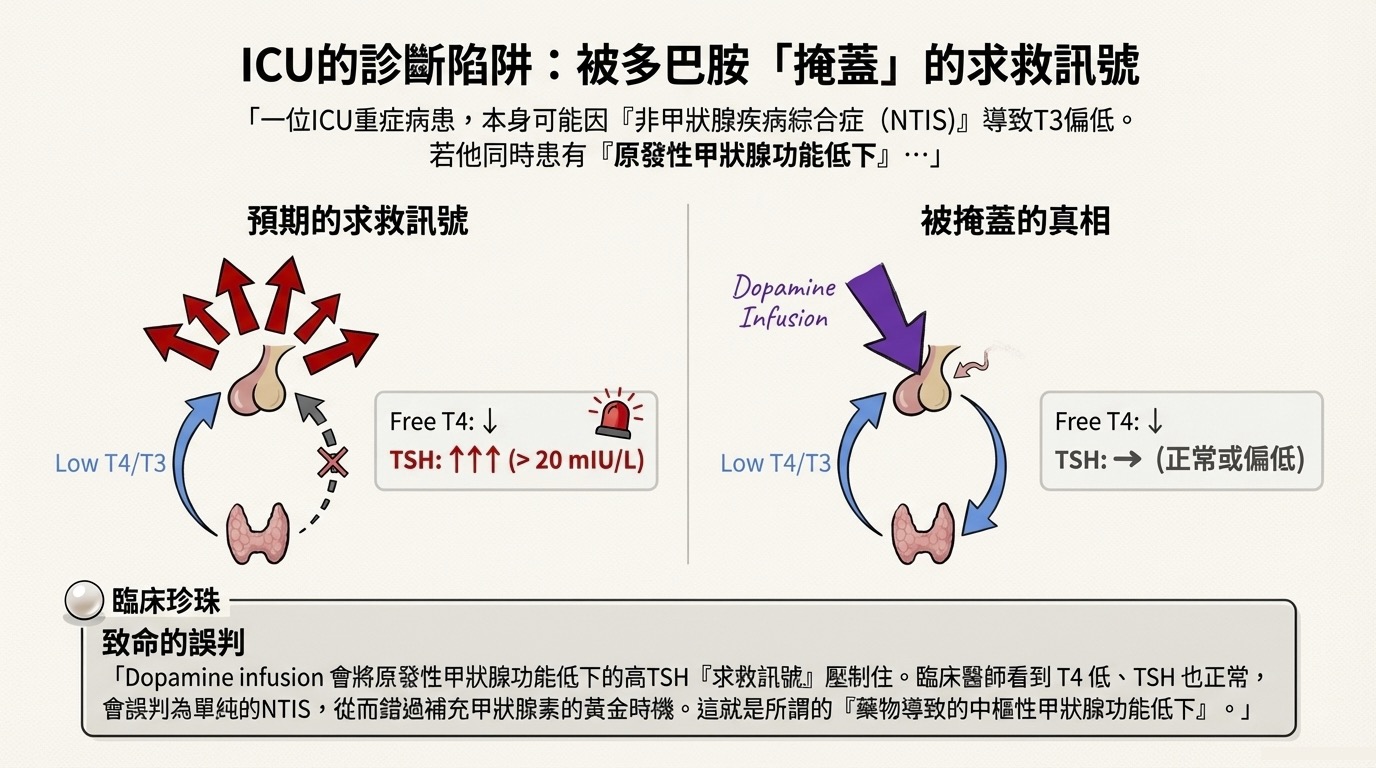
- 生理背景: 重症病患常伴隨「非甲狀腺疾病綜合症 (Nonthyroidal Illness Syndrome, NTIS)」,此時體內的 T3 因周邊轉換減少而呈現低值。
- 關鍵情境: 若該病患原本患有原發性甲狀腺功能低下 (Primary Hypothyroidism),其 TSH 本應因缺乏 T3/T4 的負回饋而大幅飆升(例如 mIU/L),這是身體發出的求救訊號。
- 陷阱機制: Dopamine infusion 強力作用於 D2R,將這個 TSH 的求救訊號硬生生「壓」回正常或偏低範圍。
- 臨床後果: 醫師看到「低 T4、TSH 正常/偏低」,誤以為這只是單純的重症反應 (NTIS),因而錯失診斷原發性甲狀腺低下及補充甲狀腺素的關鍵時機。
第二類機制:Somatostatin 的適應與暫時性抑制
Somatostatin analogs(如 Octreotide、Lanreotide)是治療肢端肥大症 (Acromegaly) 或 TSH 分泌瘤的主力藥物。
1. 生理機制
Somatostatin 會同時降低 TSH 分泌的 頻率 (Frequency) 與 振幅 (Amplitude)。理論上,這種雙重打擊應能極強力地壓制 TSH。
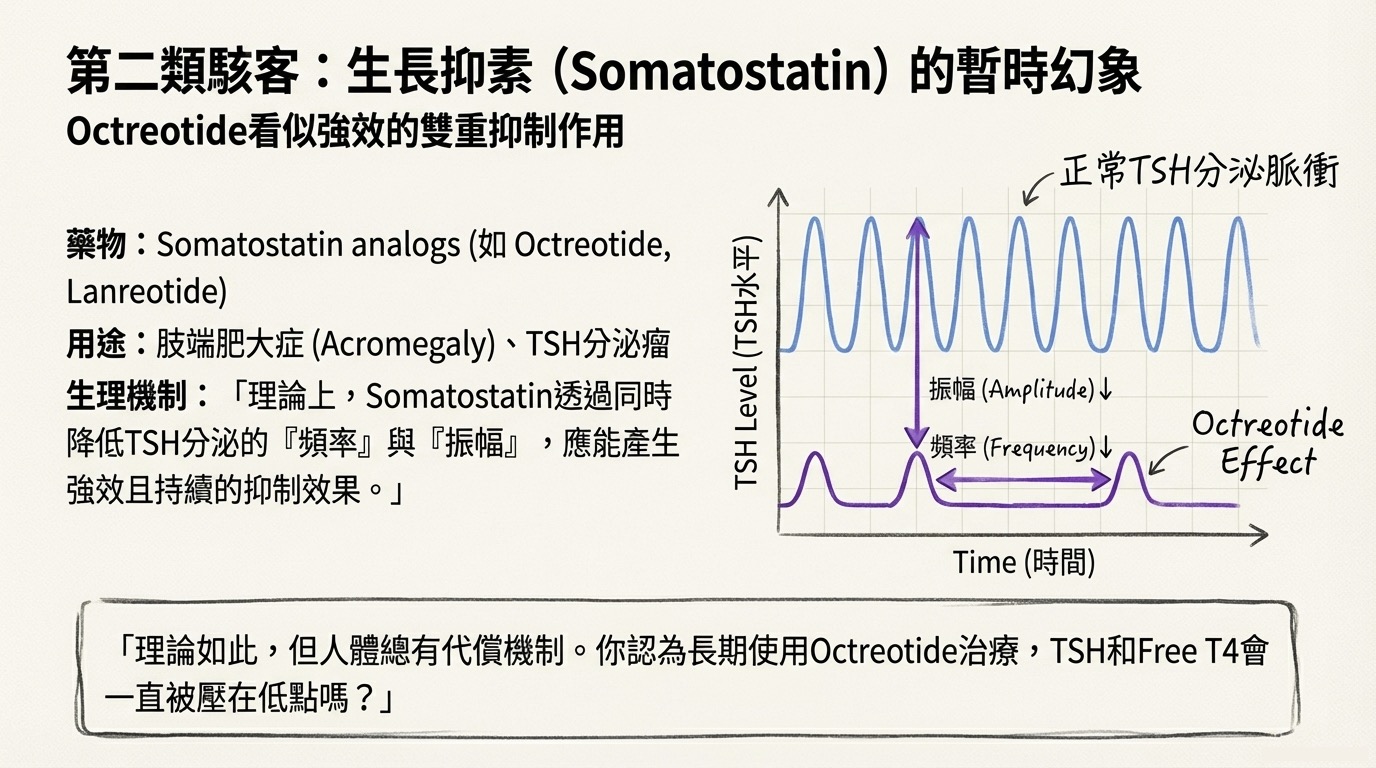
2. 長期治療的「適應 (Adaptation)」現象
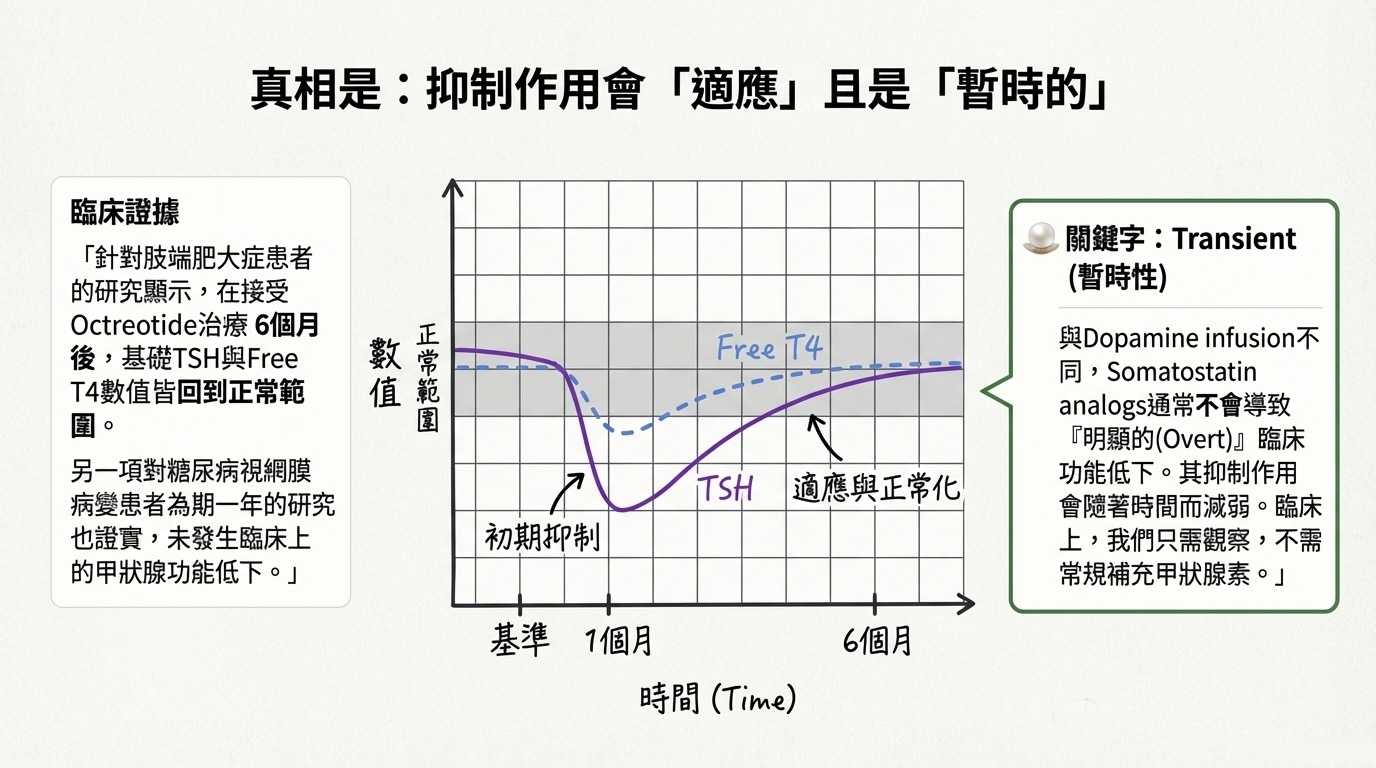 臨床數據顯示,生理系統存在強大的代償機制:
臨床數據顯示,生理系統存在強大的代償機制:
- 短期效應 (初期): 治療初期(如第 1 個月),TSH 與 TRH 的反應確實受到顯著壓抑。
- 長期效應 (> 6 個月): 文獻指出,肢端肥大症患者治療 6 個月後,基礎 TSH 和 Free T4 數值會回升至正常範圍 (Normal range)。
- 臨床結論: Somatostatin 對正常甲狀腺軸的抑制作用是 暫時的 (Transient)。即便治療一年(如糖尿病視網膜病變研究),雖 TSH 輕微下降,但極少發生具臨床意義的顯性甲狀腺功能低下 (Overt Hypothyroidism)。
第三類機制:Rexinoids 與核受體的分子風暴
 不同於上述作用於細胞膜受體的藥物,Rexinoids(如用於治療皮膚 T 細胞淋巴瘤的 Bexarotene)直接深入細胞核,其引發的甲狀腺功能低下遠比 Somatostatin 嚴重且持久。
不同於上述作用於細胞膜受體的藥物,Rexinoids(如用於治療皮膚 T 細胞淋巴瘤的 Bexarotene)直接深入細胞核,其引發的甲狀腺功能低下遠比 Somatostatin 嚴重且持久。
1. 分子生物學機制
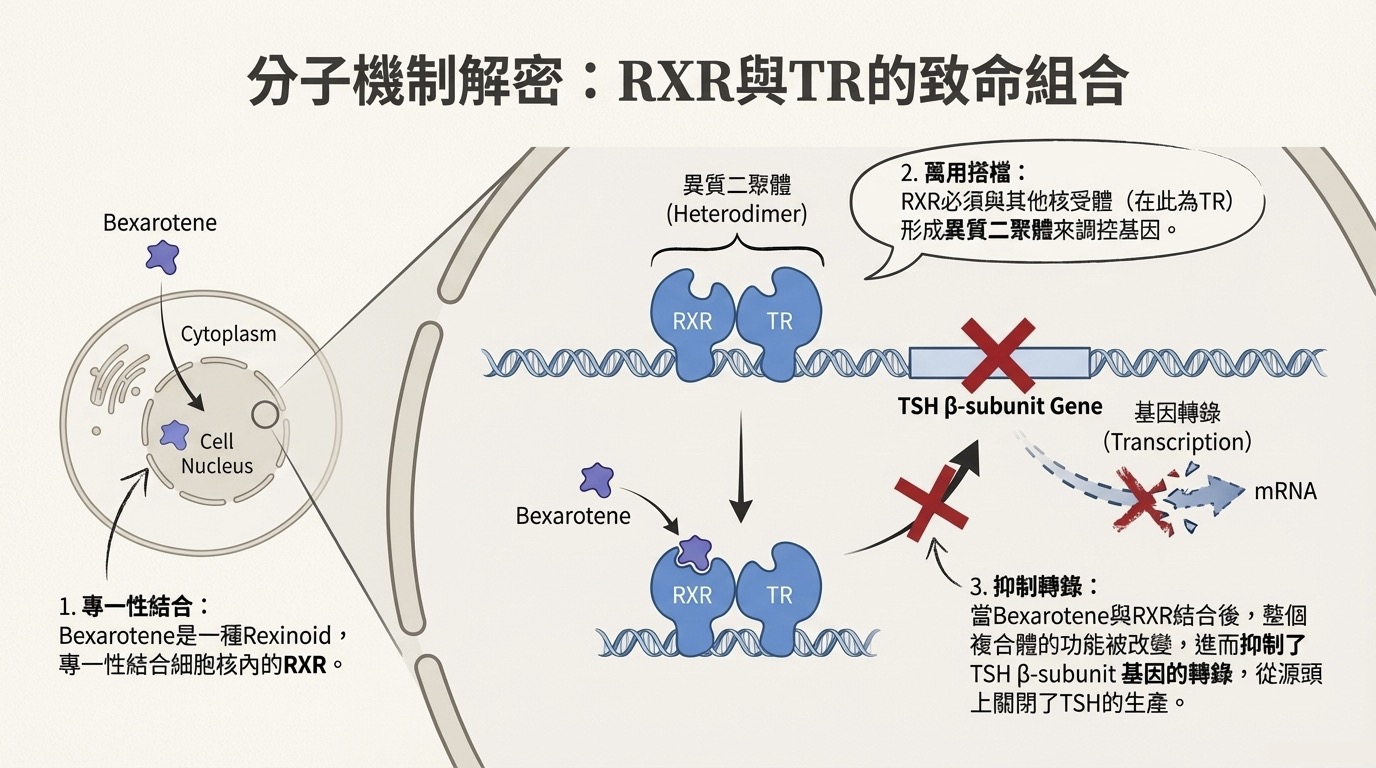
- 標靶受體: Bexarotene 專一性結合細胞核內的 Retinoid X Receptor (RXR)。
- 異質二聚體 (Heterodimer): RXR 是核受體超家族中的「萬用搭檔」。在調控 TSH 的情境下,RXR 必須與 甲狀腺素受體 (TR) 結合,形成 RXR-TR Heterodimer。
- 基因調控: 當 Bexarotene 結合上 RXR-TR 複合物後,會直接抑制 subunit 基因的轉錄 (Transcription)。
2. 臨床嚴重性

這不是暫時的適應,而是基因層級的阻斷。
- 數據證明: 研究顯示,27 位接受 Bexarotene 治療的患者中,幾乎所有人的 TSH 都下降,且約 70% (19位) 出現了顯性中樞性甲狀腺功能低下的臨床症狀(如遲鈍、水腫、無力)。
- 處置原則: 對於使用 Bexarotene 的患者,我們不能像使用 Octreotide 那樣僅作觀察,必須主動監測並給予甲狀腺素 (Levothyroxine) 補充治療。
第四類機制:腸胃道吸收的物理與化學障礙
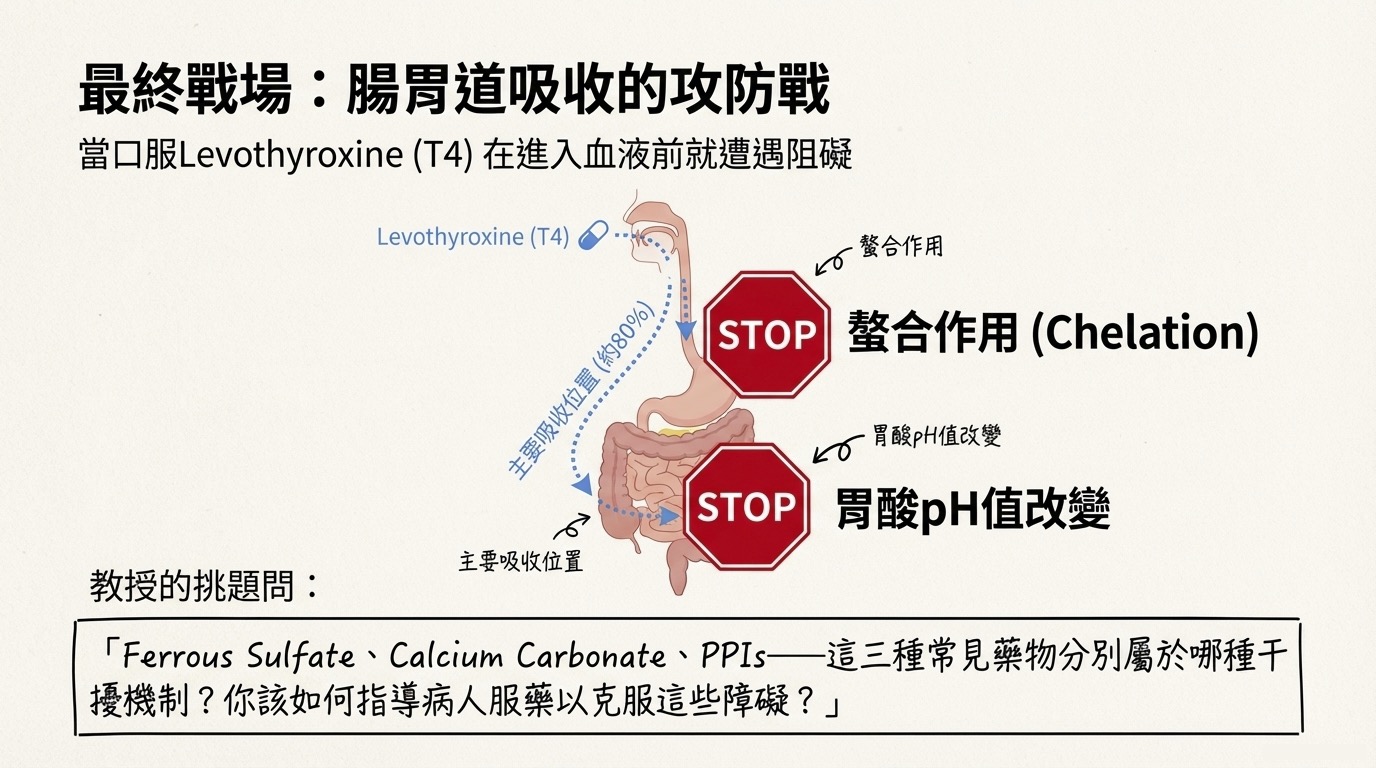 離開腦下垂體,我們來到口服 Levothyroxine (T4) 進入血液的必經之路——空腸 (Jejunum) 與迴腸 (Ileum)。約 80% 的 T4 在此吸收,但常受到兩大類藥物機制的干擾。
離開腦下垂體,我們來到口服 Levothyroxine (T4) 進入血液的必經之路——空腸 (Jejunum) 與迴腸 (Ileum)。約 80% 的 T4 在此吸收,但常受到兩大類藥物機制的干擾。
1. 螯合作用 (Chelation) / 形成不溶複合物
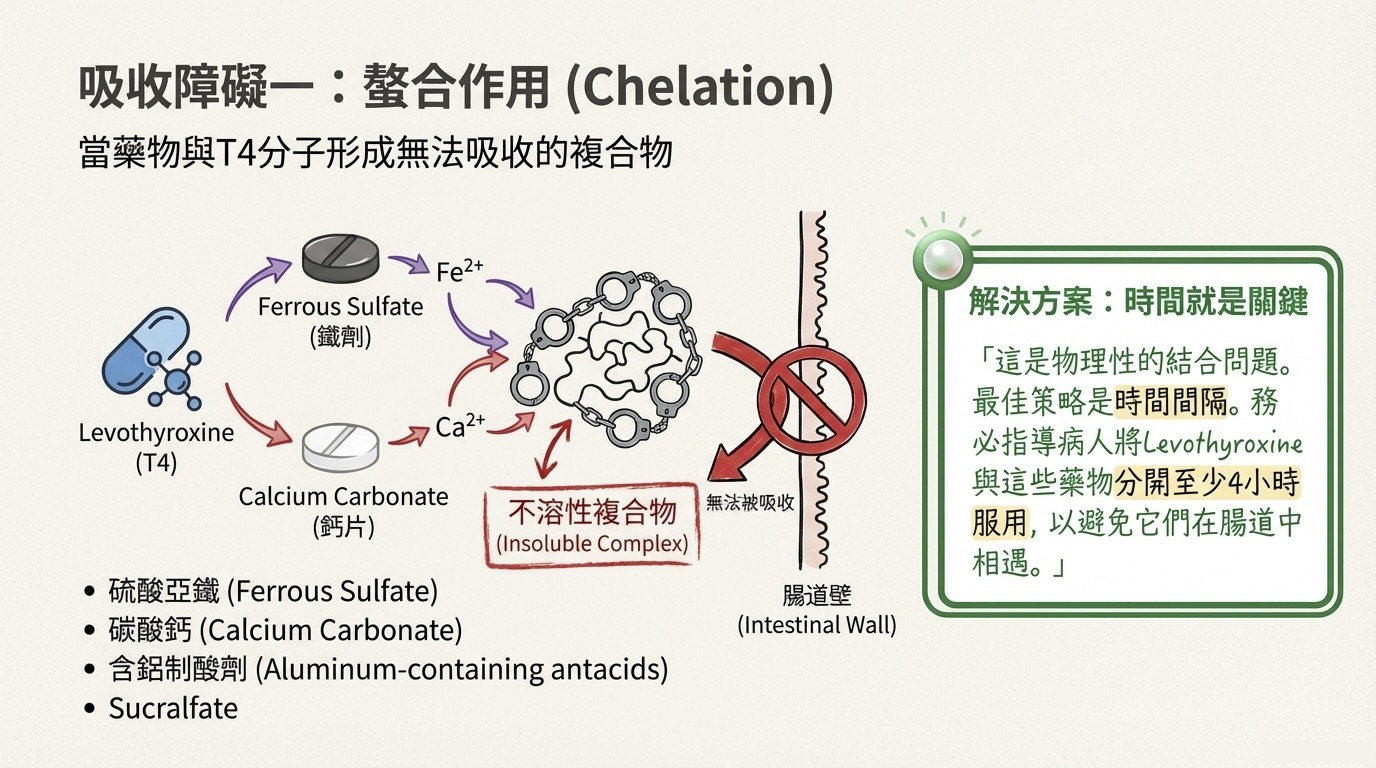
- 代表藥物:
- Ferrous Sulfate (鐵劑)
- Calcium Carbonate (碳酸鈣)
- 含鋁 (Aluminum) 制酸劑、Sucralfate
- 機制: 多價陽離子與 T4 分子在腸道內發生物理性結合,形成無法被吸收的不溶性複合物 (Insoluble complex)。
- 臨床珍珠 (Clinical Pearl): 此為物理混合問題。解決方案是「時間間隔」。建議病人將 T4 與這些藥物分開至少 4 小時服用。
2. pH 值改變與溶解度影響
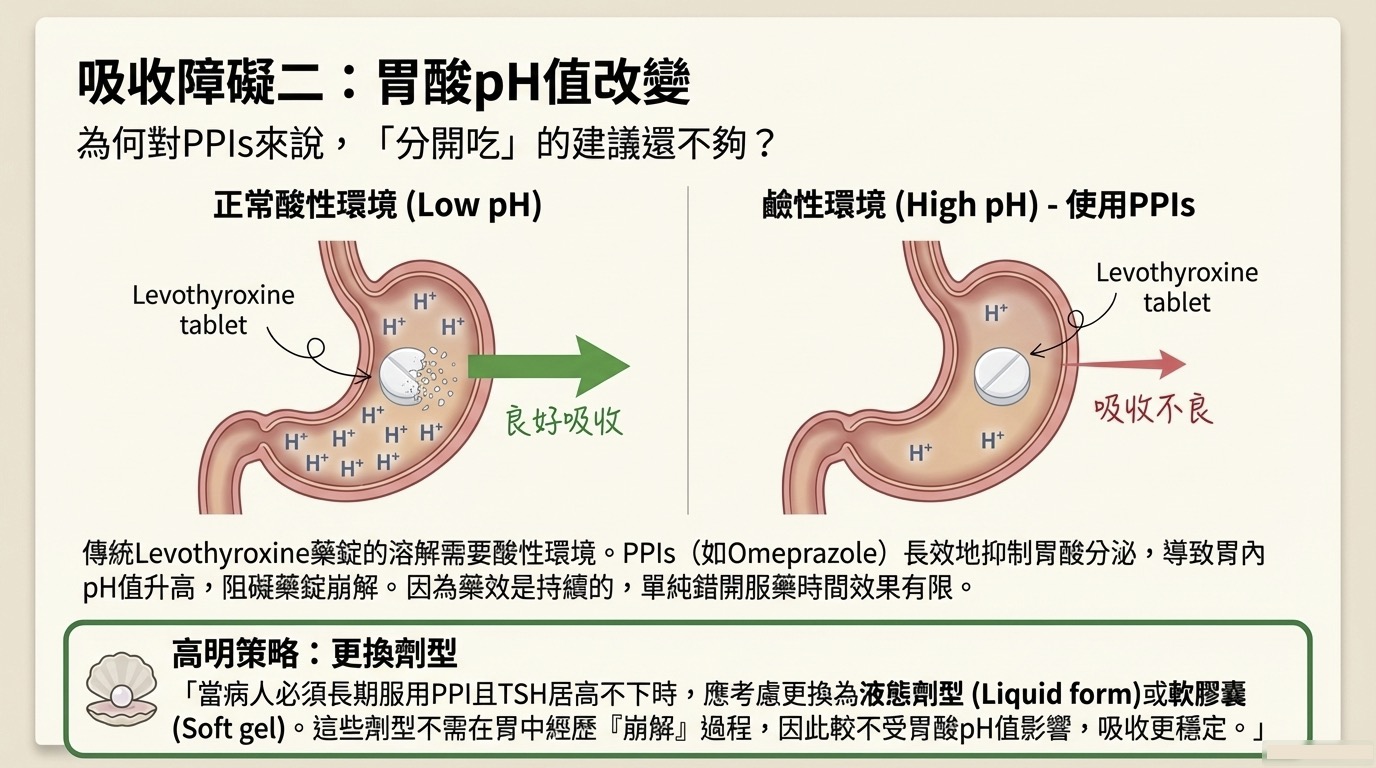
- 代表藥物: Proton Pump Inhibitors (PPIs, 如 Omeprazole)。
- 機制: 傳統的 Levothyroxine 藥錠需要在胃酸環境下進行崩解 (Dissolution) 才能溶解並被吸收。PPI 長效抑制胃酸分泌,導致胃內 pH 值上升,阻礙藥錠崩解。
- 為何「分開吃」無效? PPI 的藥效是持續性的(長效抑制 H+/K+ ATPase),單純錯開服藥時間無法解決低胃酸環境的問題。
- 高階處置 (Formulation Change): 若病人必須長期服用 PPI 且 TSH 居高不下,應考慮更換劑型:
- 液態 (Liquid form) 或 軟膠囊 (Soft gel)。
- 理由:這些劑型不需要經歷胃中崩解過程,因此其吸收率較不受 pH 值變化的影響。
總結圖表:藥物對甲狀腺軸的影響