Tirzepatide 臨床安全性綜述 — Part 1:核心器官毒性
綜述類型: 敘述性綜述(Narrative Review) 涵蓋主題: 消化道副作用、膽道疾病、胰臟安全性 文獻截止日: 2026-03-29 證據等級標示: ⬛ Strong | 🟧 Moderate | 🟨 Limited | ⬜ Expert opinion / Knowledge gap
前言
Tirzepatide(商品名 Mounjaro/Zepbound)為全球首個獲准上市的 GIP/GLP-1 雙受體激動劑(dual incretin receptor agonist),分別於 2022 年取得 FDA 批准用於第二型糖尿病(T2DM),2023 年取得肥胖適應症。其雙受體機制帶來卓越的血糖控制與減重效果(SURPASS 系列試驗 HbA1c 降低可達 −2.6%;SURMOUNT 系列體重減少可達 −22.5%),但同時引發對多器官系統安全性的關注 12。
本綜述聚焦 tirzepatide 三大核心安全性議題——消化道副作用、膽道疾病風險及胰臟安全性——整合超過 50 篇關鍵文獻(含 meta-analysis、Phase 3 RCT、藥物警戒研究及個案報告),以系統性方式呈現現有證據、爭議焦點與臨床建議。

第一章:消化道副作用
1.1 發生率概覽
消化道(GI)副作用是 tirzepatide 最常見的不良反應,也是臨床使用中最主要的耐受性障礙。根據兩大試驗平台的彙整數據,GI 副作用發生率因適應症族群而有顯著差異:
T2DM 族群(SURPASS 系列): SURPASS-1 至 SURPASS-5 的匯總分析顯示,噁心(nausea)發生率 12–24%、腹瀉(diarrhea)12–22%、嘔吐(vomiting)2–13% 3。以 SURPASS-2(tirzepatide vs. semaglutide 1mg)為最直接的頭對頭比較,tirzepatide 15mg 組的噁心率為 22.1%、嘔吐率 9.8%,均略高於 semaglutide 1mg 組(17.9% / 8.3%)4。
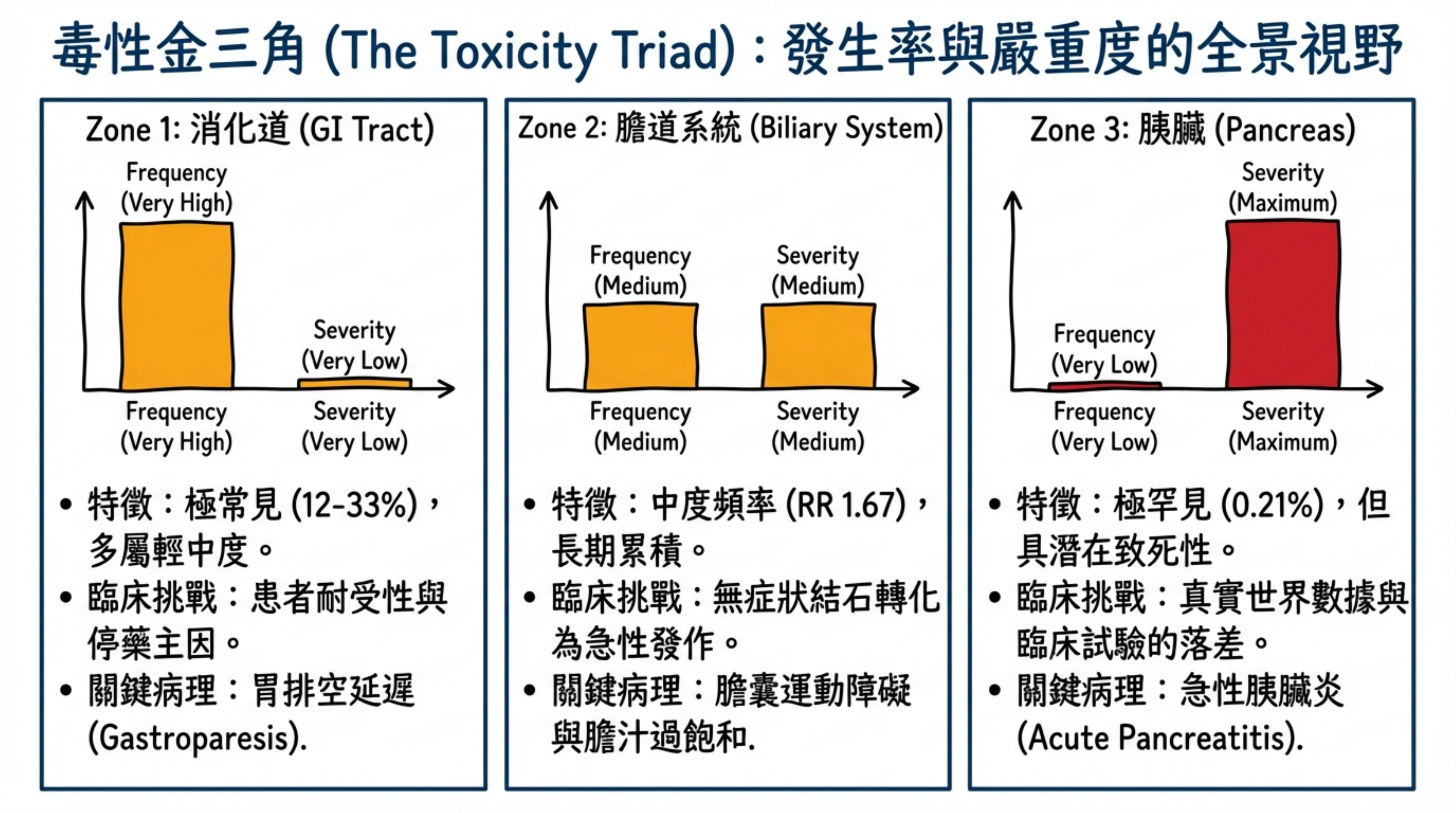
肥胖族群(SURMOUNT 系列): GI 發生率顯著高於 T2DM 族群。SURMOUNT-1 至 SURMOUNT-4 的彙整分析顯示,整體至少出現一種 GI 副作用(噁心/嘔吐/腹瀉)的比例為 28–48%,其中噁心高達 24–33%、腹瀉 18–23%、嘔吐 8–12% 56。此差異可能源於:(a) 肥胖族群主要使用較高劑量(10–15mg);(b) T2DM 患者因長期 GI 自主神經病變可能導致症狀報告偏低。
統合分析數據(⬛ Strong): Karrar et al.(2023)基於 6 個 RCT、N=4,586 的 meta-analysis 顯示,相較於混合對照組,tirzepatide 的噁心 RR=2.90(1.89–4.44)、腹瀉 RR=2.07(1.60–2.68)、嘔吐 RR=2.69(1.67–4.36)、便秘 RR=3.08(1.83–5.20)、食慾下降 RR=5.04(3.01–8.45)7。
備註: 此 meta-analysis 的對照組為混合比較組(placebo + semaglutide 1mg + insulin degludec),RR 並非純粹對安慰劑的估計,解讀需謹慎。此外,噁心的異質性極高(I² 89–94%),統計合併的可靠性存在限制。
1.2 劑量依賴性與時間分布
GI 副作用呈現明確的劑量依賴性(⬛ Strong)。以 SURMOUNT-1 為例,噁心從 5mg 的 24.6% 升至 10mg 的 33.3%;嘔吐從 8.3% 升至 15mg 的 12.2%,呈單調遞增趨勢 5。但部分指標(如噁心在 10mg 與 15mg 間持平或微降、便秘在 15mg 反而較低)顯示劑量-反應關係並非完全線性。
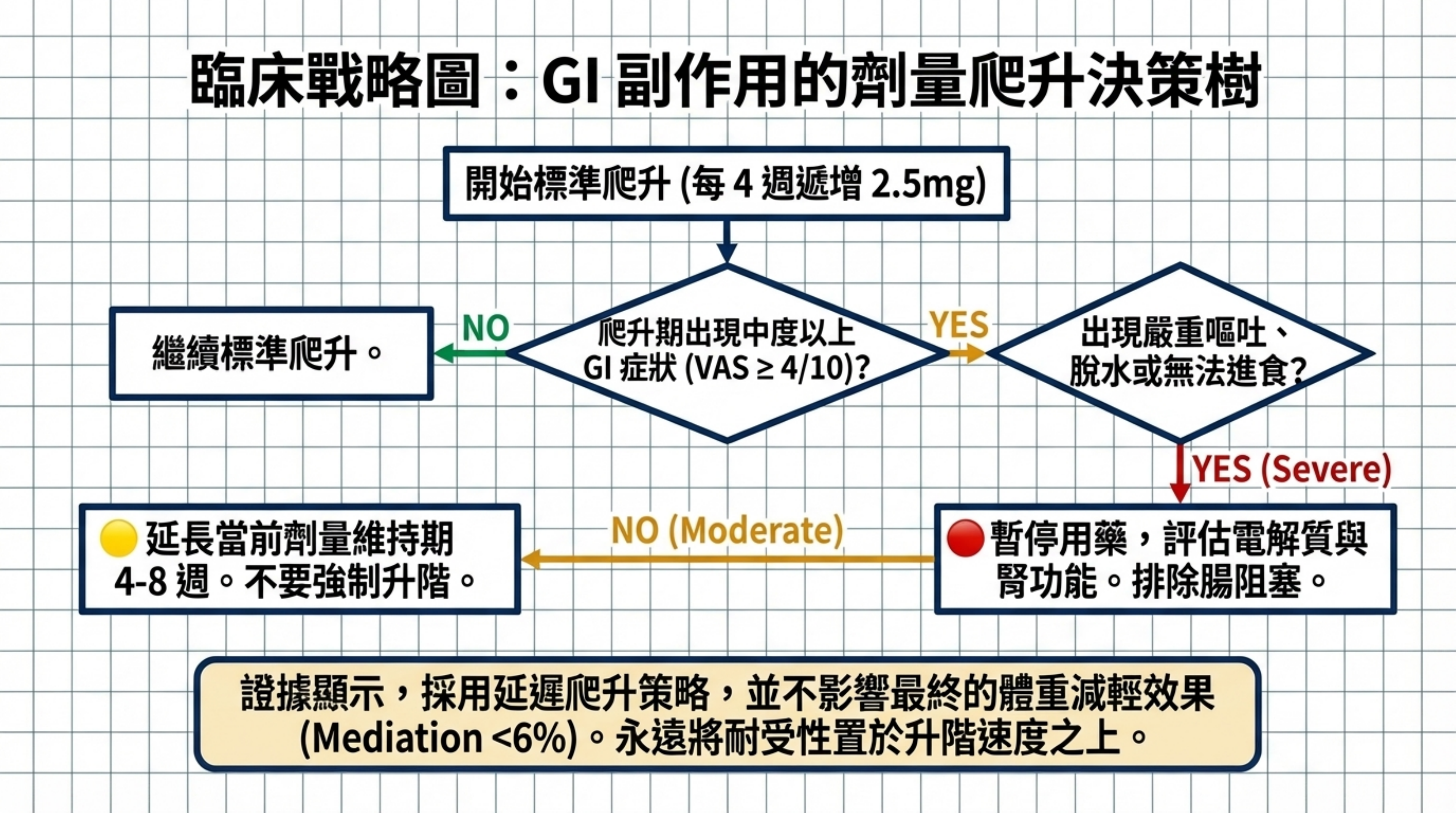
在時間分布上,GI 副作用主要集中於劑量爬升期(dose escalation period),達到維持劑量後多數在第 16–20 週後顯著緩解(⬛ Strong)36。SURPASS 和 SURMOUNT 的彙整分析均確認,體重減輕的效果獨立於 GI 副作用的報告(GI 症狀僅介導 <6% 的體重下降效果),意味著即使 GI 症狀緩解,減重效果仍可維持 36。
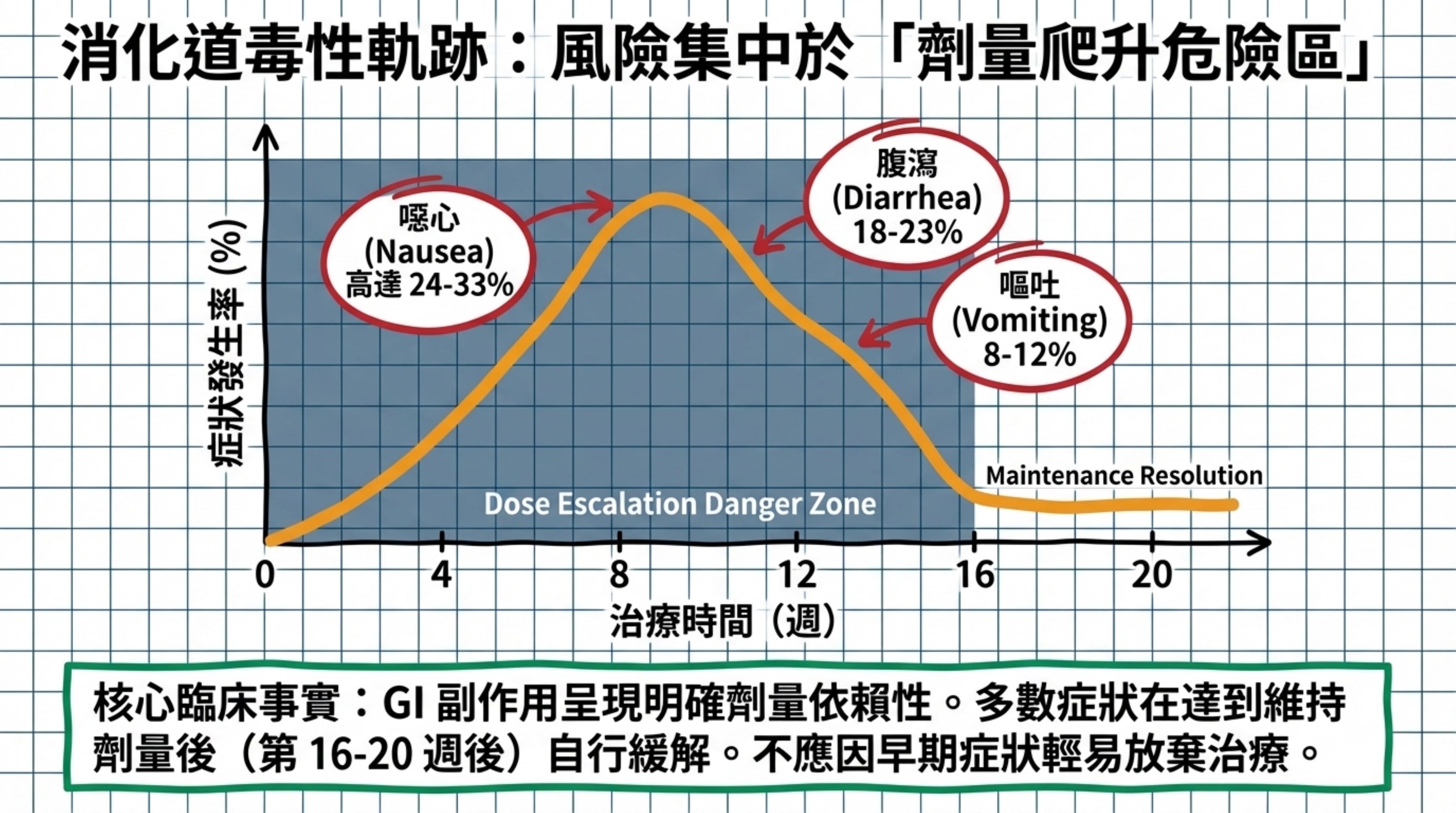
因 GI 副作用導致的停藥率在各試驗間差異較大(1.0–10.5%),取決於劑量、試驗設計與族群特性。
1.3 與 Semaglutide 的比較——一場未完的辯論
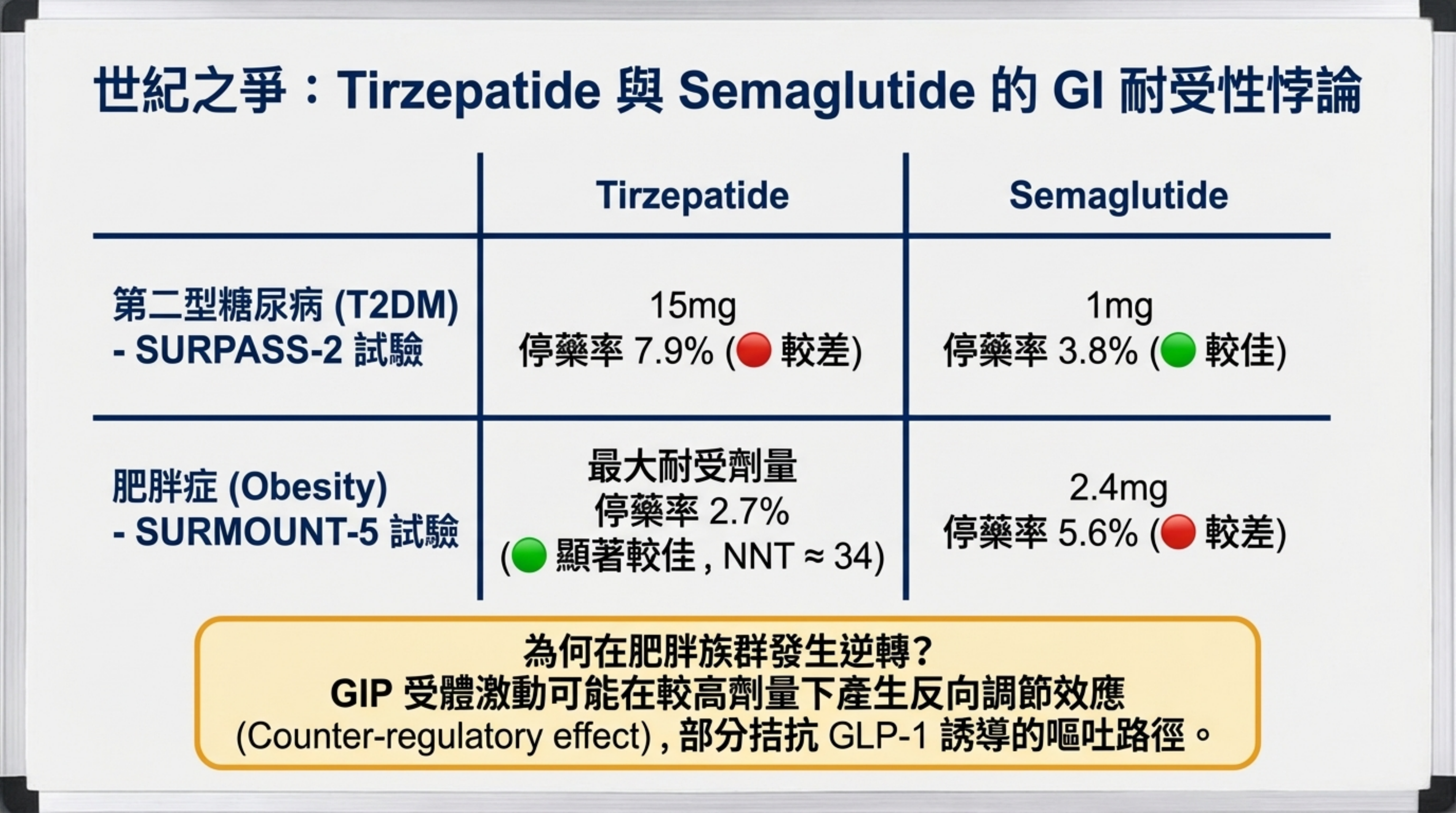
Tirzepatide 與 semaglutide 的 GI 耐受性比較是臨床上備受關注的問題,但現有數據呈現因適應症而異的矛盾結果(🟧 Moderate):
T2DM 族群不利於 tirzepatide: SURPASS-2 中,tirzepatide 15mg 的 GI 停藥率為 7.9%,顯著高於 semaglutide 1mg 的 3.8%(NNH ≈ 24)4。
肥胖族群有利於 tirzepatide: SURMOUNT-5(首個肥胖族群頭對頭比較,tirzepatide 最大耐受劑量 vs. semaglutide 2.4mg)顯示,tirzepatide 的 GI 停藥率僅 2.7%,顯著低於 semaglutide 的 5.6%(保護性 NNT ≈ 34)8。ACG 2024 會議摘要進一步顯示,tirzepatide 在噁心/嘔吐(OR 0.55)、腹瀉(OR 0.56)、胃輕癱(OR 0.36)等所有主要 GI 指標上均優於 semaglutide。
證據批判: 上述兩項比較的劑量不對等是核心問題。SURPASS-2 使用 semaglutide 1mg(非最大劑量),而 SURMOUNT-5 使用最大耐受劑量設計。在缺乏等效劑量(等效 HbA1c 降幅或等效體重減少)下的頭對頭比較前,「tirzepatide GI 耐受性優於 semaglutide」的結論僅在肥胖族群、最大耐受劑量設計下成立。真實世界研究(Blonde et al.,N=41,222)則顯示兩者 GI AE 發生率相似 9。GIP 受體激動可能部分拮抗 GLP-1 介導的胃排空延遲,提供了機制上的合理解釋,但尚需更嚴謹的驗證。
1.4 胃輕癱與腸阻塞
胃輕癱(Gastroparesis): GLP-1 RA 類別整體與胃輕癱風險升高相關(aHR 3.7;95% CI 1.2–11.9),但此估計來自僅含 liraglutide 和 semaglutide 的研究,tirzepatide 上市前數據不包括在內 10。機制上,GLP-1 受體激動直接抑制胃腸蠕動(vagus-mediated),而 GIP 可能具部分反向調節效應。ACG 2024 初步數據顯示 tirzepatide 的 de novo gastroparesis 風險較 semaglutide 低 64%(OR 0.36),但此數據尚未經同儕審查。

腸阻塞(Ileus): GLP-1 RA 整體的腸阻塞 HR 為 4.2(95% CI 1.0–17.4),CI 極寬 10。FDA 已根據上市後監測數據(FAERS 中累計 90 例 GLP-1/tirzepatide 相關 ileus 報告)更新 Mounjaro 和 Zepbound 仿單,加入 ileus 警示 11。個案報告亦記錄了低劑量 tirzepatide 即引發急性功能性胃出口阻塞的案例 12。
臨床管理: 術前管理是 GI 安全性的重要面向。根據 Jalleh et al.(2025)的回顧,GLP-1 RA 使用者的殘留胃內容物增加 5–10 倍,擇期手術前建議停用 tirzepatide 至少 1 週;急診手術應告知麻醉科採快速充序插管(RSI)預防 13。
第二章:膽道疾病風險
2.1 風險量化
膽道疾病是 GLP-1 RA 類別已確立的安全信號,tirzepatide 亦不例外。
膽石症(Cholelithiasis)(🟧 Moderate): Gong et al.(2024)基於 12 個 RCT(N=12,351)的 meta-analysis 顯示 tirzepatide 的膽石症 RR=1.67(95% CI 1.14–2.44;I²=0%),即相對風險增加 67% 14。以安慰劑基礎風險 ~1% 估算,絕對風險差約 0.67%,NNH ≈ 149(95% CI 約 80–350)。
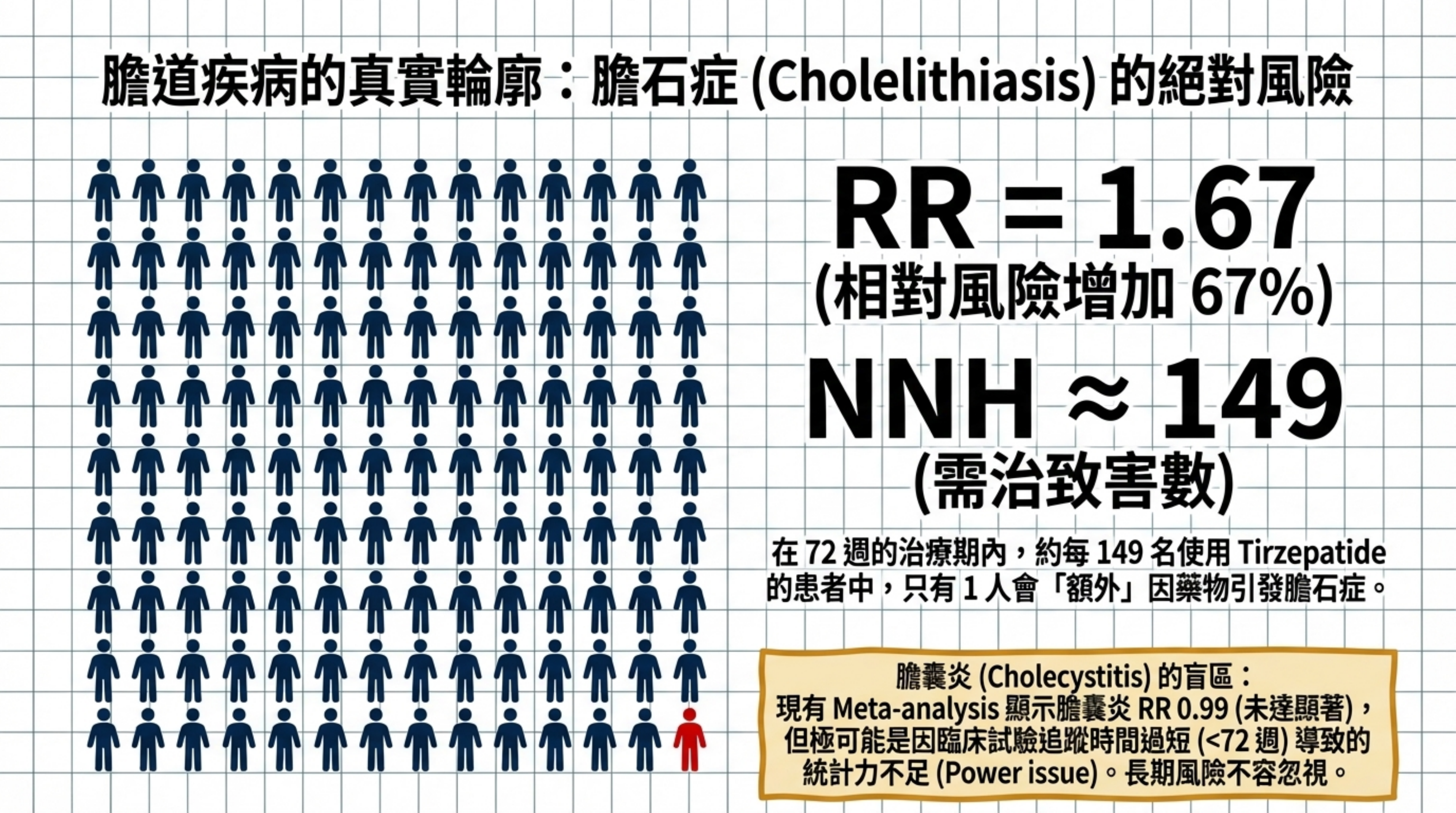
膽囊炎(Cholecystitis)(🟨 Limited): 同一 meta-analysis 顯示 tirzepatide 的膽囊炎 RR=0.99(95% CI 0.48–2.03),未達統計顯著 14。然而,95% CI 極寬,反映事件數嚴重不足(power 問題)。根據 SURMOUNT-1+2 彙整數據,膽囊炎發生率為 tirzepatide 0.7% vs. placebo 0.2%(NNH ≈ 200),提示臨床上仍有關聯。
GLP-1 RA 類別比較: GLP-1 RA 整體膽道風險已由 Sharma et al.(2022)的 76 個 RCT mega-analysis(N=103,371)確立:整體 cholelithiasis RR=1.37(1.23–1.52)、cholecystitis RR=1.36(1.14–1.62)15。Tirzepatide 的 cholelithiasis RR(1.67)略高於 semaglutide(1.28)但低於 liraglutide(1.79),可能反映其更大幅度的體重下降。LEADER 試驗(liraglutide,3.5–5 年追蹤)顯示的 HR=1.60,提示 tirzepatide 現有 72 週數據可能低估長期膽道風險。
2.2 機制辯論:快速減重 vs. 藥物特異性
膽道風險的機制歸因是本主題最核心的科學辯論:
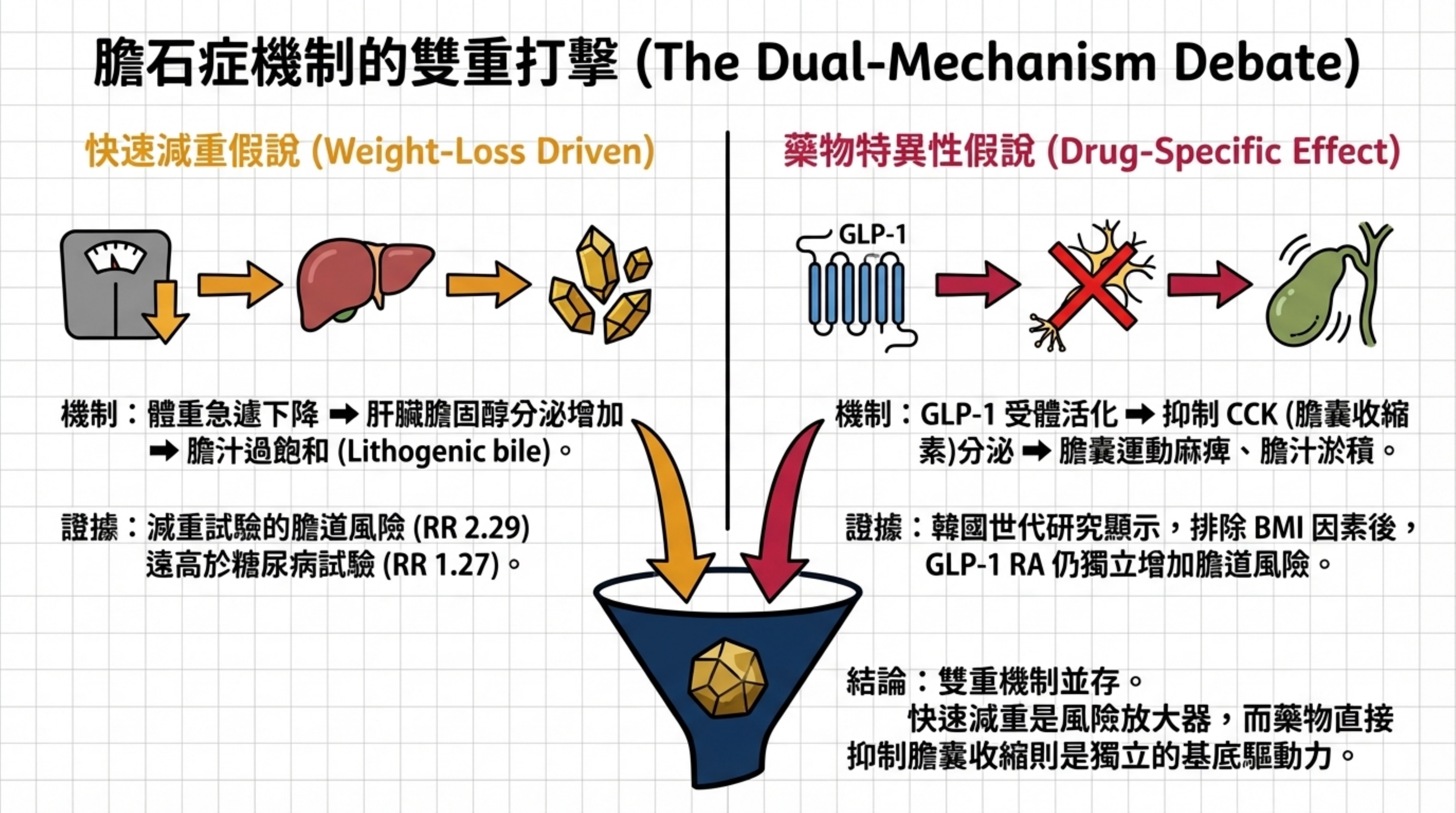
快速減重假說(⬛ Strong): 快速減重導致肝臟膽固醇合成增加、膽汁過飽和(lithogenic bile)、進食減少致膽囊收縮刺激降低。體重管理試驗中 GLP-1 RA 膽道 RR=2.29,遠高於 T2D 試驗的 RR=1.27(交互作用 p<0.001),體重下降幅度是最強預測因子 15。這一模式亦見於減重手術和極低熱量飲食。
藥物特異性假說(🟧 Moderate): (a) GLP-1 infusion 在健康人和 T1DM 患者中直接抑制餐後 CCK 分泌,CCK 是膽囊收縮的主要刺激素 16;(b) GLP-1 RA 延長膽囊再充填時間,獨立於體重變化 17;(c) 韓國全國性世代研究顯示,無論 BMI 分層(肥胖 vs. 非肥胖),GLP-1 RA 均增加膽道風險,BMI 並非顯著的效應修飾因子(effect modifier),支持藥物本身具獨立效應 18;(d) FAERS 信號在控制適應症混淆後仍存在 19。
GIP 成分的額外效應(🟨 Limited): Tirzepatide 的 GIP 受體激動可能促進膽囊鬆弛,理論上形成「GIP-mediated gallbladder relaxation + GLP-1-mediated CCK suppression」的雙重機制。然而,此假說僅有動物/細胞層級的間接證據,缺乏人體膽囊運動功能的直接測量數據。
共識結論: 兩種機制並存(雙重機制),快速減重是主要的風險放大器,藥物本身的 GLP-1 受體效應是基底風險的獨立貢獻者。各 GLP-1 RA 間的風險差異(liraglutide > tirzepatide > semaglutide > exenatide)不完全與體重下降幅度成正比,進一步支持藥物特異性成分的存在。
2.3 現有 RCT 數據的充分性
現有 RCT 在評估膽道風險上存在多項重要限制:(a) 最長追蹤僅 72 週,膽石形成為慢性過程;(b) 多數 SURPASS 試驗未將膽道事件列為預設安全終點(僅被動收集 AE);(c) meta-analysis 中對照組異質性高(placebo、basal insulin、GLP-1 RA 混合);(d) 劑量-反應關係出現矛盾結果(zero events problem 導致的統計假象)。因此,現有數據在短期(<2 年)cholelithiasis 風險估計上「可用但不充分」,長期 cholecystitis 風險則「可能被嚴重低估」。
2.4 臨床建議
- 治療前篩查: 高風險患者(女性、>40 歲、BMI ≥30、膽石家族史、多次懷孕史)建議腹部超音波。有症狀膽石者應先治療膽石再開始 tirzepatide。
- 治療中監測: 每次回診詢問右上腹/上腹痛(特別是餐後);高風險者治療 6 個月後複查超音波。
- Ursodiol 預防用藥(⬜ 無直接 RCT): 對 BMI >35 且預期快速減重 >15% 的高風險患者,可考慮 ursodiol 500–600 mg/day,尤其在體重下降最快的前 6 個月。此為 off-label 用藥,基於減重手術領域的間接類比證據(UPGRADE trial, NNT ≈ 15)20。
- 膽道事件處置: 急性膽囊炎應立即停藥;膽囊切除術後可重啟 tirzepatide。

第三章:胰臟安全性
3.1 急性胰臟炎

RCT 層級(⬛ Strong): 跨越三個年代(2014、2020、2025)的 GLP-1 RA RCT meta-analysis 一致未發現統計顯著的胰臟炎風險升高。Tirzepatide 特異性數據:Kamrul-Hasan et al.(2024)基於 17 個 RCT(N=14,645)的 meta-analysis 顯示,各劑量 RR 均無統計顯著差異(5mg RR=2.04 [0.27–15.69];10mg RR=0.63;15mg RR=1.26;合計 RR=1.46 [0.59–3.61])21。SURMOUNT 試驗中,tirzepatide 組 0.21% vs. placebo 0.24%;SURPASS-2 中 tirzepatide 各劑量 0–0.4% vs. semaglutide 0.6%,均無超額風險 45。
真實世界數據(🟧 Moderate): FAERS 分析顯示 tirzepatide 的胰臟炎 ROR 為 3.63–7.18,為不成比例報告信號 1122。但 FAERS 為被動報告系統,受 Weber effect、notoriety bias、刺激性報告等多重偏誤影響,不能建立因果關係。
證據批判——信號是否為真? 支持「人為」的論點包括:(a) 偵測偏誤(RCT 中腹痛被更積極調查);(b) 適應症混淆(肥胖/T2D/高 TG 本身增加胰臟炎風險);(c) 三個年代的 RCT meta-analysis 一致陰性。支持「信號有一定真實性」的論點包括:(a) FAERS ROR 值較高;(b) 個案報告顯示時間關聯性;(c) Wen et al.(2025)62 個 RCT 的未分層分析 RR=1.44(p=0.009),雖按背景用藥分層後消失。
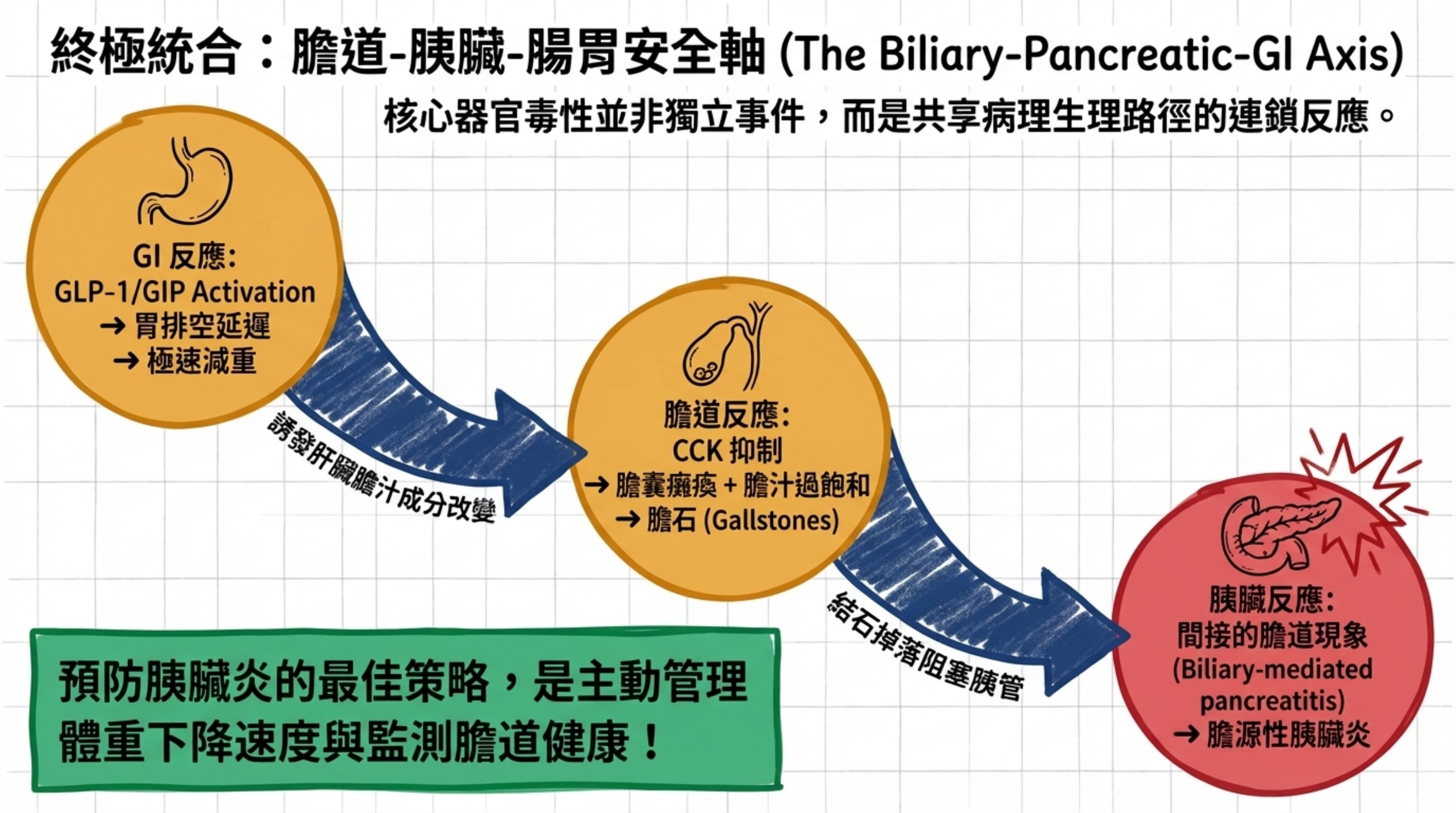
新興假說——膽道介導的胰臟炎(🟨 Limited): Koren et al.(2025)提出,GLP-1 RA 的「胰臟信號」可能為間接膽道現象——GLP-1 RA 抑制 CCK → 膽囊功能障礙 → 膽汁淤積/膽石 → 膽源性胰臟炎,並非胰腺直接毒性。此假說合理地串聯了本綜述第一章與第二章的發現。
3.2 Amylase/Lipase 變化
Tirzepatide 治療後,血清 amylase 升高 +33–38%、lipase 升高 +31–42%(⬛ Strong)21。這些無症狀的酵素升高為可逆的藥理學效應,與臨床胰臟炎風險不相關。機制假說為 GLP-1 受體在胰腺腺泡細胞的少量表達觸發酵素釋放。
臨床建議(⬛ Strong):不建議對無症狀患者常規監測 amylase/lipase。 無症狀的孤立性酵素升高不應導致停藥。僅在有症狀(持續腹痛、噁心/嘔吐)時才測定,且以 lipase 為優先指標(更高特異性)21。

3.3 胰臟癌長期風險
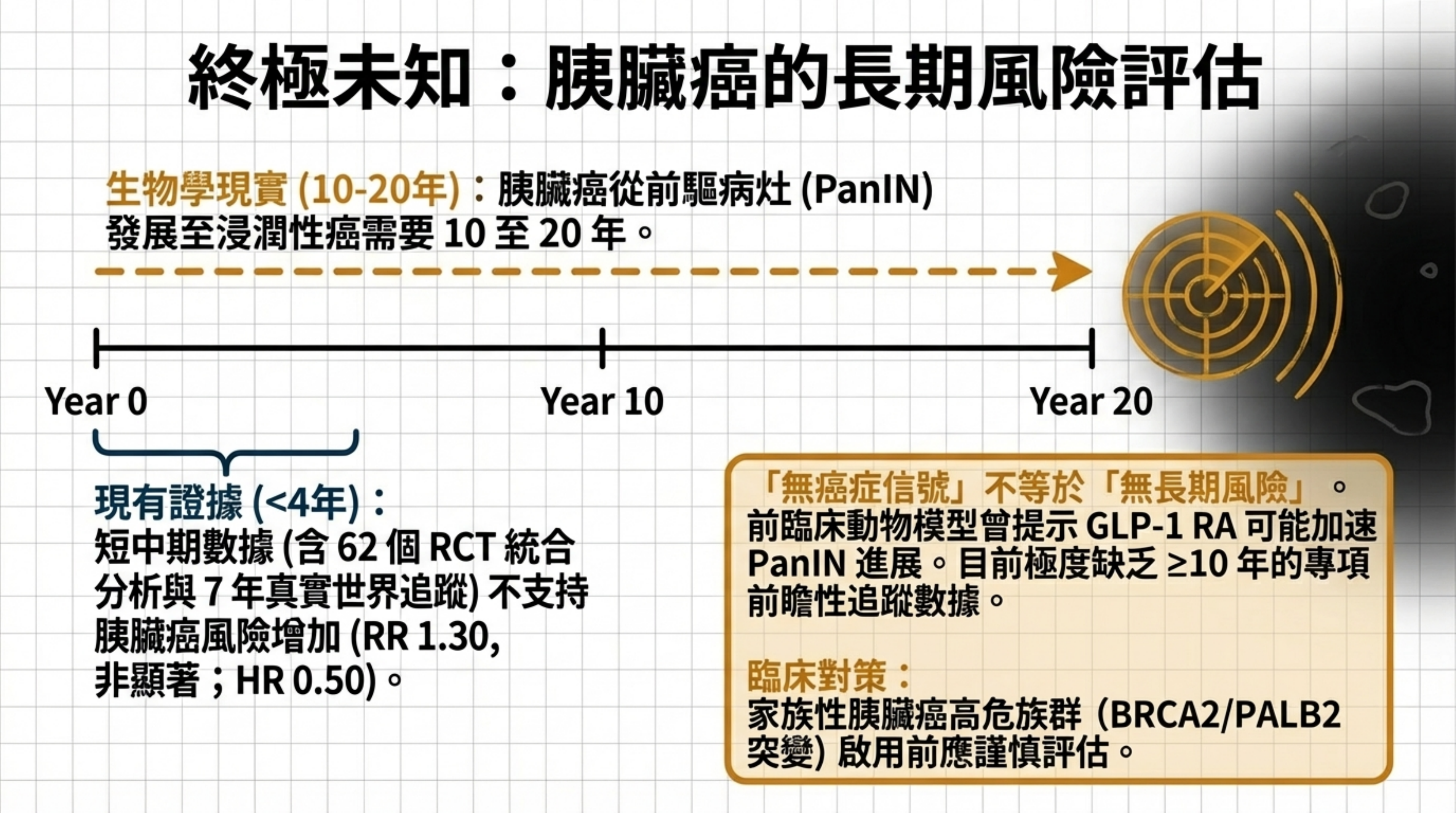
短中期數據不支持風險增加(🟧 Moderate): RCT meta-analysis(62 個 RCT)顯示胰臟癌 RR=1.30(0.86–1.97),無統計顯著差異 23。GI 癌症專項 meta-analysis(90 個 RCT,N=124,791)顯示 RR=1.05(0.77–1.43)24。以色列 Clalit 世代(N=543,595,7 年追蹤)顯示 GLP-1 RA vs. basal insulin 的胰臟癌 HR=0.50(0.15–1.71),反而傾向保護 25。SURMOUNT 試驗中無胰臟癌病例報告。
關鍵缺口(⬜ Knowledge gap): 胰臟癌的惡性進程通常需要 10–20 年(從 PanIN 前驅病灶到浸潤性癌),tirzepatide 核准時間僅 4 年,特異性長期數據完全不足。前臨床研究(Koehler et al.,2012)在高劑量 exenatide + Kras G12D 突變小鼠中觀察到 PanIN 加速和慢性胰臟炎 26,但超藥理劑量和特殊易感基因動物模型的外推性存疑。
3.4 致死性個案報告
2025 年,Mayo Clinic 報告首例 tirzepatide 致死性壞死性胰臟炎(PMID 40270999),患者在第 2–4 劑後 4 天發作 27。另有案例報告記錄從 semaglutide 轉換至 tirzepatide 後 2 天出現急性胰臟炎(PMID 39834977)。雖然極為罕見,這些案例提醒臨床醫師需維持警覺。
3.5 GIP/GLP-1 雙重激動是否帶來額外風險?
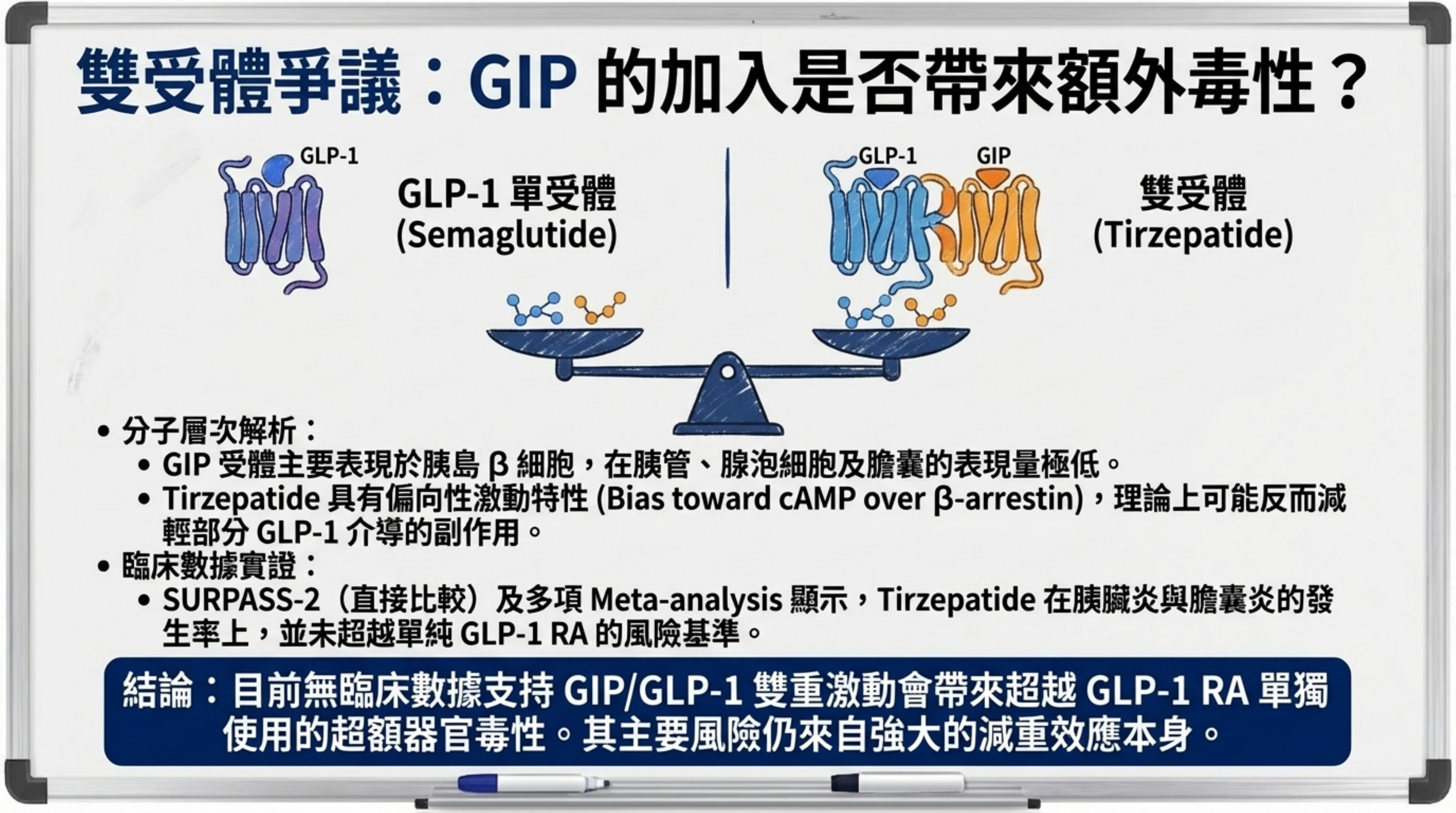
現有臨床數據不支持此論點(⬛ Strong)。SURPASS-2 中 tirzepatide 各劑量的胰臟炎率(0–0.4%)不高於 semaglutide(0.6%);tirzepatide 15mg 的 lipase 升高幅度與 GLP-1 RA 相似,不呈現超加性效應 421。GIP 受體在胰管腺體和腺泡細胞的表達遠低於 GLP-1 受體,前臨床中 GIP 特異性的胰腺外分泌毒理學資料極為有限。

跨主題交互分析:膽道-胰臟-GI 安全性軸
Part 1 三大主題並非獨立,而是通過共享的病理生理路徑緊密交織:
Tirzepatide
├── GLP-1 RA 效應
│ ├── 胃排空延遲 ──→ GI AE(噁心、嘔吐)
│ ├── CCK 抑制 ──→ 膽囊動力障礙 ──→ 膽石症
│ │ └──→ 膽源性胰臟炎
│ └── 胰腺腺泡細胞 GLP-1R 激動 ──→ 酵素釋放(amylase/lipase↑)
│
├── GIP RA 效應
│ ├── 膽囊鬆弛?(假說)──→ 額外膽道風險?
│ ├── 部分拮抗 GLP-1 胃排空延遲?──→ GI 耐受性改善?
│ └── 胰腺外分泌效應?(完全未知)
│
└── 快速減重
├── 膽固醇過飽和 ──→ 膽石形成(主要驅動力)
└── 進食減少 ──→ 膽囊收縮刺激↓ ──→ 膽汁淤積
優先知識缺口(按臨床重要性排序)
| 優先級 | 缺口 | 說明 |
|---|---|---|
| Critical | 等效劑量下 tirzepatide vs. semaglutide GI 和膽道直接比較 | 現有頭對頭比較因劑量不等效而無法確切結論 |
| Critical | Tirzepatide ≥2 年長期安全性數據 | 膽道和胰臟風險可能隨時間累積 |
| Critical | 膽囊運動功能直接測量研究 | SURPASS/SURMOUNT 均未納入系統性膽囊超音波 |
| Critical | 膽道介導胰臟炎的機制驗證 | 串聯膽道-胰臟安全性軸的關鍵假說 |
| Important | GIP 受體在膽囊和胰腺的獨立效應 | 區分 tirzepatide 與純 GLP-1 RA 安全性特徵的核心問題 |
| Important | Ursodiol 預防 GLP-1 RA 膽石的 RCT | 目前為 off-label 使用 |
| Important | 特殊族群安全性(≥75 歲、腎功能不全、既有 gastroparesis) | 前瞻性數據缺乏 |
| Exploratory | 10–20 年胰臟癌前瞻性登錄研究 | 胰臟癌潛伏期遠超現有追蹤期 |
結語

Part 1 研究顯示,tirzepatide 的核心器官安全性特徵與 GLP-1 RA 類別一致,但其更強的減重效果帶來了更高的膽道風險。GI 副作用是最常見的安全問題但多為可控;膽道疾病風險確實增加但絕對風險不高(NNH ≈ 149);急性胰臟炎在 RCT 層級無顯著增加,但真實世界數據存在微弱信號。GIP 成分的多器官獨立效應仍是貫穿全研究的核心未解之謎。臨床上,適當的劑量爬升策略、術前管理、膽道篩查和患者衛教是風險管理的關鍵。
參考文獻
Footnotes
-
Rosenstock J et al. (2021). SURPASS-1. Lancet. PMID: 34186022. ↩
-
Jastreboff AM et al. (2022). SURMOUNT-1. N Engl J Med. PMID: 35658024. ↩
-
Patel H et al. (2024). GI AE and weight reduction in SURPASS. Diabetes Obes Metab. PMID: 37853960. ↩ ↩2 ↩3
-
Frías JP et al. (2021). SURPASS-2. N Engl J Med. PMID: 34170647. ↩ ↩2 ↩3 ↩4
-
Jastreboff AM et al. (2022). SURMOUNT-1. N Engl J Med. PMID: 35658024. ↩ ↩2 ↩3
-
Rubino DM et al. (2025). GI tolerability SURMOUNT-1 to -4 pooled. Diabetes Obes Metab. PMID: 39789843. ↩ ↩2 ↩3
-
Karrar HRB et al. (2023). Tirzepatide GI meta-analysis. Cureus. PMID: 37908927. ↩
-
Jann JC et al. (2025). SURMOUNT-5. N Engl J Med. PMID: 40353578. ↩
-
Blonde L et al. (2024). Real-world semaglutide vs tirzepatide. JAMA Intern Med. PMID: 38976257. ↩
-
Sodhi M et al. (2023). GI AE associated with GLP-1 RA for weight loss. JAMA. PMID: 37796527. ↩ ↩2
-
Chen YH et al. (2024). FAERS tirzepatide safety profile. J Endocrinol Invest. PMID: 39141075. ↩ ↩2
-
Acute functional gastric outlet obstruction with tirzepatide (2025). Cureus. PMID: 40026949. ↩
-
Jalleh RJ et al. (2025). Delayed gastric emptying with GLP-1 RA. J Clin Endocrinol Metab. PMID: 39418085. ↩
-
Gong J et al. (2024). Biliary diseases in tirzepatide meta-analysis. J Diabetes Investig. PMID: 39569606. ↩ ↩2
-
Sharma A et al. (2022). GLP-1 RA biliary risk 76 RCTs. JAMA Intern Med. PMID: 35344001. ↩ ↩2
-
Rehfeld JF et al. (2019). CCK suppressed by GLP-1. Scand J Gastroenterol. PMID: 30449207. ↩
-
Gether IM et al. (2019). Gallbladder motility regulation. J Clin Endocrinol Metab. PMID: 30137354. ↩
-
Korean nationwide cohort (2025). Incretin and biliary diseases. Lancet Reg Health West Pac. PMC: 11992583. ↩
-
FAERS GLP-1 RA cholecystitis analysis (2025). Front Pharmacol. PMC: 12279493. ↩
-
Haal S et al. (2021). UPGRADE trial ursodiol. Lancet Gastroenterol Hepatol. PMID: 34715031. ↩
-
Kamrul-Hasan et al. (2024). Pancreatic safety of tirzepatide meta-analysis. Obesity Sci Pract. PMID: 39720158. ↩ ↩2 ↩3 ↩4
-
FAERS tirzepatide disproportionality analysis (2025). PMID: 39603650. ↩
-
Wen et al. (2025). GLP-1 RA pancreatitis/pancreatic cancer 62 RCTs. Endocrinol Diabetes Metab. PMID: 40988099. ↩
-
GI cancers RCT meta-analysis (2024). Pharmacol Res. 90 RCTs, N=124,791. ↩
-
Goldenberg R et al. (2024). GLP-1 RA and pancreatic cancer Israel cohort. JAMA Netw Open. PMID: 38175642. ↩
-
Koehler JA et al. (2012). Chronic exendin-4 and Kras mouse. Diabetes. PMID: 22266668. ↩
-
Grennan K et al. (2025). Fatal necrotizing pancreatitis with tirzepatide. JCEM Case Rep. PMID: 40270999. ↩